Номер 3, страница 18 - гдз по химии 8 класс сборник контрольных и самостоятельных работ Сеген, Власовец

Авторы: Сеген Е. А., Власовец Е. Н., Гарбар Е. Е., Синявская Т. С.
Тип: Сборник контрольных и самостоятельных работ
Издательство: Аверсэв
Год издания: 2019 - 2025
Цвет обложки: оранжевый с колбой
ISBN: 978-985-19-4532-6
Рекомендовано Научно-методическим учреждением "Национальный институт образования" Министерства образования Республики Беларусь
Популярные ГДЗ в 8 классе
Контрольная работа 4. По теме «Химическая связь», «Растворы». Вариант 3. Вариант 3 - номер 3, страница 18.
№3 (с. 18)
Решение. №3 (с. 18)
Решение 2. №3 (с. 18)
Для выбора ряда, в котором все вещества имеют только ковалентные неполярные связи, рассмотрим каждый предложенный вариант:
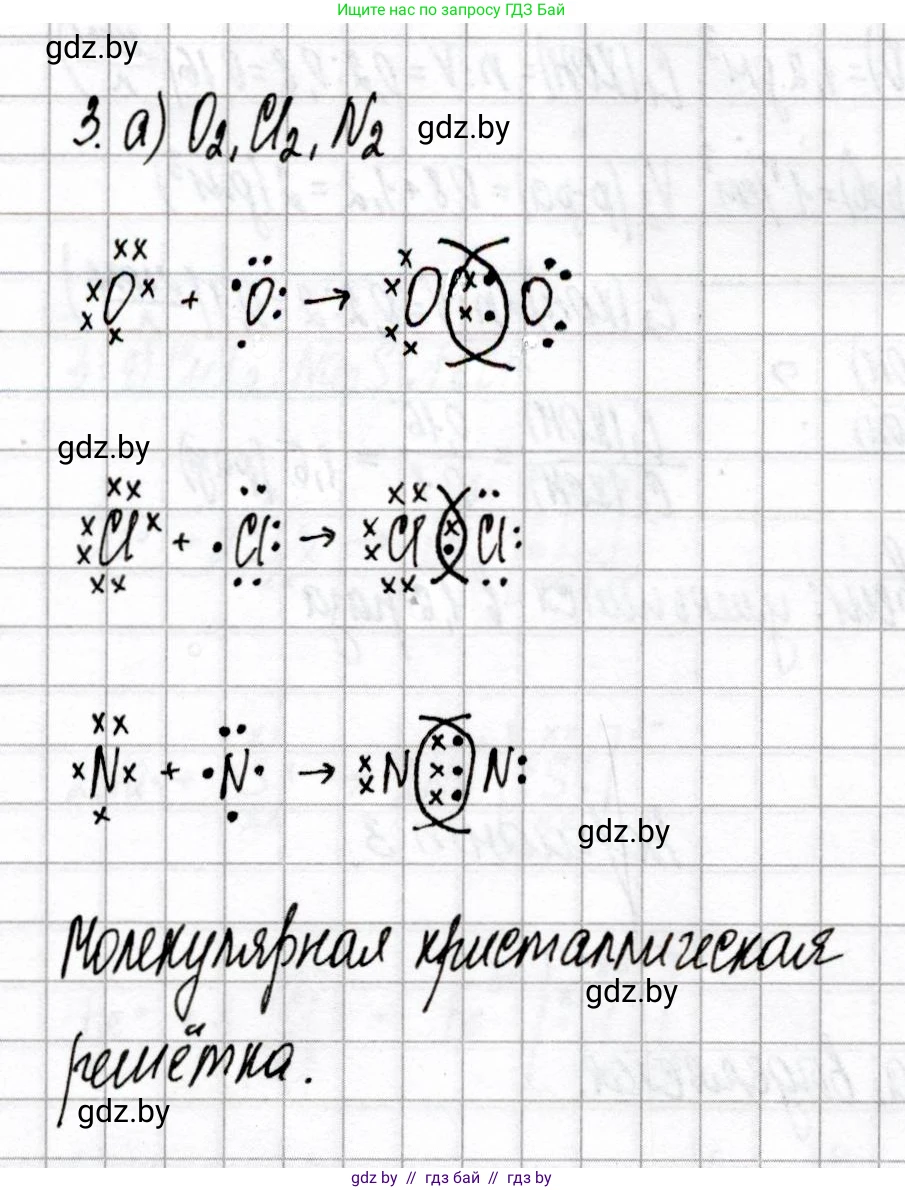
а) O2, Cl2, N2;
В молекулах O2, Cl2 и N2 связь образуется между одинаковыми атомами неметаллов (кислород-кислород, хлор-хлор, азот-азот). Разность электроотрицательностей между одинаковыми атомами равна нулю, что соответствует ковалентной неполярной связи.
б) HI, NaOH, H3PO4;
HI содержит ковалентную полярную связь (разность электроотрицательностей H и I не равна нулю). NaOH содержит ионную связь (между Na$^+$ и OH$^-$) и ковалентную полярную связь (O-H) внутри гидроксид-иона. H3PO4 содержит ковалентные полярные связи (P-O, O-H).
в) HCl, H2S, H2O;
Все эти вещества содержат ковалентные полярные связи (H-Cl, H-S, H-O), так как атомы, образующие связи, имеют разную электроотрицательность.
г) NaNO3, NaCl, H2CO3.
NaNO3 и NaCl содержат ионные связи (между Na$^+$ и NO3$^-$, а также между Na$^+$ и Cl$^-$ соответственно). В NaNO3 также присутствуют ковалентные полярные связи (N-O) внутри нитрат-иона. H2CO3 содержит ковалентные полярные связи (C-O, O-H).
Таким образом, только в ряду а) все вещества имеют исключительно ковалентные неполярные связи.
Выбранный ряд, в котором все вещества имеют только ковалентные неполярные связи:
Ряд а) O2, Cl2, N2.
Ответ: Ряд а) O2, Cl2, N2.
Схемы образования этих соединений:
Для молекулы кислорода (O2): Каждый атом кислорода имеет 6 валентных электронов. Для достижения стабильного октета атомы образуют двойную связь, и каждый атом кислорода имеет по две неподелённые электронные пары:
$: \ddot{O} = \ddot{O} :$
Для молекулы хлора (Cl2): Каждый атом хлора имеет 7 валентных электронов. Для достижения стабильного октета атомы образуют одинарную связь, и каждый атом хлора имеет по три неподелённые электронные пары:
$: \ddot{Cl} - \ddot{Cl} :$
Для молекулы азота (N2): Каждый атом азота имеет 5 валентных электронов. Для достижения стабильного октета атомы образуют тройную связь, и каждый атом азота имеет по одной неподелённой электронной паре:
$: N \equiv N :$
Ответ: Схемы образования представлены выше.
Тип кристаллической структуры, характерной для них:
Все три вещества (O2, Cl2, N2) в твердом состоянии образуют молекулярную кристаллическую решетку. Это объясняется тем, что они состоят из дискретных молекул, удерживаемых друг с другом относительно слабыми межмолекулярными силами (силами Ван-дер-Ваальса), а не сильными ковалентными связями, образующими единую структуру.
Ответ: Молекулярная кристаллическая решетка.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 3 расположенного на странице 18 к сборнику контрольных и самостоятельных работ 2019 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №3 (с. 18), авторов: Сеген (Елена Адамовна), Власовец (Евгения Николаевна), Гарбар (Елена Евгеньевна), Синявская (Тамара Степановна), учебного пособия издательства Аверсэв.













