Готовимся к олимпиадам, страница 135 - гдз по химии 8 класс учебник Шиманович, Красицкий

Авторы: Шиманович И. Е., Красицкий В. А., Сечко О. И., Хвалюк В. Н.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2024 - 2025
Цвет обложки: синий, розовый с таблицей Менделеева
ISBN: 978-985-03-2941-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава 3. Периодический закон и периодическая система химических элементов. Параграф 31. Периодический закон Д. И. Менделеева - страница 135.
Готовимся к олимпиадам (с. 135)
Условие. Готовимся к олимпиадам (с. 135)
скриншот условия
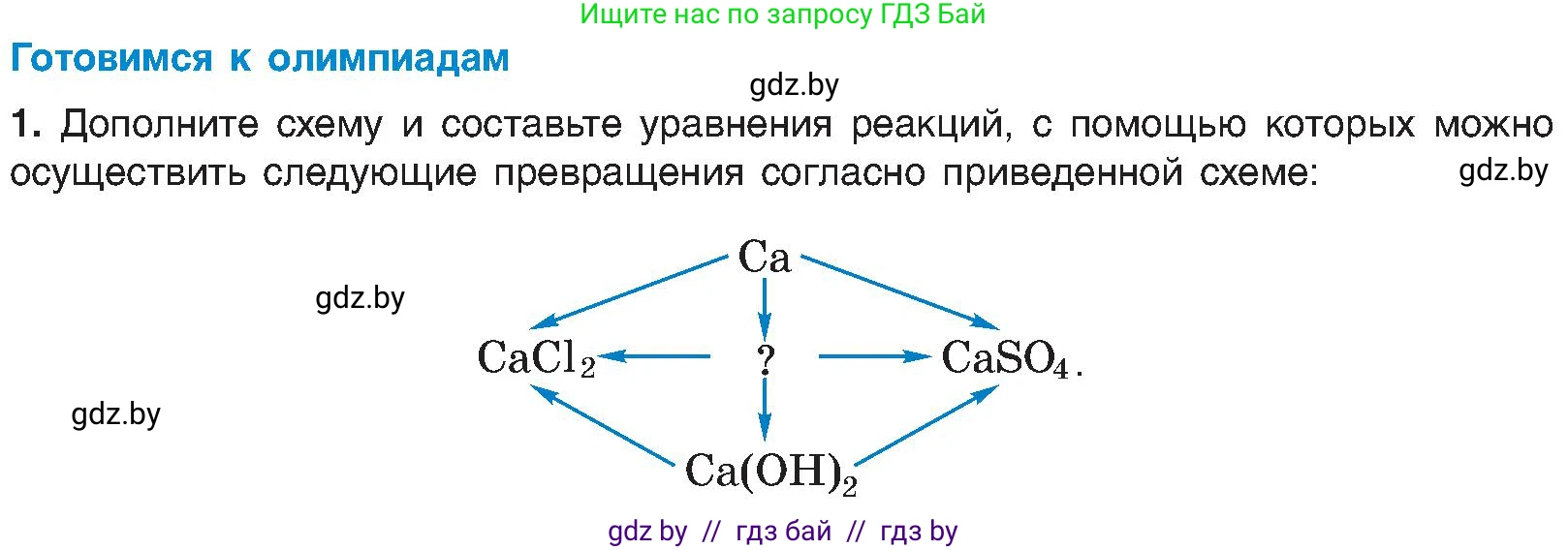
Готовимся к олимпиадам
1. Дополните схему и составьте уравнения реакций, с помощью которых можно осуществить следующие превращения согласно приведенной схеме:

Решение. Готовимся к олимпиадам (с. 135)

Решение 2. Готовимся к олимпиадам (с. 135)
В центре представленной схемы превращений находится неизвестное вещество, обозначенное вопросительным знаком. Анализ схемы показывает, что это вещество является промежуточным продуктом в цепочке превращений соединений кальция.
1. Вещество "?" образуется из металлического кальция ($Ca$).
2. Из вещества "?" можно получить гидроксид кальция ($Ca(OH)_2$).
Классическим переходом является получение оксида из металла и последующее получение гидроксида из оксида. Таким образом, наиболее вероятным веществом "?" является оксид кальция ($CaO$).
$Ca \xrightarrow{+O_2} CaO \xrightarrow{+H_2O} Ca(OH)_2$
Оксид кальция, как основной оксид, также реагирует с кислотами, образуя соли, что соответствует стрелкам, ведущим к $CaCl_2$ и $CaSO_4$.
Таким образом, неизвестное вещество (?) — это оксид кальция, $CaO$.
Ниже приведены уравнения реакций для каждого превращения на схеме.
Превращение $Ca \rightarrow CaO$
Оксид кальция получают путем сжигания металлического кальция в атмосфере кислорода.
Ответ: $2Ca + O_2 \xrightarrow{t} 2CaO$
Превращение $CaO \rightarrow Ca(OH)_2$
Оксид кальция (негашеная известь) активно реагирует с водой с образованием гидроксида кальция (гашеной извести). Реакция является экзотермической.
Ответ: $CaO + H_2O \rightarrow Ca(OH)_2$
Превращение $Ca \rightarrow CaCl_2$
Металлический кальций, как активный металл, реагирует с соляной кислотой, вытесняя из нее водород.
Ответ: $Ca + 2HCl \rightarrow CaCl_2 + H_2\uparrow$
Превращение $CaO \rightarrow CaCl_2$
Основный оксид кальция реагирует с соляной кислотой в реакции нейтрализации с образованием соли и воды.
Ответ: $CaO + 2HCl \rightarrow CaCl_2 + H_2O$
Превращение $Ca(OH)_2 \rightarrow CaCl_2$
Гидроксид кальция (основание) нейтрализуется соляной кислотой с образованием хлорида кальция и воды.
Ответ: $Ca(OH)_2 + 2HCl \rightarrow CaCl_2 + 2H_2O$
Превращение $Ca \rightarrow CaSO_4$
Кальций взаимодействует с разбавленной серной кислотой с образованием малорастворимого сульфата кальция и выделением водорода.
Ответ: $Ca + H_2SO_4 \rightarrow CaSO_4\downarrow + H_2\uparrow$
Превращение $CaO \rightarrow CaSO_4$
Оксид кальция реагирует с серной кислотой, образуя сульфат кальция и воду.
Ответ: $CaO + H_2SO_4 \rightarrow CaSO_4 + H_2O$
Превращение $Ca(OH)_2 \rightarrow CaSO_4$
Реакция нейтрализации между гидроксидом кальция и серной кислотой приводит к образованию осадка сульфата кальция и воды.
Ответ: $Ca(OH)_2 + H_2SO_4 \rightarrow CaSO_4\downarrow + 2H_2O$
Превращение $CaCl_2 \rightarrow Ca$
Металлический кальций в промышленности получают путем электролиза расплава хлорида кальция.
Ответ: $CaCl_2 \xrightarrow{электролиз \ расплава} Ca + Cl_2\uparrow$
Превращение $CaSO_4 \rightarrow Ca$
Получение кальция из сульфата — сложный процесс. В олимпиадных задачах для таких превращений может подразумеваться либо многостадийный синтез (например, алюминотермия оксида, полученного из сульфата), либо теоретически возможная реакция, например, электролиз расплава.
Ответ: $2CaSO_4 \xrightarrow{электролиз \ расплава} 2Ca + 2SO_2\uparrow + O_2\uparrow$
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения Готовимся к олимпиадам расположенного на странице 135 к учебнику 2024 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению Готовимся к олимпиадам (с. 135), авторов: Шиманович (Игорь Евгеньевич), Красицкий (Василий Анатольевич), Сечко (Ольга Ивановна), Хвалюк (Виктор Николаевич), учебного пособия издательства Адукацыя i выхаванне.













