Номер 5, страница 59 - гдз по химии 8 класс учебник Шиманович, Красицкий

Авторы: Шиманович И. Е., Красицкий В. А., Сечко О. И., Хвалюк В. Н.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2024 - 2025
Цвет обложки: синий, розовый с таблицей Менделеева
ISBN: 978-985-03-2941-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава 2. Важнейшие классы неорганических соединений. Параграф 13. Химические свойства кислотных оксидов - номер 5, страница 59.
№5 (с. 59)
Условие. №5 (с. 59)
скриншот условия

5. Рассчитайте массу серной кислоты, образовавшейся в результате реакции соответствующего ей кислотного оксида массой 36 г с водой.
Решение. №5 (с. 59)
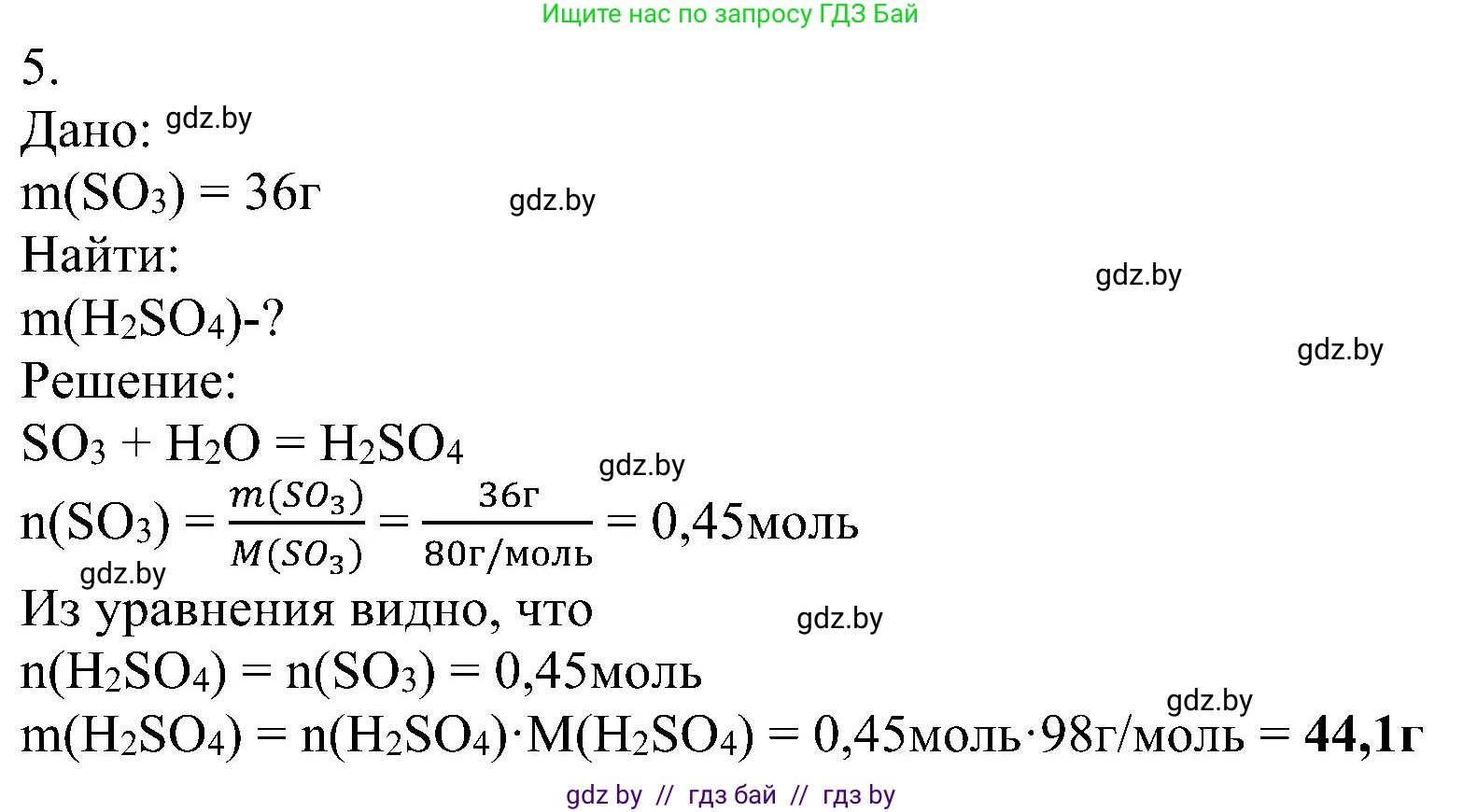
Решение 2. №5 (с. 59)
5.
Дано:
Масса кислотного оксида, соответствующего серной кислоте - $m(\text{оксида}) = 36$ г.
$m(\text{оксида}) = 36 \text{ г} = 0.036 \text{ кг}$Найти:
Массу серной кислоты - $m(H_2SO_4)$ - ?
Решение:
1. Сначала определим, какой кислотный оксид соответствует серной кислоте ($H_2SO_4$). В серной кислоте степень окисления серы равна +6. Следовательно, соответствующим ей кислотным оксидом является оксид серы(VI), химическая формула которого $SO_3$.
2. Запишем уравнение химической реакции взаимодействия оксида серы(VI) с водой. В результате этой реакции образуется серная кислота:
$SO_3 + H_2O \rightarrow H_2SO_4$
Уравнение реакции сбалансировано. Из стехиометрических коэффициентов видно, что из 1 моль оксида серы(VI) образуется 1 моль серной кислоты. Таким образом, их количества вещества соотносятся как 1:1.
$n(SO_3) = n(H_2SO_4)$
3. Рассчитаем молярные массы ($M$) оксида серы(VI) и серной кислоты. Для этого воспользуемся значениями относительных атомных масс элементов из Периодической таблицы Д.И. Менделеева: $Ar(S) = 32$, $Ar(O) = 16$, $Ar(H) = 1$.
Молярная масса оксида серы(VI):
$M(SO_3) = Ar(S) + 3 \cdot Ar(O) = 32 + 3 \cdot 16 = 32 + 48 = 80 \text{ г/моль}$
Молярная масса серной кислоты:
$M(H_2SO_4) = 2 \cdot Ar(H) + Ar(S) + 4 \cdot Ar(O) = 2 \cdot 1 + 32 + 4 \cdot 16 = 2 + 32 + 64 = 98 \text{ г/моль}$
4. Найдем количество вещества ($n$) оксида серы(VI) массой 36 г, используя формулу $n = \frac{m}{M}$:
$n(SO_3) = \frac{m(SO_3)}{M(SO_3)} = \frac{36 \text{ г}}{80 \text{ г/моль}} = 0.45 \text{ моль}$
5. Согласно уравнению реакции, количество вещества образовавшейся серной кислоты равно количеству вещества прореагировавшего оксида серы(VI):
$n(H_2SO_4) = n(SO_3) = 0.45 \text{ моль}$
6. Теперь можем рассчитать массу серной кислоты, которая образовалась в результате реакции, по формуле $m = n \cdot M$:
$m(H_2SO_4) = n(H_2SO_4) \cdot M(H_2SO_4) = 0.45 \text{ моль} \cdot 98 \text{ г/моль} = 44.1 \text{ г}$
Ответ: масса образовавшейся серной кислоты равна 44,1 г.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 5 расположенного на странице 59 к учебнику 2024 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №5 (с. 59), авторов: Шиманович (Игорь Евгеньевич), Красицкий (Василий Анатольевич), Сечко (Ольга Ивановна), Хвалюк (Виктор Николаевич), учебного пособия издательства Адукацыя i выхаванне.













