Номер 11, страница 90 - гдз по химии 8 класс учебник Шиманович, Красицкий

Авторы: Шиманович И. Е., Красицкий В. А., Сечко О. И., Хвалюк В. Н.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2024 - 2025
Цвет обложки: синий, розовый с таблицей Менделеева
ISBN: 978-985-03-2941-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава 2. Важнейшие классы неорганических соединений. Параграф 21. Химические свойства оснований - номер 11, страница 90.
№11 (с. 90)
Условие. №11 (с. 90)
скриншот условия

11. Углекислый газ прореагировал со щёлочью, в результате чего образовался карбонат натрия массой 21,2 г. Найдите объем исходного углекислого газа и массу прореагировавшей с ним щёлочи.
Решение. №11 (с. 90)
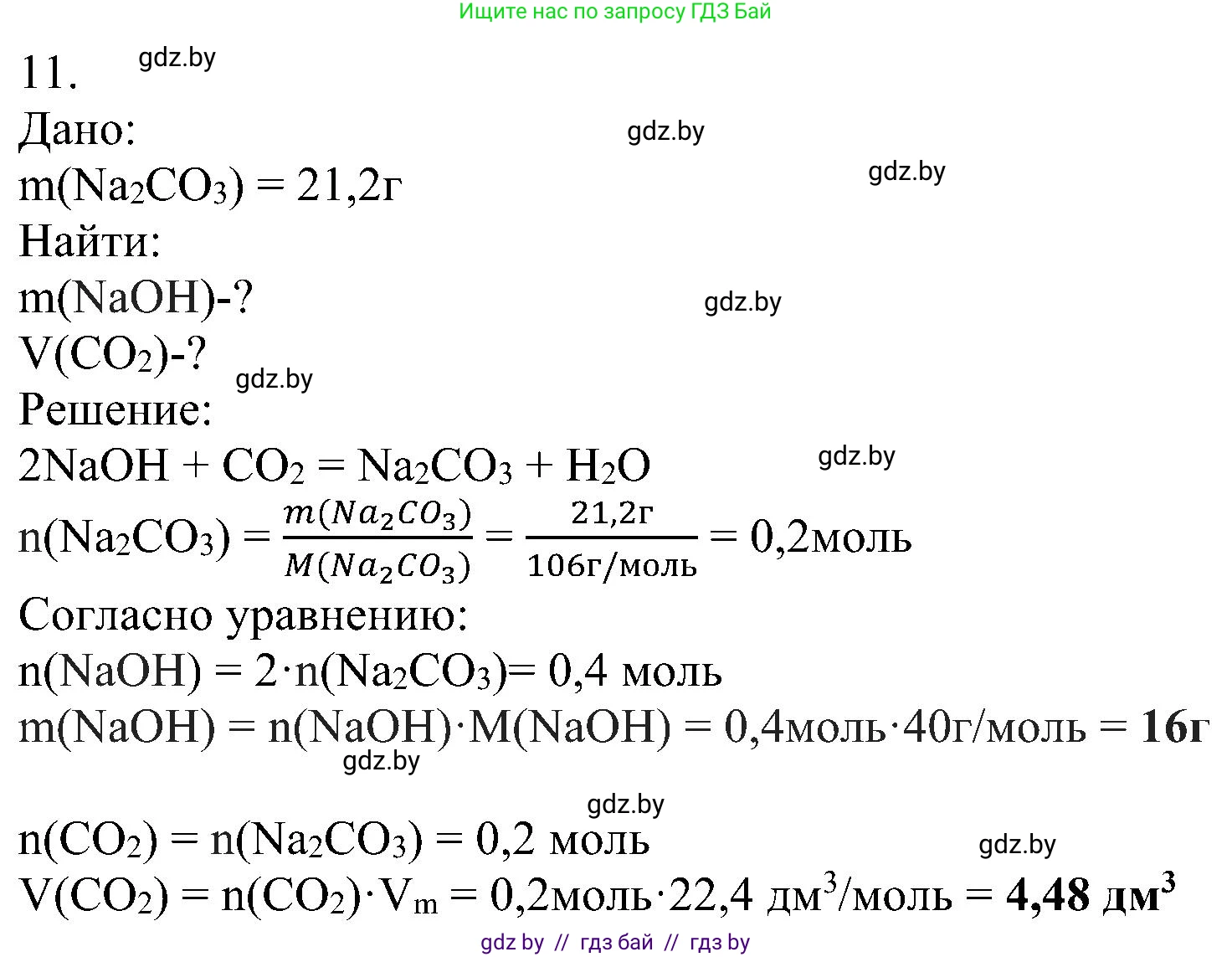
Решение 2. №11 (с. 90)
Дано:
$m(Na_2CO_3) = 21,2$ г
Найти:
$V(CO_2) - ?$
$m(щёлочи) - ?$
Решение:
1. В результате реакции углекислого газа ($CO_2$) со щёлочью образовался карбонат натрия ($Na_2CO_3$). Это означает, что в качестве щёлочи выступал гидроксид натрия ($NaOH$). Запишем уравнение реакции:
$CO_2 + 2NaOH \rightarrow Na_2CO_3 + H_2O$
2. Рассчитаем молярную массу карбоната натрия ($Na_2CO_3$):
$M(Na_2CO_3) = 2 \cdot M(Na) + M(C) + 3 \cdot M(O) = 2 \cdot 23 + 12 + 3 \cdot 16 = 46 + 12 + 48 = 106$ г/моль.
3. Найдем количество вещества (моль) образовавшегося карбоната натрия:
$n(Na_2CO_3) = \frac{m(Na_2CO_3)}{M(Na_2CO_3)} = \frac{21,2 \text{ г}}{106 \text{ г/моль}} = 0,2$ моль.
4. По уравнению реакции определим количество вещества углекислого газа и гидроксида натрия, вступивших в реакцию. Соотношение количеств веществ реагентов и продуктов составляет:
$n(CO_2) : n(NaOH) : n(Na_2CO_3) = 1 : 2 : 1$
Следовательно, количество вещества углекислого газа равно:
$n(CO_2) = n(Na_2CO_3) = 0,2$ моль.
А количество вещества гидроксида натрия:
$n(NaOH) = 2 \cdot n(Na_2CO_3) = 2 \cdot 0,2 = 0,4$ моль.
5. Теперь можем найти объем исходного углекислого газа, считая, что реакция протекает при нормальных условиях (н.у.), где молярный объем газа $V_m = 22,4$ л/моль:
$V(CO_2) = n(CO_2) \cdot V_m = 0,2 \text{ моль} \cdot 22,4 \text{ л/моль} = 4,48$ л.
6. Рассчитаем массу прореагировавшей щёлочи (гидроксида натрия). Сначала найдем молярную массу $NaOH$:
$M(NaOH) = M(Na) + M(O) + M(H) = 23 + 16 + 1 = 40$ г/моль.
Теперь найдем массу щёлочи:
$m(NaOH) = n(NaOH) \cdot M(NaOH) = 0,4 \text{ моль} \cdot 40 \text{ г/моль} = 16$ г.
Ответ: объем исходного углекислого газа составляет 4,48 л, а масса прореагировавшей с ним щёлочи - 16 г.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 11 расположенного на странице 90 к учебнику 2024 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №11 (с. 90), авторов: Шиманович (Игорь Евгеньевич), Красицкий (Василий Анатольевич), Сечко (Ольга Ивановна), Хвалюк (Виктор Николаевич), учебного пособия издательства Адукацыя i выхаванне.













