Номер 160, страница 38 - гдз по химии 8 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2019 - 2025
Цвет обложки: голубой, зелёный с кристаллами
ISBN: 978-985-599-064-3
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава І. Важнейшие классы неорганических соединений. Параграф 12. Получение и применение оксидов - номер 160, страница 38.
№160 (с. 38)
Условие. №160 (с. 38)
скриншот условия

160. С помощью каких (не менее двух) химических реакций можно получить:
а) оксид алюминия;
б) оксид кальция;
в) оксид углерода(IV)?
Составьте уравнения соответствующих химических реакций.
Решение. №160 (с. 38)
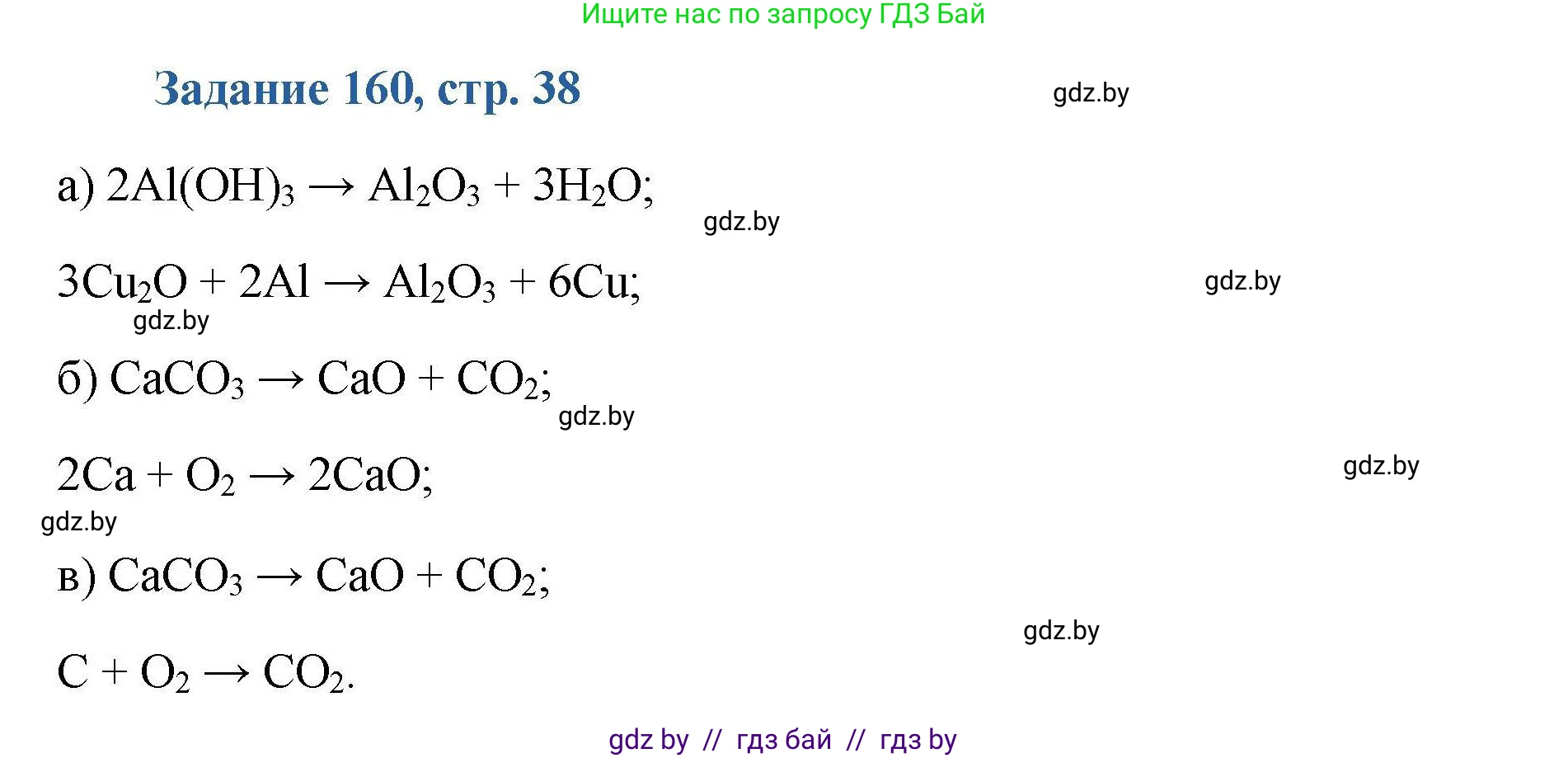
Решение 2. №160 (с. 38)
а) оксид алюминия
Оксид алюминия ($Al_2O_3$) можно получить несколькими способами. Вот два из них:
1. Прямое окисление алюминия кислородом. При нагревании алюминий активно реагирует с кислородом, образуя оксидную пленку, а в виде порошка — сгорает:
$4Al + 3O_2 \xrightarrow{t} 2Al_2O_3$
2. Термическое разложение гидроксида алюминия. Гидроксид алюминия является нерастворимым основанием и при нагревании разлагается на соответствующий оксид и воду:
$2Al(OH)_3 \xrightarrow{t} Al_2O_3 + 3H_2O$
Ответ: Оксид алюминия можно получить реакцией горения алюминия в кислороде ($4Al + 3O_2 \xrightarrow{t} 2Al_2O_3$) или термическим разложением гидроксида алюминия ($2Al(OH)_3 \xrightarrow{t} Al_2O_3 + 3H_2O$).
б) оксид кальция
Оксид кальция ($CaO$), известный как негашеная известь, можно получить следующими реакциями:
1. Термическое разложение карбоната кальция (известняка, мела, мрамора). Это основной промышленный метод получения оксида кальция:
$CaCO_3 \xrightarrow{t} CaO + CO_2 \uparrow$
2. Прямое взаимодействие металлического кальция с кислородом при нагревании:
$2Ca + O_2 \xrightarrow{t} 2CaO$
Ответ: Оксид кальция можно получить термическим разложением карбоната кальция ($CaCO_3 \xrightarrow{t} CaO + CO_2 \uparrow$) или горением кальция в кислороде ($2Ca + O_2 \xrightarrow{t} 2CaO$).
в) оксид углерода(IV)
Оксид углерода(IV) ($CO_2$), или углекислый газ, можно получить множеством способов, например:
1. Сжигание углерода или углеродсодержащих веществ (например, угля, метана, древесины) в избытке кислорода:
$C + O_2 \xrightarrow{t} CO_2$
2. Действие сильных кислот на карбонаты или гидрокарбонаты. Это распространенный лабораторный способ получения углекислого газа:
$CaCO_3 + 2HCl \rightarrow CaCl_2 + H_2O + CO_2 \uparrow$
Ответ: Оксид углерода(IV) можно получить сжиганием углерода в избытке кислорода ($C + O_2 \xrightarrow{t} CO_2$) или действием сильной кислоты, например, соляной, на карбонат кальция ($CaCO_3 + 2HCl \rightarrow CaCl_2 + H_2O + CO_2 \uparrow$).
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 160 расположенного на странице 38 к сборнику задач 2019 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №160 (с. 38), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.













