Номер 382, страница 71 - гдз по химии 8 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2019 - 2025
Цвет обложки: голубой, зелёный с кристаллами
ISBN: 978-985-599-064-3
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава II. Периодический закон и периодическая система химических элементов. Параграф 26. Естественные семейства элементов - номер 382, страница 71.
№382 (с. 71)
Условие. №382 (с. 71)
скриншот условия
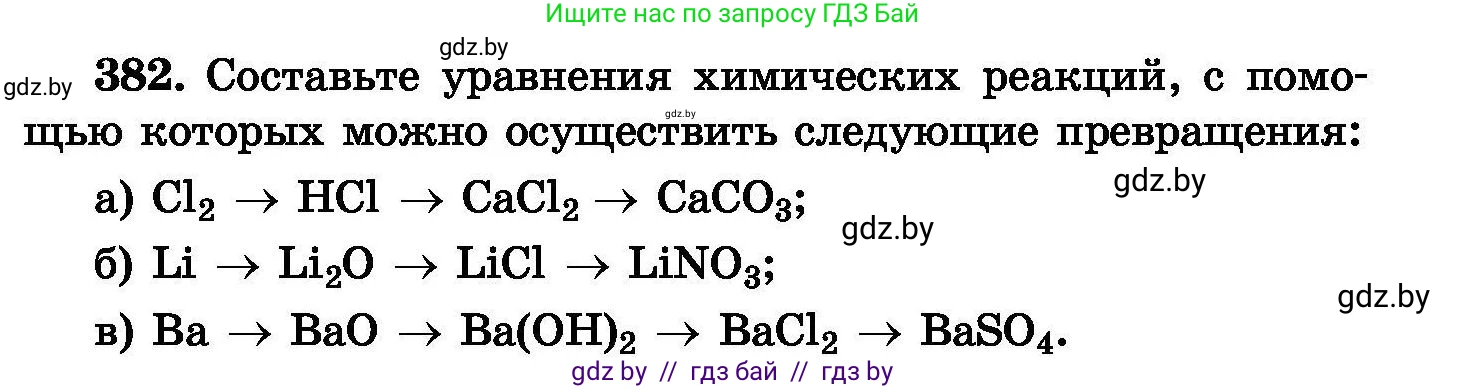
382. Составьте уравнения химических реакций, с помощью которых можно осуществить следующие превращения:
а) $Cl_2 \to HCl \to CaCl_2 \to CaCO_3$;
б) $Li \to Li_2O \to LiCl \to LiNO_3$;
в) $Ba \to BaO \to Ba(OH)_2 \to BaCl_2 \to BaSO_4$.
Решение. №382 (с. 71)

Решение 2. №382 (с. 71)
а) $Cl_2 \rightarrow HCl \rightarrow CaCl_2 \rightarrow CaCO_3$
Решение:
1. Для получения хлороводорода (соляной кислоты) из хлора, необходимо провести реакцию хлора с водородом. Это реакция соединения, протекающая при нагревании или под действием ультрафиолетового излучения.
$H_2 + Cl_2 \rightarrow 2HCl$
2. Чтобы из соляной кислоты получить хлорид кальция, можно использовать реакцию нейтрализации с основанием, например, с гидроксидом кальция, или реакцию с основным оксидом (оксидом кальция), или с самим металлом кальцием.
Возьмем реакцию с гидроксидом кальция:
$2HCl + Ca(OH)_2 \rightarrow CaCl_2 + 2H_2O$
3. Карбонат кальция — это нерастворимая соль. Её можно получить из хлорида кальция путем реакции ионного обмена с другой растворимой солью, содержащей карбонат-ион, например, с карбонатом натрия. В результате реакции выпадет белый осадок карбоната кальция.
$CaCl_2 + Na_2CO_3 \rightarrow CaCO_3\downarrow + 2NaCl$
Ответ:
$H_2 + Cl_2 \rightarrow 2HCl$
$2HCl + Ca(OH)_2 \rightarrow CaCl_2 + 2H_2O$
$CaCl_2 + Na_2CO_3 \rightarrow CaCO_3\downarrow + 2NaCl$
б) $Li \rightarrow Li_2O \rightarrow LiCl \rightarrow LiNO_3$
Решение:
1. Оксид лития можно получить при сжигании металлического лития в кислороде. Это реакция соединения.
$4Li + O_2 \rightarrow 2Li_2O$
2. Оксид лития является основным оксидом, поэтому он реагирует с кислотами с образованием соли и воды. Для получения хлорида лития нужно провести реакцию с соляной кислотой.
$Li_2O + 2HCl \rightarrow 2LiCl + H_2O$
3. Для превращения хлорида лития в нитрат лития можно использовать реакцию обмена с нитратом серебра. Так как хлорид серебра является нерастворимым соединением, он выпадет в осадок, а в растворе останется нитрат лития.
$LiCl + AgNO_3 \rightarrow LiNO_3 + AgCl\downarrow$
Ответ:
$4Li + O_2 \rightarrow 2Li_2O$
$Li_2O + 2HCl \rightarrow 2LiCl + H_2O$
$LiCl + AgNO_3 \rightarrow LiNO_3 + AgCl\downarrow$
в) $Ba \rightarrow BaO \rightarrow Ba(OH)_2 \rightarrow BaCl_2 \rightarrow BaSO_4$
Решение:
1. Оксид бария образуется при реакции металлического бария с кислородом при нагревании.
$2Ba + O_2 \rightarrow 2BaO$
2. Оксид бария — оксид щелочноземельного металла, он активно реагирует с водой с образованием соответствующего гидроксида — гидроксида бария, который является щелочью.
$BaO + H_2O \rightarrow Ba(OH)_2$
3. Для получения соли (хлорида бария) из основания (гидроксида бария) необходимо провести реакцию нейтрализации с кислотой (соляной кислотой).
$Ba(OH)_2 + 2HCl \rightarrow BaCl_2 + 2H_2O$
4. Сульфат бария является нерастворимой солью, что позволяет получить его с помощью реакции ионного обмена. Для этого к раствору хлорида бария нужно добавить вещество, содержащее сульфат-ионы, например, серную кислоту или её растворимую соль (например, сульфат натрия).
$BaCl_2 + H_2SO_4 \rightarrow BaSO_4\downarrow + 2HCl$
Ответ:
$2Ba + O_2 \rightarrow 2BaO$
$BaO + H_2O \rightarrow Ba(OH)_2$
$Ba(OH)_2 + 2HCl \rightarrow BaCl_2 + 2H_2O$
$BaCl_2 + H_2SO_4 \rightarrow BaSO_4\downarrow + 2HCl$
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 382 расположенного на странице 71 к сборнику задач 2019 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №382 (с. 71), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.













