Номер 1094, страница 174 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 6. Неметаллы. Параграф 38. Азотная кислота - номер 1094, страница 174.
№1094 (с. 174)
Условие. №1094 (с. 174)
скриншот условия

1094. Рассчитайте относительную плотность (по азоту) газа, который выделяется при прокаливании нитрата серебра.
Решение. №1094 (с. 174)
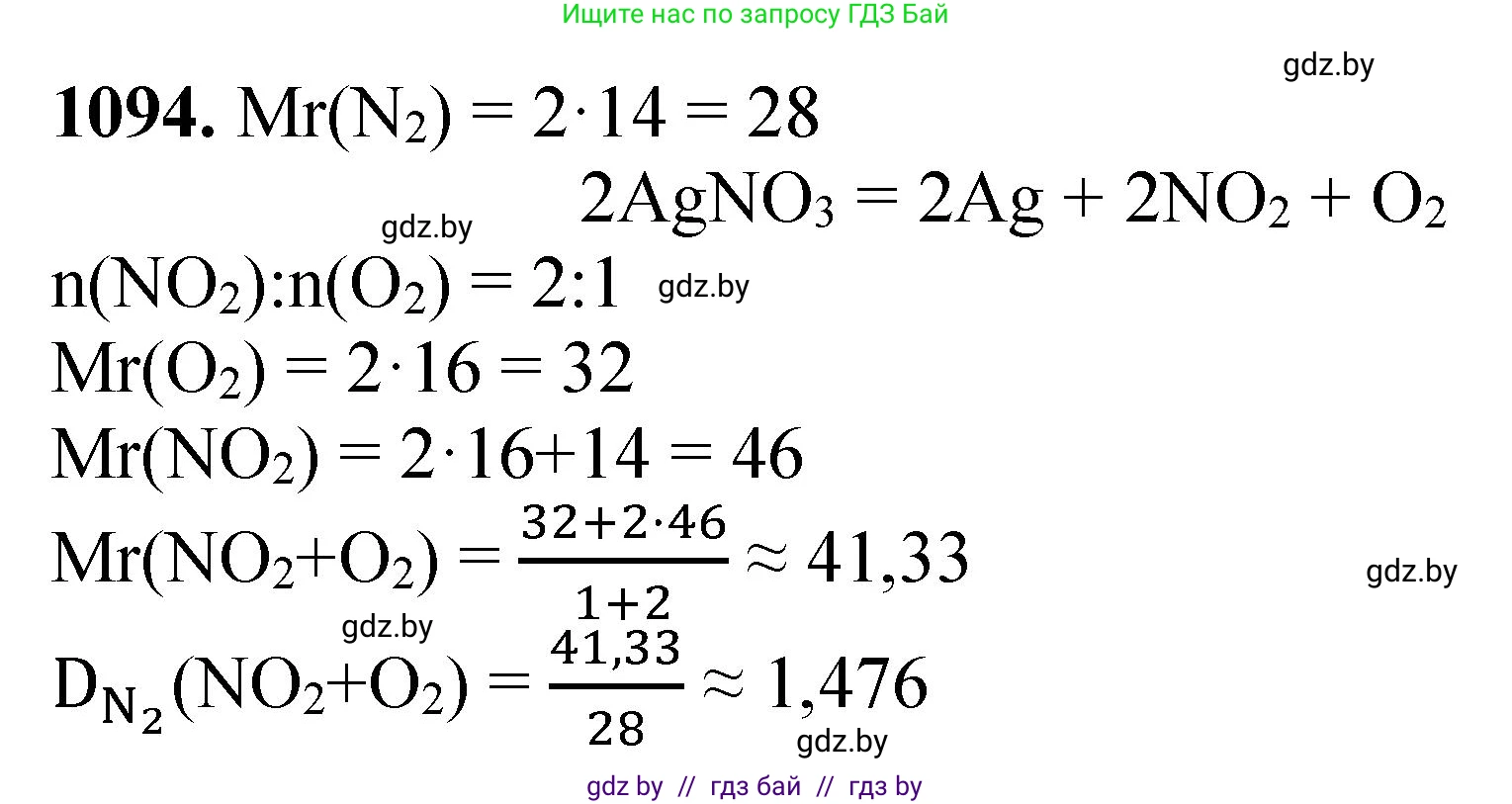
Решение 3. №1094 (с. 174)
Дано:
Вещество: нитрат серебра ($\text{AgNO}_3$)
Процесс: прокаливание
Газ для сравнения: азот ($\text{N}_2$)
Найти:
Относительную плотность ($D$) газовой смеси по азоту - $D_{\text{N}_2}(\text{смеси})$
Решение:
1. Первым шагом запишем уравнение реакции термического разложения (прокаливания) нитрата серебра. Нитраты металлов, стоящих в ряду электрохимической активности правее меди (включая серебро), разлагаются при нагревании с образованием свободного металла, диоксида азота и кислорода.
Уравнение реакции:
$2\text{AgNO}_3 \xrightarrow{t^\circ} 2\text{Ag} + 2\text{NO}_2\uparrow + \text{O}_2\uparrow$
Из уравнения видно, что в результате реакции выделяется смесь двух газов: диоксида азота ($\text{NO}_2$) и кислорода ($\text{O}_2$).
2. Определим состав газовой смеси. Согласно стехиометрическим коэффициентам в уравнении реакции, на каждые 2 моля выделившегося диоксида азота приходится 1 моль кислорода. Таким образом, их молярное соотношение в смеси составляет:
$\nu(\text{NO}_2) : \nu(\text{O}_2) = 2 : 1$
3. Рассчитаем среднюю молярную массу полученной газовой смеси ($M_{ср}$). Для этого сначала найдем молярные массы каждого газа, используя относительные атомные массы элементов: $Ar(\text{N}) \approx 14$, $Ar(\text{O}) \approx 16$.
$M(\text{NO}_2) = Ar(\text{N}) + 2 \cdot Ar(\text{O}) = 14 + 2 \cdot 16 = 46$ г/моль
$M(\text{O}_2) = 2 \cdot Ar(\text{O}) = 2 \cdot 16 = 32$ г/моль
Средняя молярная масса смеси вычисляется как средневзвешенное значение молярных масс компонентов с учетом их мольных долей. Общее количество молей в условной порции смеси равно $2 + 1 = 3$ моль.
Мольная доля $\text{NO}_2$: $\chi(\text{NO}_2) = \frac{2}{3}$
Мольная доля $\text{O}_2$: $\chi(\text{O}_2) = \frac{1}{3}$
Средняя молярная масса смеси:
$M_{ср}(\text{смеси}) = \chi(\text{NO}_2) \cdot M(\text{NO}_2) + \chi(\text{O}_2) \cdot M(\text{O}_2) = \frac{2}{3} \cdot 46 + \frac{1}{3} \cdot 32 = \frac{92 + 32}{3} = \frac{124}{3} \approx 41.33$ г/моль
4. Теперь рассчитаем относительную плотность газовой смеси по азоту. Относительная плотность газа A по газу B ($D_B(A)$) - это безразмерная величина, показывающая, во сколько раз газ A тяжелее газа B, и рассчитывается как отношение их молярных масс.
$D_B(A) = \frac{M(A)}{M(B)}$
Молярная масса азота ($\text{N}_2$):
$M(\text{N}_2) = 2 \cdot Ar(\text{N}) = 2 \cdot 14 = 28$ г/моль
Относительная плотность смеси по азоту:
$D_{\text{N}_2}(\text{смеси}) = \frac{M_{ср}(\text{смеси})}{M(\text{N}_2)} = \frac{124/3}{28} = \frac{124}{3 \cdot 28} = \frac{124}{84} = \frac{31}{21} \approx 1.48$
Ответ: относительная плотность газовой смеси по азоту составляет примерно $1.48$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 1094 расположенного на странице 174 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №1094 (с. 174), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














