Номер 8, страница 294 - гдз по химии 11 класс учебник Мычко, Прохоревич

Авторы: Мычко Д. И., Прохоревич К. Н., Борушко И. И.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2021 - 2025
Цвет обложки: зелёный с колбами
ISBN: 978-985-599-297-5
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава VIII. Химические вещества в жизни и деятельности человека. Параграф 53. Охрана окружающей среды от вредного воздействия химических веществ. «Зелёная химия» - номер 8, страница 294.
№8 (с. 294)
Условия. №8 (с. 294)
скриншот условия

8. На основании известных вам реакций с участием металлов предложите метод извлечения меди из отработанного раствора гальванического меднения, содержащего сульфат меди.
Решение. №8 (с. 294)
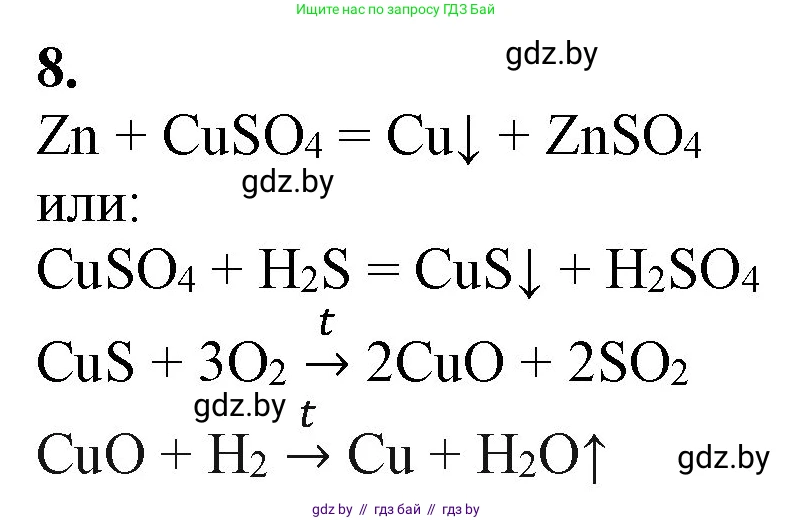
Решение 2. №8 (с. 294)
Дано:
Отработанный раствор гальванического меднения, содержащий сульфат меди ($CuSO_4$).
Найти:
Метод извлечения металлической меди ($Cu$) из данного раствора.
Решение:
Для извлечения меди из раствора ее соли (сульфата меди) можно использовать метод, основанный на вытеснении одного металла другим, более активным. Этот процесс также называют цементацией. Положение металлов в электрохимическом ряду напряжений определяет их относительную химическую активность. Металлы, стоящие в этом ряду левее (до) меди, являются более активными и способны вытеснять ее из растворов ее солей.
Электрохимический ряд напряжений (фрагмент):
... $Mg$ ... $Al$ ... $Zn$ ... $Fe$ ... $H_2$ ... $Cu$ ... $Ag$ ...
Из ряда видно, что такие металлы, как железо ($Fe$), цинк ($Zn$) или алюминий ($Al$), активнее меди ($Cu$). Наиболее экономически целесообразно использовать железные стружки или лом, так как железо является дешевым и доступным металлом.
Процедура извлечения меди будет следующей:
В отработанный раствор сульфата меди, имеющий характерный голубой цвет из-за присутствия ионов $Cu^{2+}$, помещают избыток железных стружек или гвоздей.
Происходит реакция замещения. Более активное железо растворяется, переходя в раствор в виде ионов $Fe^{2+}$, а менее активная медь восстанавливается до металлического состояния и выпадает в осадок в виде красно-коричневого порошка.
За ходом реакции можно наблюдать по изменению цвета раствора (голубая окраска постепенно исчезает, сменяясь на бледно-зеленую, характерную для солей железа(II)) и по образованию осадка меди на поверхности железа.
Уравнение химической реакции в молекулярном виде:
$Fe(тв) + CuSO_4(р-р) \rightarrow FeSO_4(р-р) + Cu(тв)\downarrow$
После завершения реакции, когда весь сульфат меди прореагирует (раствор перестанет быть голубым), полученную смесь фильтруют. Осадок на фильтре, состоящий из меди и остатков непрореагировавшего железа, промывают водой для удаления остатков раствора сульфата железа. При необходимости, для очистки меди от избытка железа, осадок можно обработать разбавленной соляной или серной кислотой (железо будет реагировать с кислотой, а медь — нет). После этого чистую медь промывают водой и высушивают.
Таким образом, с помощью простой химической реакции можно эффективно извлечь медь из отработанного гальванического раствора.
Ответ: Для извлечения меди из отработанного раствора сульфата меди можно использовать метод цементации, добавив в раствор более активный металл, например, железные стружки. Железо вытеснит медь из раствора соли в соответствии с реакцией $Fe + CuSO_4 \rightarrow FeSO_4 + Cu\downarrow$. Выпавшую в осадок металлическую медь затем отделяют фильтрованием, промывают и высушивают.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 8 расположенного на странице 294 к учебнику 2021 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №8 (с. 294), авторов: Мычко (Дмитрий Иванович), Прохоревич (Константин Николаевич), Борушко (Ирина Ивановна), учебного пособия издательства Адукацыя i выхаванне.













