Номер 2, страница 188 - гдз по химии 8 класс учебник Шиманович, Красицкий

Авторы: Шиманович И. Е., Красицкий В. А., Сечко О. И., Хвалюк В. Н.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2024 - 2025
Цвет обложки: синий, розовый с таблицей Менделеева
ISBN: 978-985-03-2941-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава 5. Химическая связь. Параграф 45. Ионная связь - номер 2, страница 188.
№2 (с. 188)
Условие. №2 (с. 188)
скриншот условия

2. Составьте схемы образования ионов $ \text{Mg}^{2+} $, $ \text{Al}^{3+} $, $ \text{S}^{2-} $, $ \text{Ca}^{2+} $, $ \text{I}^{-} $ из соответствующих атомов.
Решение. №2 (с. 188)
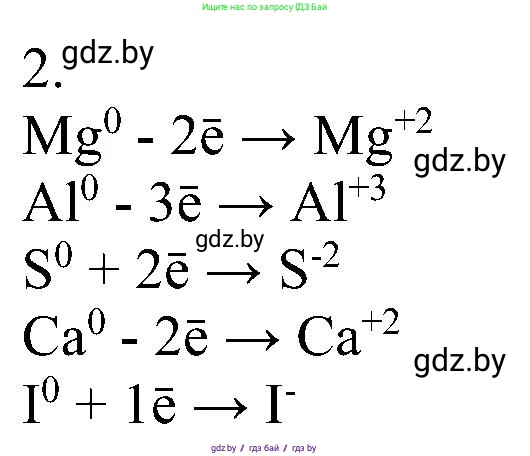
Решение 2. №2 (с. 188)
Решение
Ионы образуются из нейтральных атомов в результате отдачи или присоединения электронов. Атомы металлов, как правило, отдают электроны с внешнего энергетического уровня, превращаясь в положительно заряженные ионы (катионы). Атомы неметаллов, как правило, принимают электроны на внешний энергетический уровень, чтобы его завершить, превращаясь в отрицательно заряженные ионы (анионы). В обоих случаях атом стремится приобрести устойчивую электронную конфигурацию, чаще всего соответствующую конфигурации ближайшего благородного газа.
Mg²⁺
Атом магния ($Mg$) — металл, расположен во 2-й группе, 3-м периоде. Его порядковый номер 12. Электронная конфигурация атома: $1s^22s^22p^63s^2$. На внешнем энергетическом уровне находятся 2 электрона. Чтобы достичь стабильной электронной конфигурации, атому магния легче отдать эти 2 электрона, чем принять 6. При потере двух электронов образуется положительно заряженный ион (катион) магния $Mg^{2+}$.
Схема образования иона:
$Mg^0 - 2e^- \rightarrow Mg^{2+}$
В результате ион $Mg^{2+}$ приобретает электронную конфигурацию $1s^22s^22p^6$, как у благородного газа неона ($Ne$).
Ответ: $Mg^0 - 2e^- \rightarrow Mg^{2+}$
Al³⁺
Атом алюминия ($Al$) — металл, расположен в 13-й группе, 3-м периоде. Его порядковый номер 13. Электронная конфигурация атома: $1s^22s^22p^63s^23p^1$. На внешнем энергетическом уровне находятся 3 электрона. Атом алюминия отдает эти 3 валентных электрона, превращаясь в катион $Al^{3+}$.
Схема образования иона:
$Al^0 - 3e^- \rightarrow Al^{3+}$
Ион $Al^{3+}$ приобретает стабильную электронную конфигурацию $1s^22s^22p^6$, как у благородного газа неона ($Ne$).
Ответ: $Al^0 - 3e^- \rightarrow Al^{3+}$
S²⁻
Атом серы ($S$) — неметалл, расположен в 16-й группе, 3-м периоде. Его порядковый номер 16. Электронная конфигурация атома: $1s^22s^22p^63s^23p^4$. На внешнем энергетическом уровне находятся 6 электронов. Для завершения внешнего уровня до стабильного октета (8 электронов) атому серы энергетически выгоднее принять 2 электрона, чем отдать 6. Принимая 2 электрона, он превращается в отрицательно заряженный ион (анион) серы $S^{2-}$.
Схема образования иона:
$S^0 + 2e^- \rightarrow S^{2-}$
Ион $S^{2-}$ приобретает электронную конфигурацию $1s^22s^22p^63s^23p^6$, как у благородного газа аргона ($Ar$).
Ответ: $S^0 + 2e^- \rightarrow S^{2-}$
Ca²⁺
Атом кальция ($Ca$) — металл, расположен во 2-й группе, 4-м периоде. Его порядковый номер 20. Электронная конфигурация атома: $1s^22s^22p^63s^23p^64s^2$. На внешнем энергетическом уровне находятся 2 электрона. Атом кальция отдает эти 2 электрона для достижения стабильной конфигурации, превращаясь в катион $Ca^{2+}$.
Схема образования иона:
$Ca^0 - 2e^- \rightarrow Ca^{2+}$
Ион $Ca^{2+}$ приобретает электронную конфигурацию $1s^22s^22p^63s^23p^6$, как у благородного газа аргона ($Ar$).
Ответ: $Ca^0 - 2e^- \rightarrow Ca^{2+}$
I⁻
Атом йода ($I$) — неметалл (галоген), расположен в 17-й группе, 5-м периоде. Его порядковый номер 53. Электронная конфигурация внешнего уровня: $...5s^25p^5$. На внешнем энергетическом уровне находятся 7 электронов. Для завершения внешнего уровня до стабильного октета атому йода необходимо принять 1 электрон. Принимая электрон, он превращается в анион $I^{-}$.
Схема образования иона:
$I^0 + 1e^- \rightarrow I^{-}$
Ион $I^{-}$ приобретает электронную конфигурацию внешнего уровня $...5s^25p^6$, как у благородного газа ксенона ($Xe$).
Ответ: $I^0 + 1e^- \rightarrow I^{-}$
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 2 расположенного на странице 188 к учебнику 2024 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №2 (с. 188), авторов: Шиманович (Игорь Евгеньевич), Красицкий (Василий Анатольевич), Сечко (Ольга Ивановна), Хвалюк (Виктор Николаевич), учебного пособия издательства Адукацыя i выхаванне.













