Номер 722, страница 120 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 5. Химия растворов. Параграф 27. Химические свойства кислот, оснований, солей в свете теории электролитической диссоциации - номер 722, страница 120.
№722 (с. 120)
Условие. №722 (с. 120)
скриншот условия

722. В трёх пробирках без надписей находятся растворы карбоната калия, нитрата серебра, сульфата натрия. С помощью каких веществ можно определить, в какой из пробирок находится каждая из солей? Приведите соответствующие молекулярные, полные и сокращённые ионные уравнения.
Решение. №722 (с. 120)
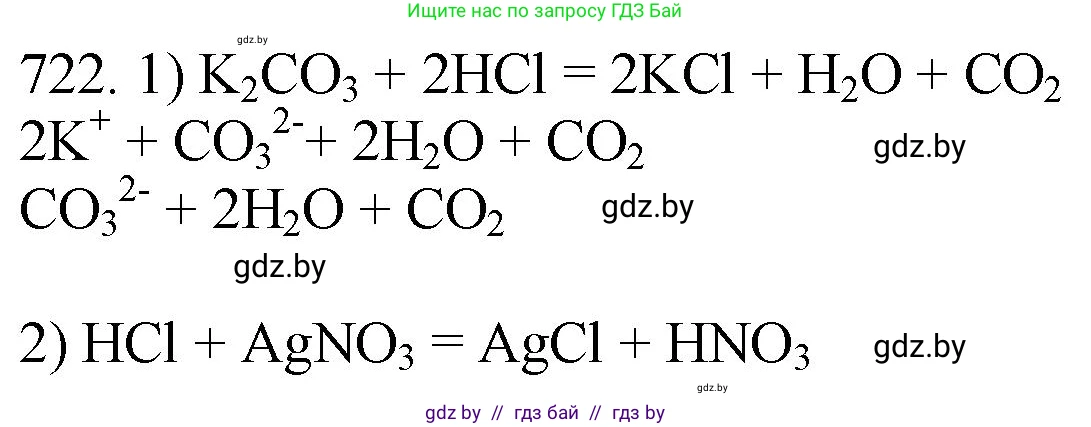
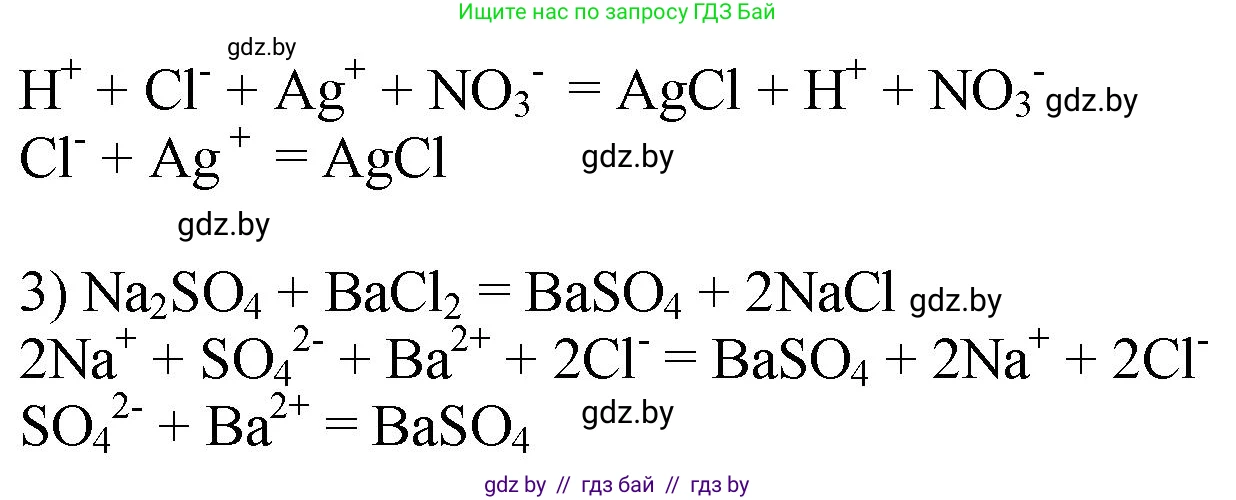
Решение 3. №722 (с. 120)
Решение
Чтобы определить, в какой из пробирок находится каждая из солей, можно использовать раствор сильной кислоты, например, соляной кислоты ($HCl$). Для этого нужно из каждой пробирки отобрать пробы в три чистые пробирки и добавить в каждую по несколько капель раствора $HCl$. По результатам наблюдений можно будет однозначно идентифицировать каждое вещество.
1. Определение карбоната калия ($K_2CO_3$)
В пробирке, содержащей раствор карбоната калия, при добавлении соляной кислоты будет наблюдаться выделение бесцветного газа без запаха — это углекислый газ ($CO_2$). Данная реакция является качественной на карбонат-ион ($CO_3^{2-}$).
Молекулярное уравнение реакции:
$K_2CO_3 + 2HCl \rightarrow 2KCl + H_2O + CO_2 \uparrow$
Полное ионное уравнение:
$2K^+ + CO_3^{2-} + 2H^+ + 2Cl^- \rightarrow 2K^+ + 2Cl^- + H_2O + CO_2 \uparrow$
Сокращенное ионное уравнение:
$CO_3^{2-} + 2H^+ \rightarrow H_2O + CO_2 \uparrow$
Ответ: Пробирка, в которой при добавлении соляной кислоты происходит выделение газа, содержит карбонат калия.
2. Определение нитрата серебра ($AgNO_3$)
В пробирке с раствором нитрата серебра при добавлении соляной кислоты будет образовываться белый творожистый осадок хлорида серебра ($AgCl$). Это качественная реакция на ион серебра ($Ag^+$), который взаимодействует с хлорид-ионами ($Cl^-$) из кислоты.
Молекулярное уравнение реакции:
$AgNO_3 + HCl \rightarrow AgCl \downarrow + HNO_3$
Полное ионное уравнение:
$Ag^+ + NO_3^- + H^+ + Cl^- \rightarrow AgCl \downarrow + H^+ + NO_3^-$
Сокращенное ионное уравнение:
$Ag^+ + Cl^- \rightarrow AgCl \downarrow$
Ответ: Пробирка, в которой при добавлении соляной кислоты выпадает белый осадок, содержит нитрат серебра.
3. Определение сульфата натрия ($Na_2SO_4$)
В пробирке с раствором сульфата натрия при добавлении соляной кислоты никаких видимых изменений не произойдет, так как эти вещества не вступают в реакцию ионного обмена (не образуется осадок, газ или слабый электролит).
$Na_2SO_4 + HCl \rightarrow \text{реакция не идет}$
Ответ: Пробирка, в которой при добавлении соляной кислоты нет видимых признаков реакции, содержит сульфат натрия.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 722 расположенного на странице 120 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №722 (с. 120), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














