Номер 733, страница 122 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 5. Химия растворов. Параграф 27. Химические свойства кислот, оснований, солей в свете теории электролитической диссоциации - номер 733, страница 122.
№733 (с. 122)
Условие. №733 (с. 122)
скриншот условия

733. Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) $Na$ → $NaOH$ → $Na_2CO_3$ → $CO_2$ → $CaCO_3$ → $CO_2$ → $H_2CO_3$;
б) $Cl_2$ → $HCl$ → $ZnCl_2$ → $Zn(OH)_2$ → $ZnO$ → $Zn(NO_3)_2$ → $ZnS$;
в) $CuO$ → $Cu$ → $CuCl_2$ → $Cu$ → $Cu(NO_3)_2$ → $Cu(OH)_2$;
г) $P_2O_5$ → $Na_3PO_4$ → $Na_2SO_4$ → $NaOH$ → $Na_2S$.
Уравнения запишите в молекулярной, полной и сокращённой ионных формах.
Решение. №733 (с. 122)
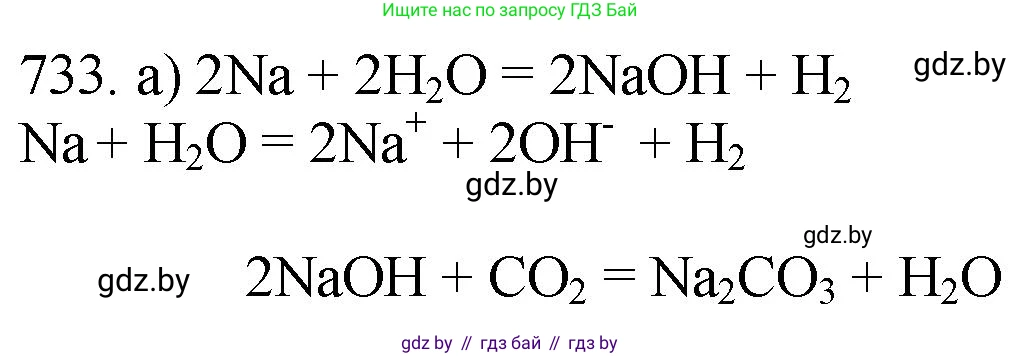

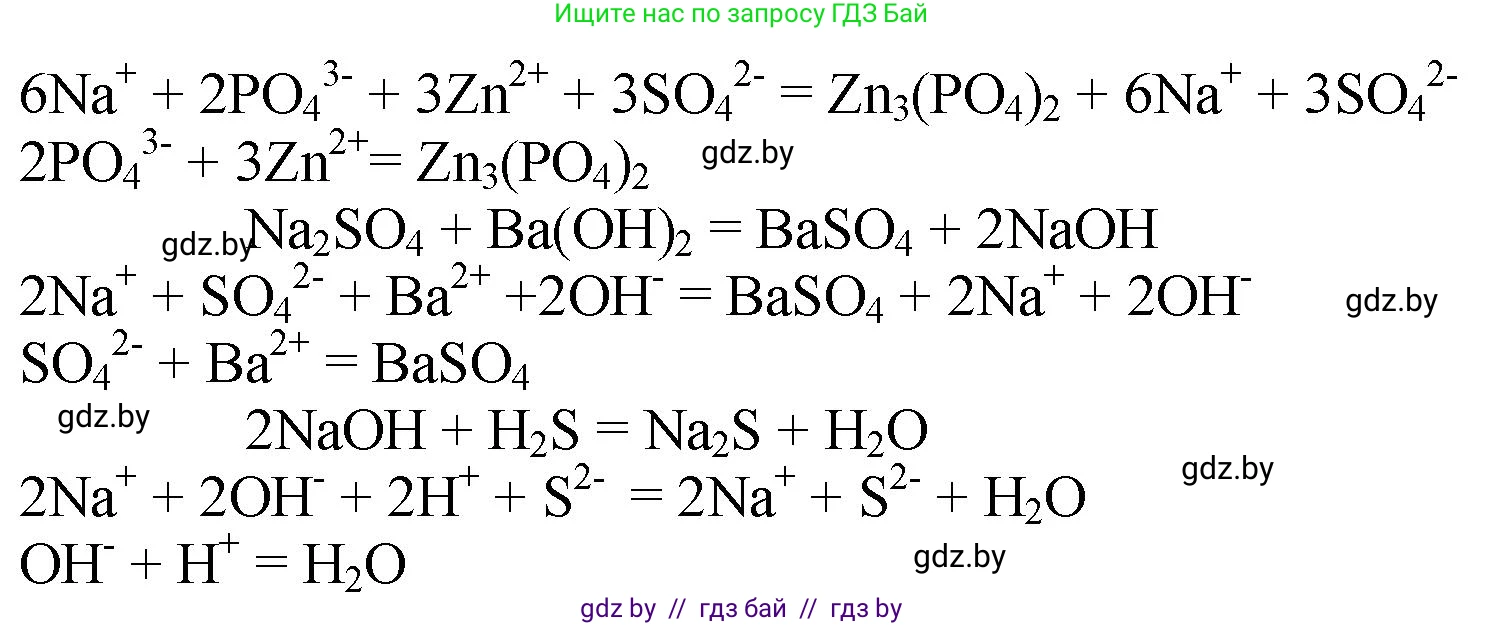
Решение 3. №733 (с. 122)
a) Na → NaOH → Na₂CO₃ → CO₂ → CaCO₃ → CO₂ → H₂CO₃
1. Получение гидроксида натрия из натрия взаимодействием с водой:
- Молекулярное уравнение: $2Na + 2H_2O \rightarrow 2NaOH + H_2 \uparrow$
- Полное ионное уравнение: $2Na + 2H_2O \rightarrow 2Na^+ + 2OH^- + H_2 \uparrow$
- Сокращенное ионное уравнение: Для данной окислительно-восстановительной реакции сокращенное ионное уравнение совпадает с полным.
2. Получение карбоната натрия из гидроксида натрия взаимодействием с оксидом углерода(IV):
- Молекулярное уравнение: $2NaOH + CO_2 \rightarrow Na_2CO_3 + H_2O$
- Полное ионное уравнение: $2Na^+ + 2OH^- + CO_2 \rightarrow 2Na^+ + CO_3^{2-} + H_2O$
- Сокращенное ионное уравнение: $2OH^- + CO_2 \rightarrow CO_3^{2-} + H_2O$
3. Получение оксида углерода(IV) из карбоната натрия действием сильной кислоты (например, соляной):
- Молекулярное уравнение: $Na_2CO_3 + 2HCl \rightarrow 2NaCl + H_2O + CO_2 \uparrow$
- Полное ионное уравнение: $2Na^+ + CO_3^{2-} + 2H^+ + 2Cl^- \rightarrow 2Na^+ + 2Cl^- + H_2O + CO_2 \uparrow$
- Сокращенное ионное уравнение: $CO_3^{2-} + 2H^+ \rightarrow H_2O + CO_2 \uparrow$
4. Получение карбоната кальция из оксида углерода(IV) пропусканием через гидроксид кальция (известковую воду):
- Молекулярное уравнение: $CO_2 + Ca(OH)_2 \rightarrow CaCO_3 \downarrow + H_2O$
- Полное ионное уравнение: $CO_2 + Ca^{2+} + 2OH^- \rightarrow CaCO_3 \downarrow + H_2O$
- Сокращенное ионное уравнение: Совпадает с полным, так как все реагенты участвуют в образовании осадка или слабого электролита.
5. Получение оксида углерода(IV) из карбоната кальция действием сильной кислоты:
- Молекулярное уравнение: $CaCO_3 + 2HCl \rightarrow CaCl_2 + H_2O + CO_2 \uparrow$
- Полное ионное уравнение: $CaCO_3(s) + 2H^+ + 2Cl^- \rightarrow Ca^{2+} + 2Cl^- + H_2O + CO_2 \uparrow$
- Сокращенное ионное уравнение: $CaCO_3(s) + 2H^+ \rightarrow Ca^{2+} + H_2O + CO_2 \uparrow$
6. Получение угольной кислоты из оксида углерода(IV) растворением в воде:
- Молекулярное уравнение: $CO_2 + H_2O \rightleftharpoons H_2CO_3$
- Полное ионное уравнение: Реакция протекает между молекулами, ионные формы не записываются.
- Сокращенное ионное уравнение: Неприменимо.
Ответ:
- $2Na + 2H_2O \rightarrow 2NaOH + H_2 \uparrow$
- $2NaOH + CO_2 \rightarrow Na_2CO_3 + H_2O$
- $Na_2CO_3 + 2HCl \rightarrow 2NaCl + H_2O + CO_2 \uparrow$
- $CO_2 + Ca(OH)_2 \rightarrow CaCO_3 \downarrow + H_2O$
- $CaCO_3 + 2HCl \rightarrow CaCl_2 + H_2O + CO_2 \uparrow$
- $CO_2 + H_2O \rightleftharpoons H_2CO_3$
б) Cl₂ → HCl → ZnCl₂ → Zn(OH)₂ → ZnO → Zn(NO₃)₂ → ZnS
1. Получение хлороводорода из хлора реакцией с водородом:
- Молекулярное уравнение: $Cl_2 + H_2 \xrightarrow{h\nu} 2HCl$
- Ионные уравнения не записываются, так как все вещества – газы, состоящие из молекул.
2. Получение хлорида цинка из соляной кислоты взаимодействием с цинком:
- Молекулярное уравнение: $Zn + 2HCl \rightarrow ZnCl_2 + H_2 \uparrow$
- Полное ионное уравнение: $Zn + 2H^+ + 2Cl^- \rightarrow Zn^{2+} + 2Cl^- + H_2 \uparrow$
- Сокращенное ионное уравнение: $Zn + 2H^+ \rightarrow Zn^{2+} + H_2 \uparrow$
3. Получение гидроксида цинка из хлорида цинка действием щелочи:
- Молекулярное уравнение: $ZnCl_2 + 2NaOH \rightarrow Zn(OH)_2 \downarrow + 2NaCl$
- Полное ионное уравнение: $Zn^{2+} + 2Cl^- + 2Na^+ + 2OH^- \rightarrow Zn(OH)_2 \downarrow + 2Na^+ + 2Cl^-$
- Сокращенное ионное уравнение: $Zn^{2+} + 2OH^- \rightarrow Zn(OH)_2 \downarrow$
4. Получение оксида цинка термическим разложением гидроксида цинка:
- Молекулярное уравнение: $Zn(OH)_2 \xrightarrow{t} ZnO + H_2O$
- Ионные уравнения не записываются, так как реагент и продукты - твердые вещества или слабые электролиты.
5. Получение нитрата цинка из оксида цинка взаимодействием с азотной кислотой:
- Молекулярное уравнение: $ZnO + 2HNO_3 \rightarrow Zn(NO_3)_2 + H_2O$
- Полное ионное уравнение: $ZnO(s) + 2H^+ + 2NO_3^- \rightarrow Zn^{2+} + 2NO_3^- + H_2O$
- Сокращенное ионное уравнение: $ZnO(s) + 2H^+ \rightarrow Zn^{2+} + H_2O$
6. Получение сульфида цинка из нитрата цинка взаимодействием с сульфидом натрия:
- Молекулярное уравнение: $Zn(NO_3)_2 + Na_2S \rightarrow ZnS \downarrow + 2NaNO_3$
- Полное ионное уравнение: $Zn^{2+} + 2NO_3^- + 2Na^+ + S^{2-} \rightarrow ZnS \downarrow + 2Na^+ + 2NO_3^-$
- Сокращенное ионное уравнение: $Zn^{2+} + S^{2-} \rightarrow ZnS \downarrow$
Ответ:
- $Cl_2 + H_2 \rightarrow 2HCl$
- $Zn + 2HCl \rightarrow ZnCl_2 + H_2 \uparrow$
- $ZnCl_2 + 2NaOH \rightarrow Zn(OH)_2 \downarrow + 2NaCl$
- $Zn(OH)_2 \xrightarrow{t} ZnO + H_2O$
- $ZnO + 2HNO_3 \rightarrow Zn(NO_3)_2 + H_2O$
- $Zn(NO_3)_2 + Na_2S \rightarrow ZnS \downarrow + 2NaNO_3$
в) CuO → Cu → CuCl₂ → Cu → Cu(NO₃)₂ → Cu(OH)₂
1. Получение меди из оксида меди(II) восстановлением водородом при нагревании:
- Молекулярное уравнение: $CuO + H_2 \xrightarrow{t} Cu + H_2O$
- Ионные уравнения не записываются для этой гетерогенной реакции.
2. Получение хлорида меди(II) из меди реакцией с хлором при нагревании:
- Молекулярное уравнение: $Cu + Cl_2 \xrightarrow{t} CuCl_2$
- Ионные уравнения не записываются для этой реакции синтеза из простых веществ.
3. Получение меди из хлорида меди(II) вытеснением более активным металлом (например, цинком):
- Молекулярное уравнение: $CuCl_2 + Zn \rightarrow ZnCl_2 + Cu \downarrow$
- Полное ионное уравнение: $Cu^{2+} + 2Cl^- + Zn \rightarrow Zn^{2+} + 2Cl^- + Cu \downarrow$
- Сокращенное ионное уравнение: $Cu^{2+} + Zn \rightarrow Zn^{2+} + Cu \downarrow$
4. Получение нитрата меди(II) из меди взаимодействием с разбавленной азотной кислотой:
- Молекулярное уравнение: $3Cu + 8HNO_3(\text{разб.}) \rightarrow 3Cu(NO_3)_2 + 2NO \uparrow + 4H_2O$
- Полное ионное уравнение: $3Cu + 8H^+ + 8NO_3^- \rightarrow 3Cu^{2+} + 6NO_3^- + 2NO \uparrow + 4H_2O$
- Сокращенное ионное уравнение: $3Cu + 8H^+ + 2NO_3^- \rightarrow 3Cu^{2+} + 2NO \uparrow + 4H_2O$
5. Получение гидроксида меди(II) из нитрата меди(II) действием щелочи:
- Молекулярное уравнение: $Cu(NO_3)_2 + 2NaOH \rightarrow Cu(OH)_2 \downarrow + 2NaNO_3$
- Полное ионное уравнение: $Cu^{2+} + 2NO_3^- + 2Na^+ + 2OH^- \rightarrow Cu(OH)_2 \downarrow + 2Na^+ + 2NO_3^-$
- Сокращенное ионное уравнение: $Cu^{2+} + 2OH^- \rightarrow Cu(OH)_2 \downarrow$
Ответ:
- $CuO + H_2 \xrightarrow{t} Cu + H_2O$
- $Cu + Cl_2 \xrightarrow{t} CuCl_2$
- $CuCl_2 + Zn \rightarrow ZnCl_2 + Cu \downarrow$
- $3Cu + 8HNO_3(\text{разб.}) \rightarrow 3Cu(NO_3)_2 + 2NO \uparrow + 4H_2O$
- $Cu(NO_3)_2 + 2NaOH \rightarrow Cu(OH)_2 \downarrow + 2NaNO_3$
г) P₂O₅ → Na₃PO₄ → Na₂SO₄ → NaOH → Na₂S
1. Получение фосфата натрия из оксида фосфора(V) взаимодействием с избытком гидроксида натрия:
- Молекулярное уравнение: $P_2O_5 + 6NaOH \rightarrow 2Na_3PO_4 + 3H_2O$
- Полное ионное уравнение: $P_2O_5(s) + 6Na^+ + 6OH^- \rightarrow 6Na^+ + 2PO_4^{3-} + 3H_2O$
- Сокращенное ионное уравнение: $P_2O_5(s) + 6OH^- \rightarrow 2PO_4^{3-} + 3H_2O$
2. Получение сульфата натрия из фосфата натрия взаимодействием с серной кислотой:
- Молекулярное уравнение: $2Na_3PO_4 + 3H_2SO_4 \rightarrow 3Na_2SO_4 + 2H_3PO_4$
- Полное ионное уравнение: $6Na^+ + 2PO_4^{3-} + 6H^+ + 3SO_4^{2-} \rightarrow 6Na^+ + 3SO_4^{2-} + 2H_3PO_4$
- Сокращенное ионное уравнение: $2PO_4^{3-} + 6H^+ \rightarrow 2H_3PO_4$
3. Получение гидроксида натрия из сульфата натрия реакцией с гидроксидом бария:
- Молекулярное уравнение: $Na_2SO_4 + Ba(OH)_2 \rightarrow BaSO_4 \downarrow + 2NaOH$
- Полное ионное уравнение: $2Na^+ + SO_4^{2-} + Ba^{2+} + 2OH^- \rightarrow BaSO_4 \downarrow + 2Na^+ + 2OH^-$
- Сокращенное ионное уравнение: $Ba^{2+} + SO_4^{2-} \rightarrow BaSO_4 \downarrow$
4. Получение сульфида натрия из гидроксида натрия взаимодействием с сероводородом:
- Молекулярное уравнение: $2NaOH + H_2S \rightarrow Na_2S + 2H_2O$
- Полное ионное уравнение: $2Na^+ + 2OH^- + H_2S \rightarrow 2Na^+ + S^{2-} + 2H_2O$
- Сокращенное ионное уравнение: $2OH^- + H_2S \rightarrow S^{2-} + 2H_2O$
Ответ:
- $P_2O_5 + 6NaOH \rightarrow 2Na_3PO_4 + 3H_2O$
- $2Na_3PO_4 + 3H_2SO_4 \rightarrow 3Na_2SO_4 + 2H_3PO_4$
- $Na_2SO_4 + Ba(OH)_2 \rightarrow BaSO_4 \downarrow + 2NaOH$
- $2NaOH + H_2S \rightarrow Na_2S + 2H_2O$
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 733 расположенного на странице 122 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №733 (с. 122), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














