вариант 1, страница 6, часть 1 - гдз по химии 8 класс тетрадь для практических работ Борушко

Авторы: Борушко И. И.
Тип: Тетрадь для практических работ
Издательство: Сэр-Вит
Год издания: 2022 - 2025
Часть: 1
Цвет обложки: розовый с пробирками
ISBN: 978-985-597-607-4
Рекомендовано Научно-методическим учреждением «Национальный институт образования» Министерства образования Республики Беларусь
Популярные ГДЗ в 8 классе
Часть 1. Практические работы. Практическая работа 1 - страница 6.
вариант 1 (с. 6)
Условие. вариант 1 (с. 6)
скриншот условия
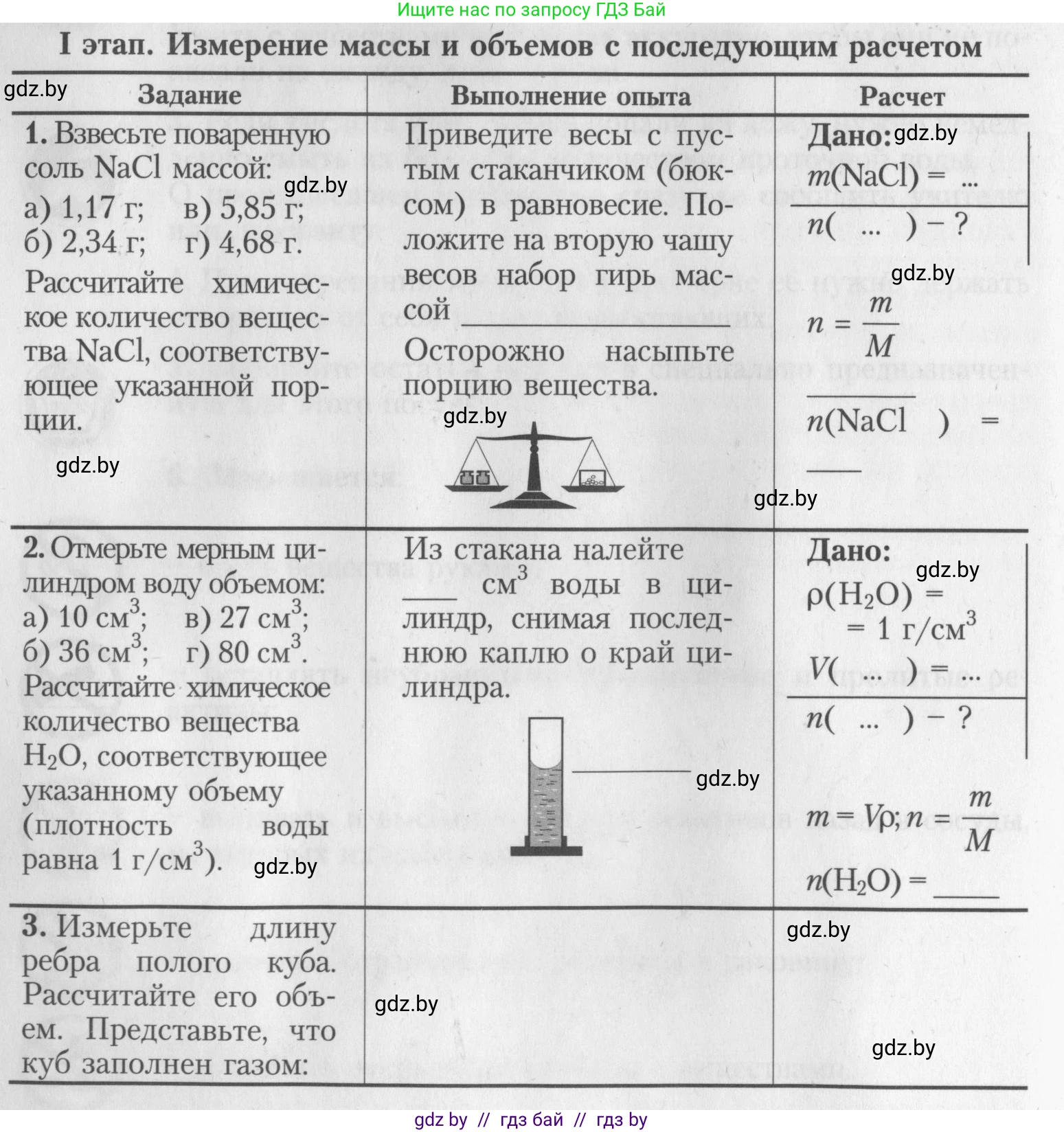


I этап. Измерение массы и объемов с последующим расчетом
| Задание | Выполнение опыта | Расчет |
1. Взвесьте поваренную соль NaCl массой: а) 1,17 г; б) 2,34 г; Рассчитайте химическое количество вещества NaCl, соответствующее указанной порции. | Приведите весы с пустым стаканчиком (бюксом) в равновесие. Положите на вторую чашу весов набор гирь массой _______. Осторожно насыпьте порцию вещества. 
| Дано: $m(NaCl) = ...$ $n(...) = ?$ $n = \frac{m}{M}$ $n(NaCl) = $ |
2. Отмерьте мерным цилиндром воду объемом: а) 10 см$^3$; б) 36 см$^3$; в) 27 см$^3$; г) 80 см$^3$. Рассчитайте химическое количество вещества H$_2$O, соответствующее указанному объему (плотность воды равна 1 г/см$^3$). | Из стакана налейте ______ см$^3$ воды в цилиндр, снимая последнюю каплю с края цилиндра. 
| Дано: $\rho(H_2O) = 1 \, г/см^3$ $V(...) = ...$ $n(...) = ?$ $m = V\rho;$ $n = \frac{m}{M}$ $n(H_2O) =$ |
3. Измерьте длину ребра полого куба. Рассчитайте его объем. Представьте, что куб заполнен газом:
|
Оборудование
Оборудование: весы и разновесы, бюкс (или стаканчик на 25 см$^3$ (мл)), мерный цилиндр, полый куб, линейка, шпатели.
Вещества
Вещества: вода (в колбе), поваренная соль NaCl, питьевая сода NaHCO$_3$, кальцинированная сода Na$_2$CO$_3$, поташ K$_2$CO$_3$.
химическое количество вещества
| Вывод | |
Решение $M_r(NaCl) = $ $M(NaCl) = $ | Твердые вещества взвешивают Химическое количество поваренной соли NaCl в навеске массой _______ равно _______ |
Решение $M_r(H_2O) = $ $M(H_2O) = $ | Химическое количество воды H$_2$O в порции объемом _______ равно _______ |
Решение $V = a^3; n = \frac{V}{V_m}; V_m = 22,4 \, дм^3/моль$ |
| Задание | Выполнение опыта | Расчет |
а) O$_2$; б) N$_2$; в) CO$_2$; г) NO$_2$. Рассчитайте химическое количество газообразного вещества в объеме данного куба. | Измерьте линейкой длину ребра выданного куба. Длина ребра: $a = $ 
Формула газа _______ | Дано: $a = ...$ Найти: $n(...) = ?$ Решение |
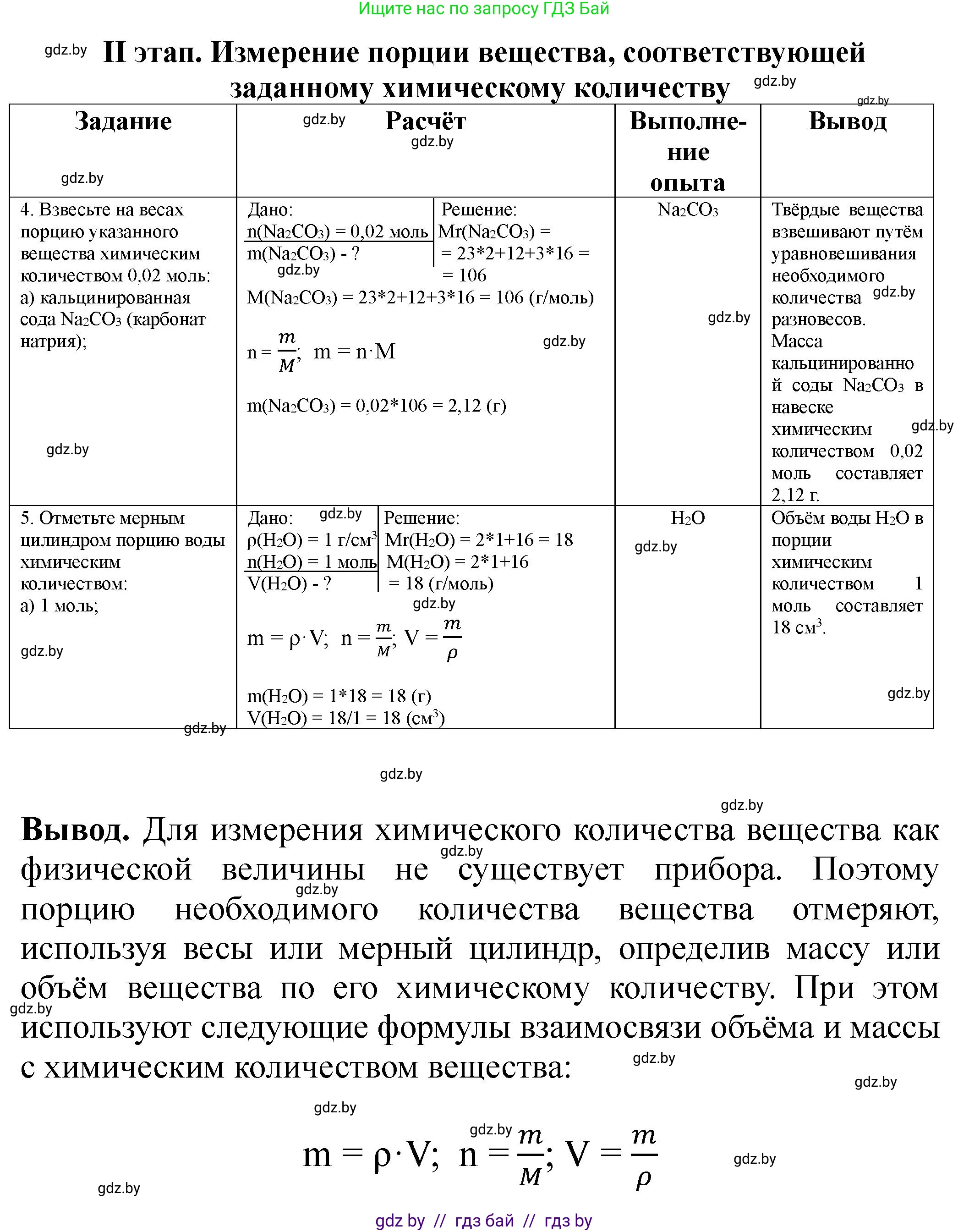
II этап. Измерение порции вещества, соответствующей
| Задание | Расчет |
4. Взвесьте на весах порцию указанного вещества химическим количеством 0,02 моль: а) кальцинированная сода Na$_2$CO$_3$ (карбонат натрия); б) питьевая сода NaHCO$_3$ (гидрокарбонат натрия); в) поваренная соль NaCl (хлорид натрия); г) поташ K$_2$CO$_3$ (карбонат калия). | Дано:
Решение |
5. Отмерьте мерным цилиндром порцию воды химическим количеством: а) 1 моль; б) 2,5 моль; г) 5 моль. | Дано:
Решение |
Вывод. Для измерения химического количества вещества как физической величины не существует прибора. Поэтому порцию необходимого химического количества вещества отмеряют, используя весы или мерный цилиндр, определив массу или объем вещества по его химическому количеству. При этом используют следующие формулы взаимосвязи объема и массы с химическим количеством вещества:
| Вывод | |
заданному химическому количеству
| Выполнение опыта | Вывод | |

| ||
|
Решение. вариант 1 (с. 6)
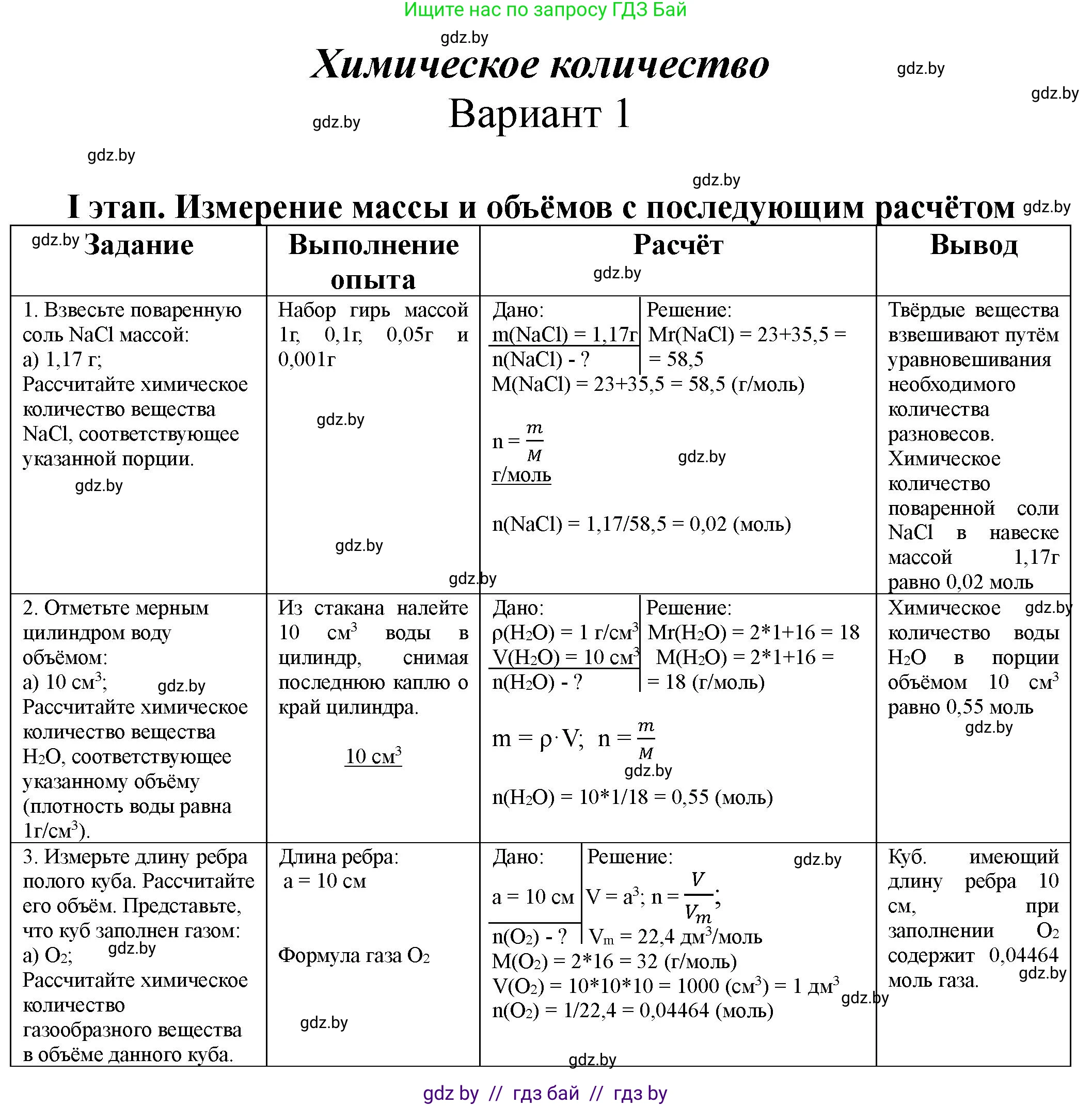
Решение 2. вариант 1 (с. 6)
Взвесьте поваренную соль NaCl массой: a) 1,17 г; б) 2,34 г; в) 5,85 г; г) 4,68 г. Рассчитайте химическое количество вещества NaCl, соответствующее указанной порции.
а) 1,17 г
Дано:
Масса NaCl: $m(\text{NaCl}) = 1.17 \text{ г}$
Перевод в СИ:
$m(\text{NaCl}) = 1.17 \cdot 10^{-3} \text{ кг}$
Найти:
Химическое количество NaCl: $n(\text{NaCl}) - ?$
Решение:
Молярная масса хлорида натрия (NaCl) рассчитывается как сумма атомных масс натрия (Na) и хлора (Cl):
$M(\text{NaCl}) = A_r(\text{Na}) + A_r(\text{Cl}) = 22.98977 \text{ г/моль} + 35.453 \text{ г/моль} = 58.44277 \text{ г/моль}$
Химическое количество вещества рассчитывается по формуле:
$n = \frac{m}{M}$
$n(\text{NaCl}) = \frac{1.17 \text{ г}}{58.44277 \text{ г/моль}} \approx 0.020020 \text{ моль}$
Ответ: $n(\text{NaCl}) \approx 0.020020 \text{ моль}$
б) 2,34 г
Дано:
Масса NaCl: $m(\text{NaCl}) = 2.34 \text{ г}$
Перевод в СИ:
$m(\text{NaCl}) = 2.34 \cdot 10^{-3} \text{ кг}$
Найти:
Химическое количество NaCl: $n(\text{NaCl}) - ?$
Решение:
Молярная масса NaCl: $M(\text{NaCl}) = 58.44277 \text{ г/моль}$
$n(\text{NaCl}) = \frac{2.34 \text{ г}}{58.44277 \text{ г/моль}} \approx 0.040040 \text{ моль}$
Ответ: $n(\text{NaCl}) \approx 0.040040 \text{ моль}$
в) 5,85 г
Дано:
Масса NaCl: $m(\text{NaCl}) = 5.85 \text{ г}$
Перевод в СИ:
$m(\text{NaCl}) = 5.85 \cdot 10^{-3} \text{ кг}$
Найти:
Химическое количество NaCl: $n(\text{NaCl}) - ?$
Решение:
Молярная масса NaCl: $M(\text{NaCl}) = 58.44277 \text{ г/моль}$
$n(\text{NaCl}) = \frac{5.85 \text{ г}}{58.44277 \text{ г/моль}} \approx 0.100098 \text{ моль}$
Ответ: $n(\text{NaCl}) \approx 0.100098 \text{ моль}$
г) 4,68 г
Дано:
Масса NaCl: $m(\text{NaCl}) = 4.68 \text{ г}$
Перевод в СИ:
$m(\text{NaCl}) = 4.68 \cdot 10^{-3} \text{ кг}$
Найти:
Химическое количество NaCl: $n(\text{NaCl}) - ?$
Решение:
Молярная масса NaCl: $M(\text{NaCl}) = 58.44277 \text{ г/моль}$
$n(\text{NaCl}) = \frac{4.68 \text{ г}}{58.44277 \text{ г/моль}} \approx 0.080080 \text{ моль}$
Ответ: $n(\text{NaCl}) \approx 0.080080 \text{ моль}$
2. Отмерьте мерным цилиндром воду объемом: а) 10 см$^3$; б) 27 см$^3$; в) 36 см$^3$; г) 80 см$^3$. Рассчитайте химическое количество вещества H$_2$O, соответствующее указанному объему (плотность воды равна 1 г/см$^3$).
а) 10 см$^3$
Дано:
Объем воды: $V(\text{H}_2\text{O}) = 10 \text{ см}^3$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Перевод в СИ:
$V(\text{H}_2\text{O}) = 10 \cdot 10^{-6} \text{ м}^3$
$\rho(\text{H}_2\text{O}) = 1 \cdot 10^3 \text{ кг/м}^3$
Найти:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды (H$_2$O) рассчитывается как сумма атомных масс двух атомов водорода (H) и одного атома кислорода (O):
$M(\text{H}_2\text{O}) = 2 \cdot A_r(\text{H}) + A_r(\text{O}) = 2 \cdot 1.008 \text{ г/моль} + 15.999 \text{ г/моль} = 18.015 \text{ г/моль}$
Масса воды рассчитывается по формуле: $m = \rho \cdot V$
$m(\text{H}_2\text{O}) = 1 \text{ г/см}^3 \cdot 10 \text{ см}^3 = 10 \text{ г}$
Химическое количество вещества рассчитывается по формуле: $n = \frac{m}{M}$
$n(\text{H}_2\text{O}) = \frac{10 \text{ г}}{18.015 \text{ г/моль}} \approx 0.55509 \text{ моль}$
Ответ: $n(\text{H}_2\text{O}) \approx 0.55509 \text{ моль}$
б) 27 см$^3$
Дано:
Объем воды: $V(\text{H}_2\text{O}) = 27 \text{ см}^3$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Перевод в СИ:
$V(\text{H}_2\text{O}) = 27 \cdot 10^{-6} \text{ м}^3$
$\rho(\text{H}_2\text{O}) = 1 \cdot 10^3 \text{ кг/м}^3$
Найти:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды: $M(\text{H}_2\text{O}) = 18.015 \text{ г/моль}$
$m(\text{H}_2\text{O}) = 1 \text{ г/см}^3 \cdot 27 \text{ см}^3 = 27 \text{ г}$
$n(\text{H}_2\text{O}) = \frac{27 \text{ г}}{18.015 \text{ г/моль}} \approx 1.49875 \text{ моль}$
Ответ: $n(\text{H}_2\text{O}) \approx 1.49875 \text{ моль}$
в) 36 см$^3$
Дано:
Объем воды: $V(\text{H}_2\text{O}) = 36 \text{ см}^3$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Перевод в СИ:
$V(\text{H}_2\text{O}) = 36 \cdot 10^{-6} \text{ м}^3$
$\rho(\text{H}_2\text{O}) = 1 \cdot 10^3 \text{ кг/м}^3$
Найти:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды: $M(\text{H}_2\text{O}) = 18.015 \text{ г/моль}$
$m(\text{H}_2\text{O}) = 1 \text{ г/см}^3 \cdot 36 \text{ см}^3 = 36 \text{ г}$
$n(\text{H}_2\text{O}) = \frac{36 \text{ г}}{18.015 \text{ г/моль}} \approx 1.99833 \text{ моль}$
Ответ: $n(\text{H}_2\text{O}) \approx 1.99833 \text{ моль}$
г) 80 см$^3$
Дано:
Объем воды: $V(\text{H}_2\text{O}) = 80 \text{ см}^3$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Перевод в СИ:
$V(\text{H}_2\text{O}) = 80 \cdot 10^{-6} \text{ м}^3$
$\rho(\text{H}_2\text{O}) = 1 \cdot 10^3 \text{ кг/м}^3$
Найти:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды: $M(\text{H}_2\text{O}) = 18.015 \text{ г/моль}$
$m(\text{H}_2\text{O}) = 1 \text{ г/см}^3 \cdot 80 \text{ см}^3 = 80 \text{ г}$
$n(\text{H}_2\text{O}) = \frac{80 \text{ г}}{18.015 \text{ г/моль}} \approx 4.44074 \text{ моль}$
Ответ: $n(\text{H}_2\text{O}) \approx 4.44074 \text{ моль}$
3. Измерьте длину ребра полого куба. Рассчитайте его объем. Представьте, что куб заполнен газом: а) O$_2$; б) N$_2$; в) CO$_2$; г) NO$_2$. Рассчитайте химическое количество газообразного вещества в объеме данного куба.
Примечание: Для решения этой задачи требуется фактическое измерение длины ребра куба. Так как физическое измерение невозможно, примем условную длину ребра куба, например, $a = 2.0 \text{ см}$. Молярный объем газов при нормальных условиях (н.у., 0°C и 1 атм) составляет $22.4 \text{ дм}^3/\text{моль}$.
Дано:
Длина ребра куба: $a = 2.0 \text{ см}$
Молярный объем газа при н.у.: $V_m = 22.4 \text{ дм}^3/\text{моль}$
Перевод в СИ:
$a = 2.0 \cdot 10^{-2} \text{ м}$
$V_m = 22.4 \cdot 10^{-3} \text{ м}^3/\text{моль}$ (или $22400 \text{ см}^3/\text{моль}$)
Найти:
Объем куба: $V - ?$
Химическое количество газа: $n(газ) - ?$
Решение:
Объем куба рассчитывается по формуле:
$V = a^3$
$V = (2.0 \text{ см})^3 = 8.0 \text{ см}^3$
Химическое количество газообразного вещества рассчитывается по формуле, используя молярный объем газа при н.у.:
$n = \frac{V}{V_m}$
$n = \frac{8.0 \text{ см}^3}{22400 \text{ см}^3/\text{моль}} \approx 0.00035714 \text{ моль}$
Поскольку молярный объем газов при одинаковых условиях одинаков, химическое количество вещества будет одинаковым для всех перечисленных газов.
а) O$_2$
Ответ: $n(\text{O}_2) \approx 0.000357 \text{ моль}$
б) N$_2$
Ответ: $n(\text{N}_2) \approx 0.000357 \text{ моль}$
в) CO$_2$
Ответ: $n(\text{CO}_2) \approx 0.000357 \text{ моль}$
г) NO$_2$
Ответ: $n(\text{NO}_2) \approx 0.000357 \text{ моль}$
4. Взвесьте на весах порцию указанного вещества химическим количеством 0,02 моль:
а) кальцинированная сода Na$_2$CO$_3$ (карбонат натрия)
Дано:
Химическое количество Na$_2$CO$_3$: $n(\text{Na}_2\text{CO}_3) = 0.02 \text{ моль}$
Найти:
Масса Na$_2$CO$_3$: $m(\text{Na}_2\text{CO}_3) - ?$
Решение:
Молярная масса Na$_2$CO$_3$ рассчитывается как:
$M(\text{Na}_2\text{CO}_3) = 2 \cdot A_r(\text{Na}) + A_r(\text{C}) + 3 \cdot A_r(\text{O})$
$M(\text{Na}_2\text{CO}_3) = 2 \cdot 22.98977 \text{ г/моль} + 12.011 \text{ г/моль} + 3 \cdot 15.999 \text{ г/моль} = 105.98754 \text{ г/моль}$
Масса вещества рассчитывается по формуле: $m = n \cdot M$
$m(\text{Na}_2\text{CO}_3) = 0.02 \text{ моль} \cdot 105.98754 \text{ г/моль} \approx 2.11975 \text{ г}$
Ответ: $m(\text{Na}_2\text{CO}_3) \approx 2.12 \text{ г}$
б) питьевая сода NaHCO$_3$ (гидрокарбонат натрия)
Дано:
Химическое количество NaHCO$_3$: $n(\text{NaHCO}_3) = 0.02 \text{ моль}$
Найти:
Масса NaHCO$_3$: $m(\text{NaHCO}_3) - ?$
Решение:
Молярная масса NaHCO$_3$ рассчитывается как:
$M(\text{NaHCO}_3) = A_r(\text{Na}) + A_r(\text{H}) + A_r(\text{C}) + 3 \cdot A_r(\text{O})$
$M(\text{NaHCO}_3) = 22.98977 \text{ г/моль} + 1.008 \text{ г/моль} + 12.011 \text{ г/моль} + 3 \cdot 15.999 \text{ г/моль} = 84.00577 \text{ г/моль}$
$m(\text{NaHCO}_3) = 0.02 \text{ моль} \cdot 84.00577 \text{ г/моль} \approx 1.68012 \text{ г}$
Ответ: $m(\text{NaHCO}_3) \approx 1.68 \text{ г}$
в) поваренная соль NaCl (хлорид натрия)
Дано:
Химическое количество NaCl: $n(\text{NaCl}) = 0.02 \text{ моль}$
Найти:
Масса NaCl: $m(\text{NaCl}) - ?$
Решение:
Молярная масса NaCl: $M(\text{NaCl}) = 58.44277 \text{ г/моль}$
$m(\text{NaCl}) = 0.02 \text{ моль} \cdot 58.44277 \text{ г/моль} \approx 1.16886 \text{ г}$
Ответ: $m(\text{NaCl}) \approx 1.17 \text{ г}$
г) поташ K$_2$CO$_3$ (карбонат калия)
Дано:
Химическое количество K$_2$CO$_3$: $n(\text{K}_2\text{CO}_3) = 0.02 \text{ моль}$
Найти:
Масса K$_2$CO$_3$: $m(\text{K}_2\text{CO}_3) - ?$
Решение:
Молярная масса K$_2$CO$_3$ рассчитывается как:
$M(\text{K}_2\text{CO}_3) = 2 \cdot A_r(\text{K}) + A_r(\text{C}) + 3 \cdot A_r(\text{O})$
$M(\text{K}_2\text{CO}_3) = 2 \cdot 39.0983 \text{ г/моль} + 12.011 \text{ г/моль} + 3 \cdot 15.999 \text{ г/моль} = 138.2046 \text{ г/моль}$
$m(\text{K}_2\text{CO}_3) = 0.02 \text{ моль} \cdot 138.2046 \text{ г/моль} \approx 2.76409 \text{ г}$
Ответ: $m(\text{K}_2\text{CO}_3) \approx 2.76 \text{ г}$
5. Отмерьте мерным цилиндром порцию воды химическим количеством:
а) 1 моль
Дано:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) = 1 \text{ моль}$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Найти:
Объем H$_2$O: $V(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды: $M(\text{H}_2\text{O}) = 18.015 \text{ г/моль}$
Масса воды рассчитывается по формуле: $m = n \cdot M$
$m(\text{H}_2\text{O}) = 1 \text{ моль} \cdot 18.015 \text{ г/моль} = 18.015 \text{ г}$
Объем воды рассчитывается по формуле: $V = \frac{m}{\rho}$
$V(\text{H}_2\text{O}) = \frac{18.015 \text{ г}}{1 \text{ г/см}^3} = 18.015 \text{ см}^3$
Ответ: $V(\text{H}_2\text{O}) = 18.015 \text{ см}^3$
б) 2,5 моль
Дано:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) = 2.5 \text{ моль}$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Найти:
Объем H$_2$O: $V(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды: $M(\text{H}_2\text{O}) = 18.015 \text{ г/моль}$
$m(\text{H}_2\text{O}) = 2.5 \text{ моль} \cdot 18.015 \text{ г/моль} = 45.0375 \text{ г}$
$V(\text{H}_2\text{O}) = \frac{45.0375 \text{ г}}{1 \text{ г/см}^3} = 45.0375 \text{ см}^3$
Ответ: $V(\text{H}_2\text{O}) = 45.0375 \text{ см}^3$
в) 4 моль
Дано:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) = 4 \text{ моль}$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Найти:
Объем H$_2$O: $V(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды: $M(\text{H}_2\text{O}) = 18.015 \text{ г/моль}$
$m(\text{H}_2\text{O}) = 4 \text{ моль} \cdot 18.015 \text{ г/моль} = 72.06 \text{ г}$
$V(\text{H}_2\text{O}) = \frac{72.06 \text{ г}}{1 \text{ г/см}^3} = 72.06 \text{ см}^3$
Ответ: $V(\text{H}_2\text{O}) = 72.06 \text{ см}^3$
г) 5 моль
Дано:
Химическое количество H$_2$O: $n(\text{H}_2\text{O}) = 5 \text{ моль}$
Плотность воды: $\rho(\text{H}_2\text{O}) = 1 \text{ г/см}^3$
Найти:
Объем H$_2$O: $V(\text{H}_2\text{O}) - ?$
Решение:
Молярная масса воды: $M(\text{H}_2\text{O}) = 18.015 \text{ г/моль}$
$m(\text{H}_2\text{O}) = 5 \text{ моль} \cdot 18.015 \text{ г/моль} = 90.075 \text{ г}$
$V(\text{H}_2\text{O}) = \frac{90.075 \text{ г}}{1 \text{ г/см}^3} = 90.075 \text{ см}^3$
Ответ: $V(\text{H}_2\text{O}) = 90.075 \text{ см}^3$
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения вариант 1 расположенного на странице 6 для 1-й части к тетради для практических работ 2022 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению вариант 1 (с. 6), автора: Борушко (Ирина Ивановна), 1-й части учебного пособия издательства Сэр-Вит.














