Номер 15, страница 10 - гдз по химии 9 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2020 - 2025
Цвет обложки: салатовый, голубой с колбами
ISBN: 978-985-599-248-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 9 классе
Глава I. Повторение основных вопросов курса химии VIII класса. Параграф 1. Основные классы неорганических веществ - номер 15, страница 10.
№15 (с. 10)
Условие. №15 (с. 10)
скриншот условия

15. Рассчитайте массовую долю:
а) кислорода в оксиде натрия;
б) водорода в гидроксиде кальция;
в) кислорода в фосфорной кислоте;
г) серы в сульфате железа(III).
Решение. №15 (с. 10)
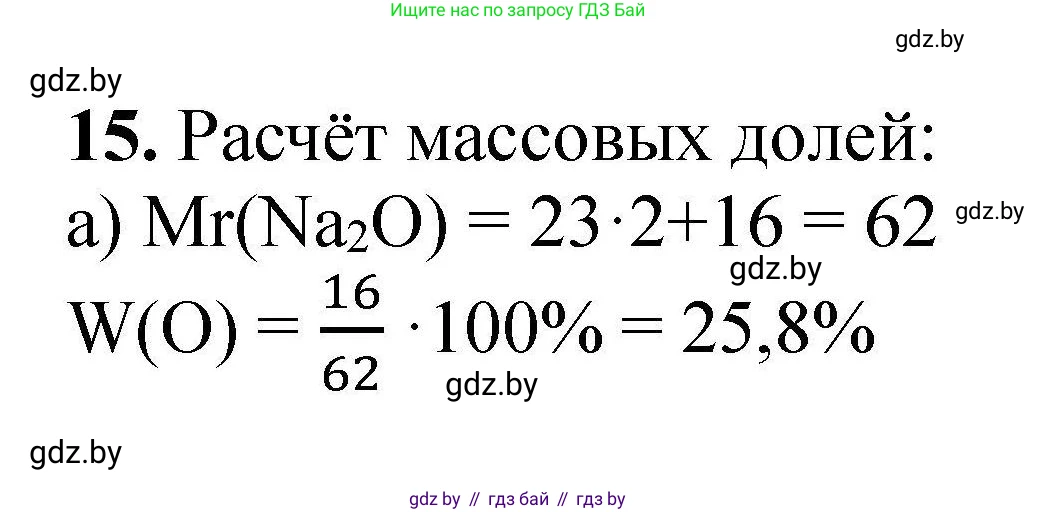

Решение 2. №15 (с. 10)
а) кислорода в оксиде натрия
Дано: Оксид натрия с химической формулой $Na_2O$. Относительные атомные массы: $Ar(Na) = 23$, $Ar(O) = 16$.
Найти: Массовую долю кислорода $\omega(O)$ в $Na_2O$.
Решение:
Массовая доля элемента в соединении рассчитывается по формуле: $ \omega(\text{элемента}) = \frac{n \cdot Ar(\text{элемента})}{Mr(\text{соединения})} $, где $n$ — количество атомов элемента, $Ar$ — относительная атомная масса, $Mr$ — относительная молекулярная масса.
1. Рассчитаем относительную молекулярную массу оксида натрия:
$ Mr(Na_2O) = 2 \cdot Ar(Na) + 1 \cdot Ar(O) = 2 \cdot 23 + 16 = 62 $.
2. Рассчитаем массовую долю кислорода (в $Na_2O$ один атом кислорода):
$ \omega(O) = \frac{1 \cdot Ar(O)}{Mr(Na_2O)} = \frac{1 \cdot 16}{62} \approx 0.258 $.
Для выражения в процентах, умножим на 100%: $0.258 \cdot 100\% = 25.8\%$.
Ответ: массовая доля кислорода в оксиде натрия составляет 25.8%.
б) водорода в гидроксиде кальция
Дано: Гидроксид кальция с химической формулой $Ca(OH)_2$. Относительные атомные массы: $Ar(Ca) = 40$, $Ar(O) = 16$, $Ar(H) = 1$.
Найти: Массовую долю водорода $\omega(H)$ в $Ca(OH)_2$.
Решение:
1. Рассчитаем относительную молекулярную массу гидроксида кальция:
$ Mr(Ca(OH)_2) = 1 \cdot Ar(Ca) + 2 \cdot (Ar(O) + Ar(H)) = 40 + 2 \cdot (16 + 1) = 74 $.
2. Рассчитаем массовую долю водорода (в $Ca(OH)_2$ два атома водорода):
$ \omega(H) = \frac{2 \cdot Ar(H)}{Mr(Ca(OH)_2)} = \frac{2 \cdot 1}{74} \approx 0.027 $.
В процентах: $0.027 \cdot 100\% = 2.7\%$.
Ответ: массовая доля водорода в гидроксиде кальция составляет 2.7%.
в) кислорода в фосфорной кислоте
Дано: Фосфорная кислота с химической формулой $H_3PO_4$. Относительные атомные массы: $Ar(H) = 1$, $Ar(P) = 31$, $Ar(O) = 16$.
Найти: Массовую долю кислорода $\omega(O)$ в $H_3PO_4$.
Решение:
1. Рассчитаем относительную молекулярную массу фосфорной кислоты:
$ Mr(H_3PO_4) = 3 \cdot Ar(H) + 1 \cdot Ar(P) + 4 \cdot Ar(O) = 3 \cdot 1 + 31 + 4 \cdot 16 = 98 $.
2. Рассчитаем массовую долю кислорода (в $H_3PO_4$ четыре атома кислорода):
$ \omega(O) = \frac{4 \cdot Ar(O)}{Mr(H_3PO_4)} = \frac{4 \cdot 16}{98} = \frac{64}{98} \approx 0.653 $.
В процентах: $0.653 \cdot 100\% = 65.3\%$.
Ответ: массовая доля кислорода в фосфорной кислоте составляет 65.3%.
г) серы в сульфате железа(III)
Дано: Сульфат железа(III). Валентность железа (Fe) равна III, сульфат-иона ($SO_4$) — II. Химическая формула: $Fe_2(SO_4)_3$. Относительные атомные массы: $Ar(Fe) = 56$, $Ar(S) = 32$, $Ar(O) = 16$.
Найти: Массовую долю серы $\omega(S)$ в $Fe_2(SO_4)_3$.
Решение:
1. Рассчитаем относительную молекулярную массу сульфата железа(III):
$ Mr(Fe_2(SO_4)_3) = 2 \cdot Ar(Fe) + 3 \cdot (Ar(S) + 4 \cdot Ar(O)) = 2 \cdot 56 + 3 \cdot (32 + 4 \cdot 16) = 112 + 3 \cdot 96 = 400 $.
2. Рассчитаем массовую долю серы (в $Fe_2(SO_4)_3$ три атома серы):
$ \omega(S) = \frac{3 \cdot Ar(S)}{Mr(Fe_2(SO_4)_3)} = \frac{3 \cdot 32}{400} = \frac{96}{400} = 0.24 $.
В процентах: $0.24 \cdot 100\% = 24\%$.
Ответ: массовая доля серы в сульфате железа(III) составляет 24%.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 9 класс, для упражнения номер 15 расположенного на странице 10 к сборнику задач 2020 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №15 (с. 10), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














