Номер 1339, страница 207 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 7. Металлы. Параграф 46. Щелочные металлы - номер 1339, страница 207.
№1339 (с. 207)
Условие. №1339 (с. 207)
скриншот условия
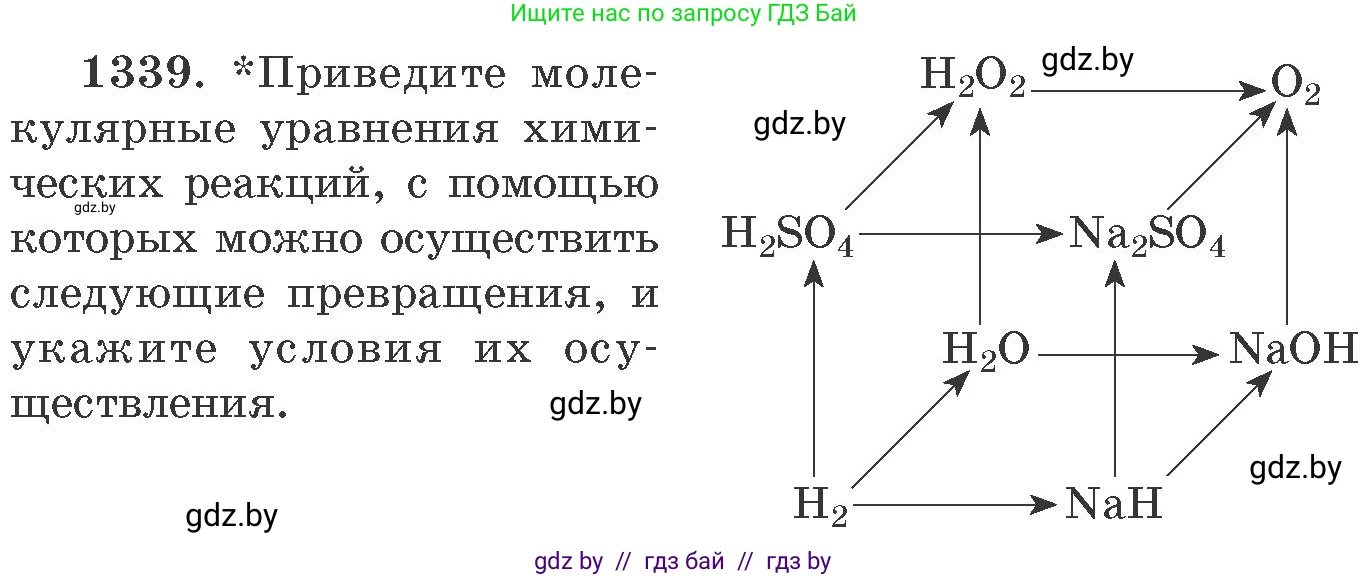
1339. *Приведите молекулярные уравнения химических реакций, с помощью которых можно осуществить следующие превращения, и укажите условия их осуществления.
Превращение 1: $H_2 \rightarrow NaH$
Превращение 2: $H_2 \rightarrow H_2O$
Превращение 3: $H_2 \rightarrow H_2SO_4$
Превращение 4: $NaH \rightarrow NaOH$
Превращение 5: $H_2O \rightarrow NaOH$
Превращение 6: $H_2O \rightarrow H_2O_2$
Превращение 7: $H_2O \rightarrow Na_2SO_4$
Превращение 8: $NaOH \rightarrow O_2$
Превращение 9: $H_2SO_4 \rightarrow Na_2SO_4$
Превращение 10: $H_2SO_4 \rightarrow H_2O_2$
Превращение 11: $Na_2SO_4 \rightarrow O_2$
Превращение 12: $H_2O_2 \rightarrow O_2$
Решение. №1339 (с. 207)

Решение 3. №1339 (с. 207)
Для осуществления представленных на схеме превращений можно провести следующие химические реакции:
H₂ → H₂O: Данное превращение представляет собой реакцию горения (окисления) водорода в кислороде. Реакция является экзотермической и для её начала требуется инициирование: нагревание до температуры выше 550°C, искра, или использование катализатора (например, платины), при котором реакция протекает при комнатной температуре. Ответ: $2H_2 + O_2 \xrightarrow{t^{\circ} \text{ или } Pt} 2H_2O$.
H₂ → NaH: Гидрид натрия получают прямым взаимодействием металлического натрия с водородом при повышенной температуре. Ответ: $2Na + H_2 \xrightarrow{250-400^{\circ}C} 2NaH$.
H₂ → H₂SO₄: Прямое получение серной кислоты из водорода в одну стадию затруднительно. В промышленности используют многостадийный процесс, например, из сероводорода (который можно получить из водорода и серы). Однако, формально, можно записать реакцию гидрогенизации пероксодисерной кислоты (кислоты Маршалла), которая является окислителем. Ответ: $H_2 + H_2S_2O_8 \xrightarrow{Pt} 2H_2SO_4$.
H₂O → NaOH: Гидроксид натрия образуется при бурной реакции металлического натрия с водой. Также его можно получить электролизом водного раствора хлорида натрия. Наиболее прямое превращение из воды — реакция с активным металлом. Ответ: $2Na + 2H_2O \rightarrow 2NaOH + H_2 \uparrow$.
H₂O → H₂O₂: Пероксид водорода можно получить, действуя на пероксиды металлов, например, натрия или бария, водой (часто в присутствии кислоты для нейтрализации щелочи). При реакции пероксида натрия с холодной водой образуется пероксид водорода и гидроксид натрия. Ответ: $Na_2O_2 + 2H_2O (\text{холодн.}) \rightarrow 2NaOH + H_2O_2$.
H₂O → H₂SO₄: Это заключительная стадия промышленного контактного способа получения серной кислоты. Оксид серы(VI) энергично реагирует с водой, образуя серную кислоту. Ответ: $SO_3 + H_2O \rightarrow H_2SO_4$.
NaH → NaOH: Гидрид натрия является солью, образованной сильным основанием и очень слабой кислотой (H₂), поэтому он полностью и бурно гидролизуется водой с образованием гидроксида натрия и выделением водорода. Ответ: $NaH + H_2O \rightarrow NaOH + H_2 \uparrow$.
H₂SO₄ → Na₂SO₄: Сульфат натрия является солью, которую можно получить в результате реакции нейтрализации серной кислоты основанием (гидроксидом натрия), оксидом натрия или солью натрия (например, карбонатом). Наиболее типичная реакция — с гидроксидом натрия. Ответ: $H_2SO_4 + 2NaOH \rightarrow Na_2SO_4 + 2H_2O$.
H₂SO₄ → H₂O₂: Лабораторный способ получения пероксида водорода заключается во взаимодействии пероксида бария с охлажденной разбавленной серной кислотой. В результате реакции образуется нерастворимый сульфат бария, который отделяется фильтрованием. Ответ: $BaO_2 + H_2SO_4 \rightarrow BaSO_4 \downarrow + H_2O_2$.
NaOH → Na₂SO₄: Данное превращение является реакцией нейтрализации, где гидроксид натрия реагирует с серной кислотой с образованием соли (сульфата натрия) и воды. Ответ: $2NaOH + H_2SO_4 \rightarrow Na_2SO_4 + 2H_2O$.
H₂O₂ → O₂: Пероксид водорода — неустойчивое соединение, которое разлагается на воду и кислород. Процесс значительно ускоряется при нагревании, на свету или в присутствии катализаторов (например, оксида марганца(IV)). Ответ: $2H_2O_2 \xrightarrow{MnO_2} 2H_2O + O_2 \uparrow$.
Na₂SO₄ → O₂: Сульфат натрия — очень устойчивая соль. Кислород из него напрямую получить сложно. Однако, кислород можно получить электролизом водного раствора сульфата натрия. В этом процессе электролизу подвергается вода, а сульфат натрия служит электролитом, обеспечивающим проводимость раствора. На аноде выделяется кислород. Ответ: $2H_2O \xrightarrow{\text{электролиз, р-р } Na_2SO_4} 2H_2 \uparrow + O_2 \uparrow$.
NaOH → O₂: Аналогично случаю с сульфатом натрия, кислород можно получить при электролизе водного раствора гидроксида натрия. Вода разлагается на водород (на катоде) и кислород (на аноде), а гидроксид натрия является электролитом. Ответ: $2H_2O \xrightarrow{\text{электролиз, р-р } NaOH} 2H_2 \uparrow + O_2 \uparrow$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 1339 расположенного на странице 207 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №1339 (с. 207), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














