Номер 9, страница 41 - гдз по химии 11 класс учебник Мычко, Прохоревич

Авторы: Мычко Д. И., Прохоревич К. Н., Борушко И. И.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2021 - 2025
Цвет обложки: зелёный с колбами
ISBN: 978-985-599-297-5
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава II. Строение атома и периодический закон. Параграф 7. Строение атома - номер 9, страница 41.
№9 (с. 41)
Условия. №9 (с. 41)
скриншот условия

9. Рассчитайте относительную атомную массу природной меди, если известно, что она состоит из двух изотопов $^{63}\text{Cu}$ (69 %) и $^{65}\text{Cu}$ (31 %), причём $\text{A}_{\text{r}}({}^{63}\text{Cu}) = 62,93$, $\text{A}_{\text{r}}({}^{65}\text{Cu}) = 64,93$. Ответ проверьте по периодической системе Менделеева.
Решение. №9 (с. 41)
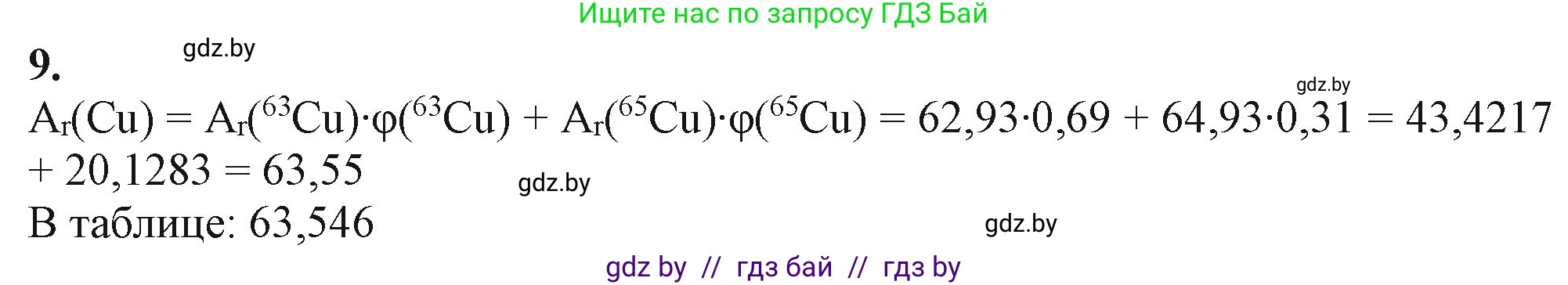
Решение 2. №9 (с. 41)
Дано:
Массовая доля изотопа $^{63}\text{Cu}$, $w(^{63}\text{Cu}) = 69\%$
Массовая доля изотопа $^{65}\text{Cu}$, $w(^{65}\text{Cu}) = 31\%$
Относительная атомная масса изотопа $^{63}\text{Cu}$, $A_r(^{63}\text{Cu}) = 62,93$
Относительная атомная масса изотопа $^{65}\text{Cu}$, $A_r(^{65}\text{Cu}) = 64,93$
Найти:
Относительную атомную массу природной меди $A_r(\text{Cu})$ - ?
Решение:
Относительная атомная масса химического элемента, который в природе существует в виде смеси изотопов, вычисляется как средневзвешенное значение атомных масс этих изотопов с учетом их распространенности (массовой доли).
Общая формула для расчёта:
$A_r(Э) = \sum(w_i \cdot A_{r,i})$
где $w_i$ — массовая доля (распространённость) i-го изотопа в долях от единицы, а $A_{r,i}$ — относительная атомная масса этого изотопа.
Для меди, состоящей из двух изотопов, формула будет выглядеть так:
$A_r(\text{Cu}) = w(^{63}\text{Cu}) \cdot A_r(^{63}\text{Cu}) + w(^{65}\text{Cu}) \cdot A_r(^{65}\text{Cu})$
Перед расчётом переведём процентное содержание изотопов в доли от единицы:
$w(^{63}\text{Cu}) = 69\% = 0,69$
$w(^{65}\text{Cu}) = 31\% = 0,31$
Теперь подставим все известные значения в формулу:
$A_r(\text{Cu}) = 0,69 \cdot 62,93 + 0,31 \cdot 64,93$
Выполним вычисления:
$A_r(\text{Cu}) = 43,4217 + 20,1283$
$A_r(\text{Cu}) = 63,55$
Проверим полученный результат по периодической системе Д.И. Менделеева. Стандартная относительная атомная масса меди (Cu) составляет 63,546. Наш результат, округленный до сотых (63,55), практически полностью совпадает с табличным значением, что подтверждает правильность расчетов.
Ответ: относительная атомная масса природной меди равна $63,55$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 9 расположенного на странице 41 к учебнику 2021 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №9 (с. 41), авторов: Мычко (Дмитрий Иванович), Прохоревич (Константин Николаевич), Борушко (Ирина Ивановна), учебного пособия издательства Адукацыя i выхаванне.













