Номер 7, страница 268 - гдз по химии 11 класс учебник Мычко, Прохоревич

Авторы: Мычко Д. И., Прохоревич К. Н., Борушко И. И.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2021 - 2025
Цвет обложки: зелёный с колбами
ISBN: 978-985-599-297-5
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава VII. Металлы. Параграф 48. Алюминий и его соединения - номер 7, страница 268.
№7 (с. 268)
Условия. №7 (с. 268)
скриншот условия

7. К раствору нитрата алюминия добавили небольшое количество раствора гидроксида калия. Полученный осадок разделили на две части и растворили в серной кислоте и щёлочи (КОН) соответственно. Составьте уравнения протекавших реакций в молекулярной и ионной формах.
Решение. №7 (с. 268)
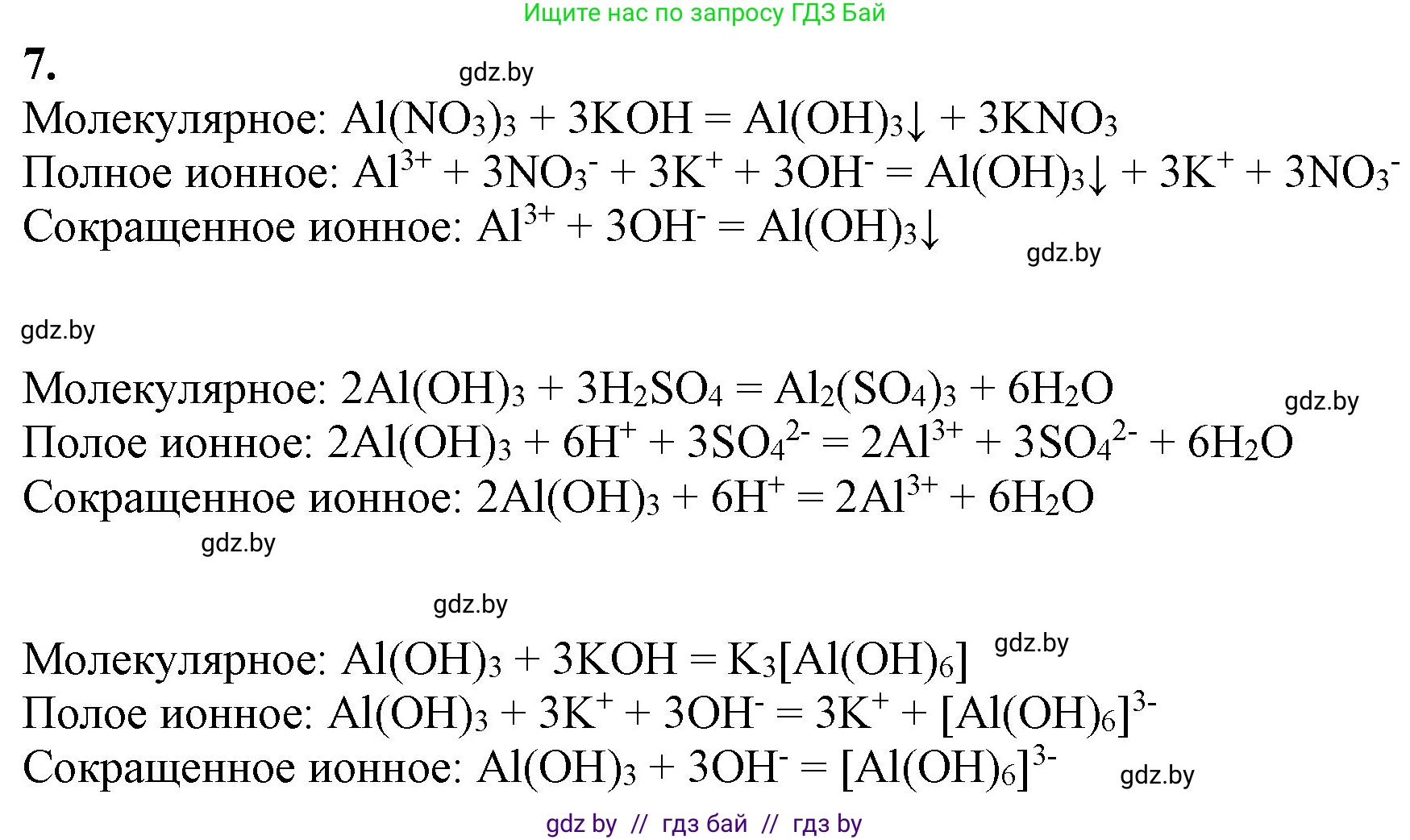
Решение 2. №7 (с. 268)
В задаче описана последовательность химических превращений, в ходе которых проявляются амфотерные свойства гидроксида алюминия. Составим уравнения для каждой стадии в молекулярной и ионной формах.
1. Получение осадка гидроксида алюминия
К раствору нитрата алюминия $Al(NO_3)_3$ добавляют раствор гидроксида калия $KOH$. Так как щёлочь добавляют в небольшом количестве, происходит реакция ионного обмена с образованием нерастворимого осадка гидроксида алюминия $Al(OH)_3$.
Молекулярное уравнение:
$Al(NO_3)_3 + 3KOH \rightarrow Al(OH)_3 \downarrow + 3KNO_3$
Полное ионное уравнение (с учётом того, что $Al(NO_3)_3, KOH, KNO_3$ - сильные электролиты, а $Al(OH)_3$ - нерастворимое основание):
$Al^{3+} + 3NO_3^- + 3K^+ + 3OH^- \rightarrow Al(OH)_3 \downarrow + 3K^+ + 3NO_3^-$
Сокращенное ионное уравнение (после исключения ионов-наблюдателей $K^+$ и $NO_3^-$):
$Al^{3+} + 3OH^- \rightarrow Al(OH)_3 \downarrow$
Ответ: Молекулярное уравнение: $Al(NO_3)_3 + 3KOH \rightarrow Al(OH)_3 \downarrow + 3KNO_3$. Сокращенное ионное уравнение: $Al^{3+} + 3OH^- \rightarrow Al(OH)_3 \downarrow$.
2. Растворение части осадка в серной кислоте
Гидроксид алюминия $Al(OH)_3$ является амфотерным соединением, поэтому он реагирует с кислотами, проявляя свои основные свойства. При взаимодействии с серной кислотой $H_2SO_4$ образуется соль (сульфат алюминия) и вода.
Молекулярное уравнение:
$2Al(OH)_3 + 3H_2SO_4 \rightarrow Al_2(SO_4)_3 + 6H_2O$
Полное ионное уравнение (с учётом того, что $H_2SO_4$ и $Al_2(SO_4)_3$ - сильные электролиты):
$2Al(OH)_3 \downarrow + 6H^+ + 3SO_4^{2-} \rightarrow 2Al^{3+} + 3SO_4^{2-} + 6H_2O$
Сокращенное ионное уравнение (после исключения иона-наблюдателя $SO_4^{2-}$ и сокращения коэффициентов):
$Al(OH)_3 \downarrow + 3H^+ \rightarrow Al^{3+} + 3H_2O$
Ответ: Молекулярное уравнение: $2Al(OH)_3 + 3H_2SO_4 \rightarrow Al_2(SO_4)_3 + 6H_2O$. Сокращенное ионное уравнение: $Al(OH)_3 \downarrow + 3H^+ \rightarrow Al^{3+} + 3H_2O$.
3. Растворение второй части осадка в щёлочи (KOH)
При взаимодействии со щёлочью амфотерный гидроксид алюминия проявляет кислотные свойства. Осадок растворяется с образованием растворимой комплексной соли — тетрагидроксоалюмината калия.
Молекулярное уравнение:
$Al(OH)_3 + KOH \rightarrow K[Al(OH)_4]$
Полное ионное уравнение (с учётом того, что $KOH$ и $K[Al(OH)_4]$ - сильные электролиты):
$Al(OH)_3 \downarrow + K^+ + OH^- \rightarrow K^+ + [Al(OH)_4]^-$
Сокращенное ионное уравнение (после исключения иона-наблюдателя $K^+$):
$Al(OH)_3 \downarrow + OH^- \rightarrow [Al(OH)_4]^-$
Ответ: Молекулярное уравнение: $Al(OH)_3 + KOH \rightarrow K[Al(OH)_4]$. Сокращенное ионное уравнение: $Al(OH)_3 \downarrow + OH^- \rightarrow [Al(OH)_4]^-$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 7 расположенного на странице 268 к учебнику 2021 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №7 (с. 268), авторов: Мычко (Дмитрий Иванович), Прохоревич (Константин Николаевич), Борушко (Ирина Ивановна), учебного пособия издательства Адукацыя i выхаванне.













