Номер 434, страница 85 - гдз по химии 9 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2020 - 2025
Цвет обложки: салатовый, голубой с колбами
ISBN: 978-985-599-248-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 9 классе
Глава 3. Неметаллы. Параграф 26. Нитраты. Применение азотной кислоты и нитратов - номер 434, страница 85.
№434 (с. 85)
Условие. №434 (с. 85)
скриншот условия

434. Ионы каким суммарным химическим количеством содержатся в водном растворе нитрата алюминия массой $270 \text{ г}$ с массовой долей соли, равной $8,50 \%$?
Решение. №434 (с. 85)

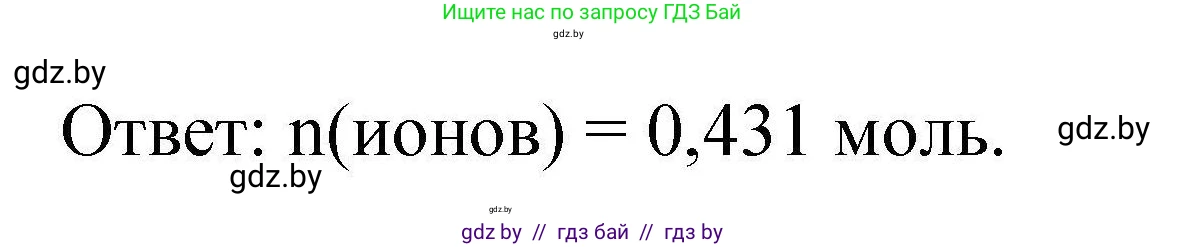
Решение 2. №434 (с. 85)
Дано:
Масса раствора нитрата алюминия, $m_{р-ра} = 270 \text{ г}$
Массовая доля нитрата алюминия, $\omega(Al(NO_3)_3) = 8,50 \% = 0,0850$
Масса раствора в СИ: $m_{р-ра} = 0,270 \text{ кг}$
Найти:
Суммарное химическое количество ионов, $n_{ионов} - ?$
Решение:
1. Найдем массу нитрата алюминия ($Al(NO_3)_3$) в растворе. Масса растворенного вещества вычисляется как произведение массы раствора на массовую долю этого вещества:
$m(Al(NO_3)_3) = m_{р-ра} \times \omega(Al(NO_3)_3)$
$m(Al(NO_3)_3) = 270 \text{ г} \times 0,0850 = 22,95 \text{ г}$
2. Рассчитаем молярную массу нитрата алюминия ($M(Al(NO_3)_3)$). Она равна сумме атомных масс составляющих его элементов с учетом их количества в формульной единице.
$M(Al(NO_3)_3) = M(Al) + 3 \times (M(N) + 3 \times M(O))$
Используя округленные значения атомных масс из периодической таблицы:
$M(Al) \approx 27 \text{ г/моль}$
$M(N) \approx 14 \text{ г/моль}$
$M(O) \approx 16 \text{ г/моль}$
$M(Al(NO_3)_3) = 27 + 3 \times (14 + 3 \times 16) = 27 + 3 \times (14 + 48) = 27 + 3 \times 62 = 27 + 186 = 213 \text{ г/моль}$
3. Найдем химическое количество (число молей) нитрата алюминия, содержащегося в растворе, по формуле $n = m/M$:
$n(Al(NO_3)_3) = \frac{m(Al(NO_3)_3)}{M(Al(NO_3)_3)} = \frac{22,95 \text{ г}}{213 \text{ г/моль}} \approx 0,1077 \text{ моль}$
4. Нитрат алюминия является сильным электролитом и в водном растворе полностью диссоциирует на ионы. Запишем уравнение диссоциации:
$Al(NO_3)_3 \rightarrow Al^{3+} + 3NO_3^-$
Из уравнения следует, что из 1 моль нитрата алюминия образуется 1 моль катионов алюминия ($Al^{3+}$) и 3 моль нитрат-анионов ($NO_3^-$).
Таким образом, общее количество молей ионов, образующихся из 1 моль соли, составляет:
$1 \text{ моль} + 3 \text{ моль} = 4 \text{ моль}$
5. Рассчитаем суммарное химическое количество всех ионов в данном растворе, умножив химическое количество соли на 4:
$n_{ионов} = n(Al(NO_3)_3) \times 4$
$n_{ионов} = 0,1077 \text{ моль} \times 4 \approx 0,4308 \text{ моль}$
Учитывая, что исходные данные (масса раствора 270 г и массовая доля 8,50 %) представлены с тремя значащими цифрами, округлим полученный результат до трех значащих цифр.
Ответ: $0,431 \text{ моль}$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 9 класс, для упражнения номер 434 расположенного на странице 85 к сборнику задач 2020 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №434 (с. 85), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














