Номер 537, страница 100 - гдз по химии 9 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2020 - 2025
Цвет обложки: салатовый, голубой с колбами
ISBN: 978-985-599-248-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 9 классе
Глава 3. Неметаллы. Параграф 32. Угольная кислота и её соли - номер 537, страница 100.
№537 (с. 100)
Условие. №537 (с. 100)
скриншот условия

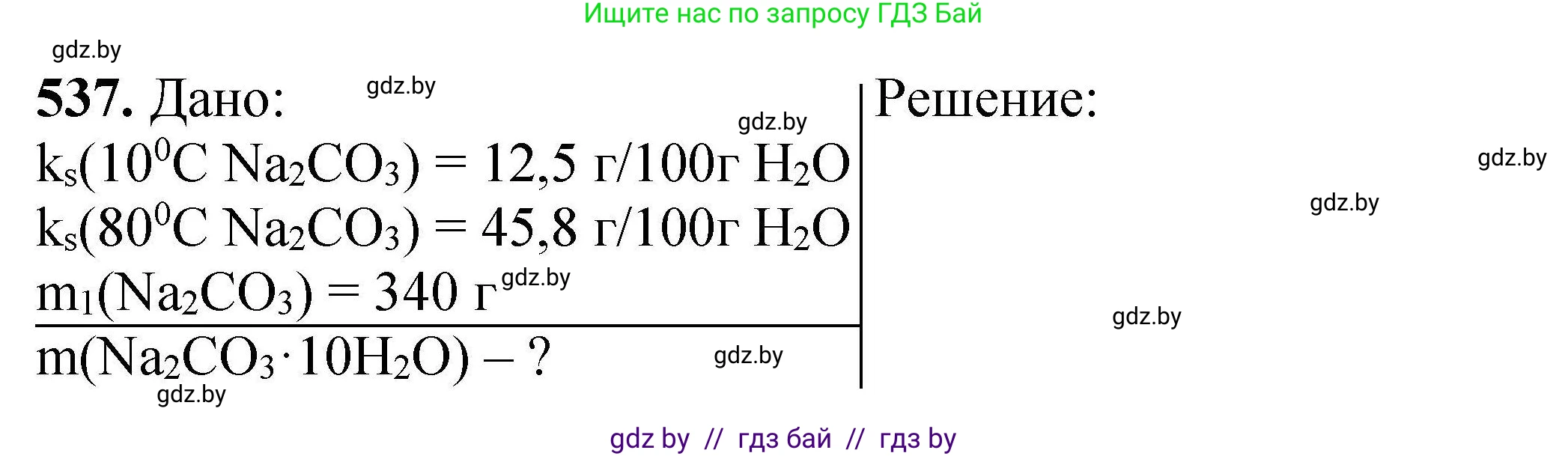
537. Растворимость карбоната натрия при $10°C$ и при $80°C$ соответственно равна $12,5 \, \text{г}$ и $45,8 \, \text{г}$ на $100 \, \text{г}$ воды. Осадок какой массы выпадает при охлаждении до $10°C$ насыщенного при $80°C$ раствора карбоната натрия массой $340 \, \text{г}$?
Решение. №537 (с. 100)

Решение 2. №537 (с. 100)
Дано:
Растворимость карбоната натрия ($S_{10}$) при $t_1 = 10 ^\circ\text{С}$ равна 12,5 г на 100 г воды.
Растворимость карбоната натрия ($S_{80}$) при $t_2 = 80 ^\circ\text{С}$ равна 45,8 г на 100 г воды.
Масса насыщенного раствора при $t_2 = 80 ^\circ\text{С}$ ($m_{\text{р-ра}}(80 ^\circ\text{С})$) равна 340 г.
Найти:
Массу выпавшего осадка ($m_{\text{осадка}}$) — ?
Решение:
1. Сначала определим массу карбоната натрия ($Na_2CO_3$) и воды ($H_2O$) в исходном 340 г насыщенном растворе при $80 ^\circ\text{С}$.
Согласно условию, растворимость при $80 ^\circ\text{С}$ составляет 45,8 г соли на 100 г воды. Это означает, что масса такого насыщенного раствора будет:
$m_{\text{эталонного р-ра}} = m(H_2O) + m(Na_2CO_3) = 100 \text{ г} + 45,8 \text{ г} = 145,8 \text{ г}$
В 145,8 г насыщенного раствора при $80 ^\circ\text{С}$ содержится 45,8 г карбоната натрия.
Вычислим массу карбоната натрия в 340 г такого же раствора, используя пропорцию:
$m(Na_2CO_3 \text{ при } 80 ^\circ\text{С}) = \frac{340 \text{ г} \times 45,8 \text{ г}}{145,8 \text{ г}} \approx 106,804 \text{ г}$
Теперь найдем массу воды в исходном растворе. Она не изменится при охлаждении.
$m(H_2O) = m_{\text{р-ра}}(80 ^\circ\text{С}) - m(Na_2CO_3 \text{ при } 80 ^\circ\text{С}) = 340 \text{ г} - 106,804 \text{ г} \approx 233,196 \text{ г}$
2. Далее рассчитаем, какая масса карбоната натрия может остаться растворенной в 233,196 г воды при охлаждении раствора до $10 ^\circ\text{С}$.
Растворимость при $10 ^\circ\text{С}$ составляет 12,5 г на 100 г воды. Снова воспользуемся пропорцией:
В 100 г воды растворяется 12,5 г $Na_2CO_3$.
В 233,196 г воды растворится $x$ г $Na_2CO_3$.
$m(Na_2CO_3 \text{ при } 10 ^\circ\text{С}) = \frac{233,196 \text{ г} \times 12,5 \text{ г}}{100 \text{ г}} \approx 29,150 \text{ г}$
3. Масса выпавшего осадка — это разница между массой соли в горячем растворе и массой соли, которая может остаться в растворе после его охлаждения.
$m_{\text{осадка}} = m(Na_2CO_3 \text{ при } 80 ^\circ\text{С}) - m(Na_2CO_3 \text{ при } 10 ^\circ\text{С})$
$m_{\text{осадка}} = 106,804 \text{ г} - 29,150 \text{ г} \approx 77,654 \text{ г}$
Округляя результат до десятых, получаем 77,7 г.
Ответ: масса выпавшего осадка составляет 77,7 г.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 9 класс, для упражнения номер 537 расположенного на странице 100 к сборнику задач 2020 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №537 (с. 100), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














