Номер 309, страница 50 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 2. Строение атома и периодический закон. Параграф 12. Значение периодического закона и периодической системы Д. И. Менделеева для развития науки - номер 309, страница 50.
№309 (с. 50)
Условие. №309 (с. 50)
скриншот условия

309. Какое химическое количество гидроксида щелочного металла потребуется для полной нейтрализации раствора массой 708 г с массовой долей фосфорной кислоты 19,6 % ?
Решение. №309 (с. 50)
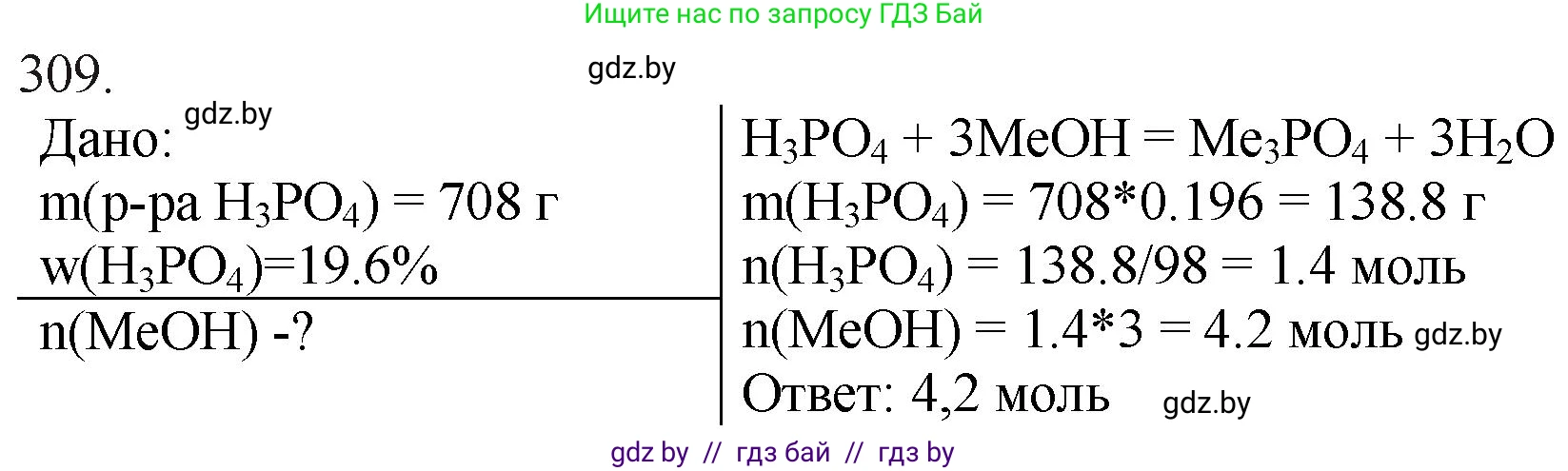
Решение 3. №309 (с. 50)
Дано:
$m_{р-ра(H_3PO_4)} = 708 \text{ г}$
$\omega(H_3PO_4) = 19,6 \% = 0.196$
В системе СИ:
$m_{р-ра(H_3PO_4)} = 0.708 \text{ кг}$
Найти:
$n(MOH)$
Решение:
Реакция нейтрализации фосфорной кислоты гидроксидом щелочного металла (общая формула $MOH$, где $M$ - щелочной металл) до средней соли (полная нейтрализация) описывается следующим уравнением:
$H_3PO_4 + 3MOH \rightarrow M_3PO_4 + 3H_2O$
Сначала найдем массу чистой фосфорной кислоты ($H_3PO_4$) в растворе:
$m(H_3PO_4) = m_{р-ра(H_3PO_4)} \cdot \omega(H_3PO_4)$
$m(H_3PO_4) = 708 \text{ г} \cdot 0.196 = 138.768 \text{ г}$
Далее рассчитаем молярную массу фосфорной кислоты. Используем относительные атомные массы: $A_r(H) = 1$, $A_r(P) = 31$, $A_r(O) = 16$.
$M(H_3PO_4) = 3 \cdot 1 + 31 + 4 \cdot 16 = 98 \text{ г/моль}$
Теперь определим химическое количество фосфорной кислоты, вступившей в реакцию:
$n(H_3PO_4) = \frac{m(H_3PO_4)}{M(H_3PO_4)} = \frac{138.768 \text{ г}}{98 \text{ г/моль}} = 1.416 \text{ моль}$
Согласно уравнению реакции, химические количества фосфорной кислоты и гидроксида щелочного металла соотносятся как 1:3.
$\frac{n(H_3PO_4)}{1} = \frac{n(MOH)}{3}$
Отсюда находим химическое количество гидроксида щелочного металла:
$n(MOH) = 3 \cdot n(H_3PO_4) = 3 \cdot 1.416 \text{ моль} = 4.248 \text{ моль}$
Ответ: для полной нейтрализации потребуется 4.248 моль гидроксида щелочного металла.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 309 расположенного на странице 50 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №309 (с. 50), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














