Номер 354, страница 56 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 3. Химическая связь и строение вещества. Параграф 13. Природа и типы химической связи - номер 354, страница 56.
№354 (с. 56)
Условие. №354 (с. 56)
скриншот условия

354. Какое суммарное число ионов содержится в образце карбоната калия массой 24 г?
Решение. №354 (с. 56)
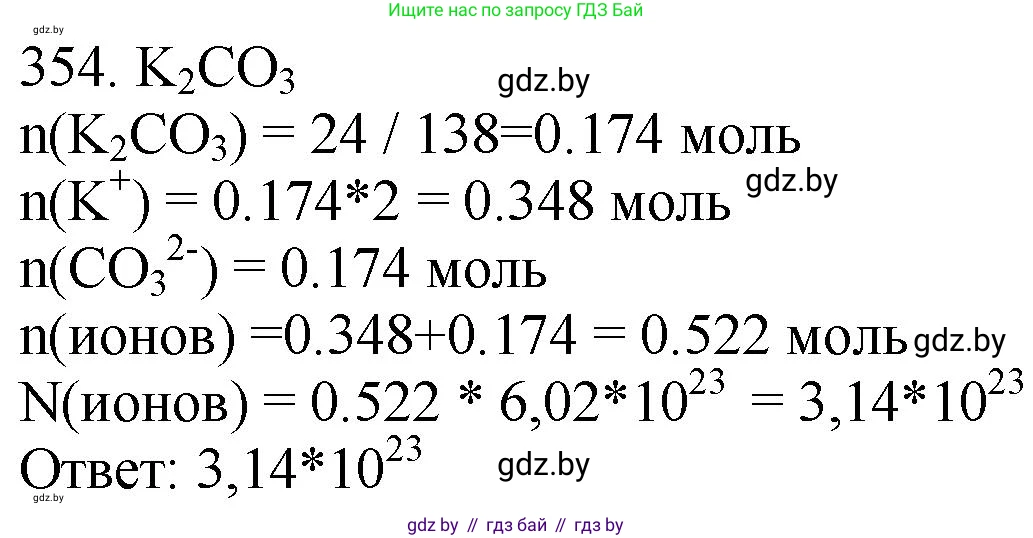
Решение 3. №354 (с. 56)
Дано:
$m(K_2CO_3) = 24$ г
$m(K_2CO_3) = 0.024$ кг
Найти:
$N_{ионов}$ - ?
Решение:
1. Для начала определим молярную массу карбоната калия ($K_2CO_3$). Она рассчитывается как сумма атомных масс всех атомов, входящих в состав молекулы. Воспользуемся периодической системой химических элементов Д.И. Менделеева для нахождения относительных атомных масс (с округлением до целых):
$Ar(K) = 39$ а.е.м.
$Ar(C) = 12$ а.е.м.
$Ar(O) = 16$ а.е.м.
Молярная масса $M$ численно равна относительной молекулярной массе $Mr$:
$M(K_2CO_3) = 2 \cdot Ar(K) + Ar(C) + 3 \cdot Ar(O) = 2 \cdot 39 + 12 + 3 \cdot 16 = 78 + 12 + 48 = 138$ г/моль.
2. Теперь найдем количество вещества (число молей) $n$ карбоната калия в образце массой 24 г, используя формулу:
$n = \frac{m}{M}$
$n(K_2CO_3) = \frac{24 \text{ г}}{138 \text{ г/моль}} = \frac{4}{23}$ моль $\approx 0.174$ моль.
3. Карбонат калия является ионным соединением. В твердом состоянии он состоит из ионов калия $K^+$ и карбонат-ионов $CO_3^{2-}$. Уравнение диссоциации для одной формульной единицы $K_2CO_3$ выглядит так:
$K_2CO_3 \rightarrow 2K^+ + CO_3^{2-}$
Из уравнения следует, что одна формульная единица карбоната калия содержит 2 иона калия ($K^+$) и 1 карбонат-ион ($CO_3^{2-}$). Суммарное число ионов в одной формульной единице:
$2 + 1 = 3$ иона.
4. Чтобы найти общее число ионов в образце, необходимо умножить количество вещества $n(K_2CO_3)$ на постоянную Авогадро $N_A$ ($N_A \approx 6.022 \times 10^{23}$ моль⁻¹) и на число ионов, образующихся из одной формульной единицы.
$N_{ионов} = n(K_2CO_3) \times N_A \times 3$
$N_{ионов} = \frac{4}{23} \text{ моль} \times 6.022 \times 10^{23} \text{ моль}^{-1} \times 3 = \frac{12}{23} \times 6.022 \times 10^{23}$
$N_{ионов} \approx 0.5217 \times 6.022 \times 10^{23} \approx 3.14 \times 10^{23}$ ионов.
Ответ: суммарное число ионов в образце карбоната калия массой 24 г составляет примерно $3.14 \times 10^{23}$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 354 расположенного на странице 56 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №354 (с. 56), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














