Номер 358, страница 56 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 3. Химическая связь и строение вещества. Параграф 13. Природа и типы химической связи - номер 358, страница 56.
№358 (с. 56)
Условие. №358 (с. 56)
скриншот условия

358. Массовая доля меди в соединении с золотом равна 13,89 %. Установите простейшую формулу этого соединения. Укажите тип химической связи между атомами в этом веществе.
Решение. №358 (с. 56)
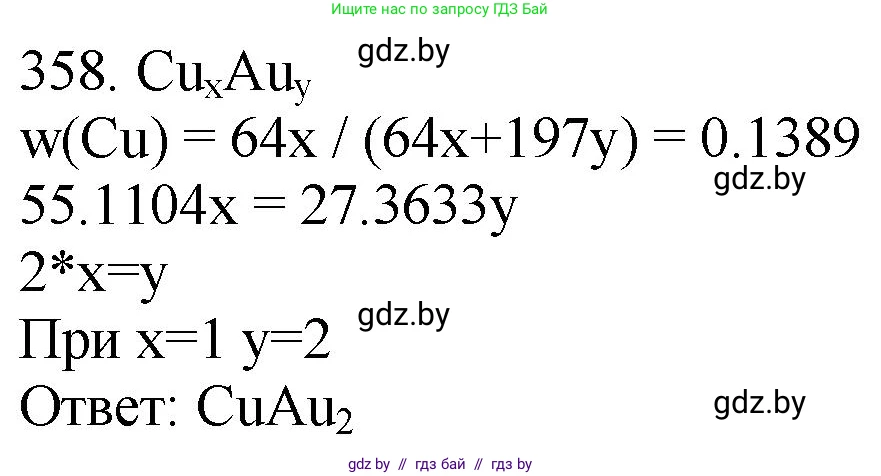
Решение 3. №358 (с. 56)
Дано:
Массовая доля меди в соединении с золотом: $\omega(\text{Cu}) = 13,89 \% = 0,1389$
Найти:
1. Простейшую формулу соединения.
2. Тип химической связи в веществе.
Решение:
1.Установление простейшей формулы соединения.
Предположим, что у нас есть 100 г этого соединения. Тогда масса меди в этом образце составит:
$m(\text{Cu}) = 100 \text{ г} \cdot 0,1389 = 13,89 \text{ г}$
Массовая доля золота в соединении будет равна:
$\omega(\text{Au}) = 100\% - 13,89\% = 86,11\% = 0,8611$
Следовательно, масса золота в 100 г образца составляет:
$m(\text{Au}) = 100 \text{ г} \cdot 0,8611 = 86,11 \text{ г}$
Теперь найдем количество вещества (число молей) для каждого элемента. Для этого используем молярные массы меди и золота (округленные значения из Периодической системы химических элементов Д.И. Менделеева):
$M(\text{Cu}) \approx 63,5 \text{ г/моль}$
$M(\text{Au}) \approx 197 \text{ г/моль}$
Количество вещества меди:
$n(\text{Cu}) = \frac{m(\text{Cu})}{M(\text{Cu})} = \frac{13,89 \text{ г}}{63,5 \text{ г/моль}} \approx 0,2187 \text{ моль}$
Количество вещества золота:
$n(\text{Au}) = \frac{m(\text{Au})}{M(\text{Au})} = \frac{86,11 \text{ г}}{197 \text{ г/моль}} \approx 0,4371 \text{ моль}$
Для нахождения простейшей формулы (например, $Au_xCu_y$) необходимо найти соотношение количеств веществ $x : y = n(\text{Au}) : n(\text{Cu})$. Для этого разделим оба значения на наименьшее из них (в данном случае, на $n(\text{Cu})$):
$x : y = \frac{n(\text{Au})}{n(\text{Cu})} : \frac{n(\text{Cu})}{n(\text{Cu})}$
$x : y = \frac{0,4371}{0,2187} : \frac{0,2187}{0,2187}$
$x : y \approx 2 : 1$
Таким образом, на один атом меди в соединении приходится два атома золота. Простейшая формула соединения — $Au_2Cu$.
2.Определение типа химической связи.
Соединение состоит из атомов золота (Au) и меди (Cu). Оба эти элемента являются металлами (переходными металлами). Химическая связь, которая образуется между атомами металлов, называется металлической связью. Она характеризуется наличием в кристаллической решетке положительно заряженных ионов металлов и свободно перемещающихся между ними обобществленных электронов («электронного газа»).
Ответ: простейшая формула соединения – $Au_2Cu$; тип химической связи между атомами в этом веществе – металлическая.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 358 расположенного на странице 56 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №358 (с. 56), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














