Номер 631, страница 106 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 5. Химия растворов. Параграф 23. Растворение как физико-химический процесс - номер 631, страница 106.
№631 (с. 106)
Условие. №631 (с. 106)
скриншот условия

631. *Кристаллогидрат карбоната натрия массой 2,86 г растворили в воде. Массовая доля карбоната натрия в растворе при этом составила 2,12 %, а масса раствора — 50,0 г. Установите формулу кристаллогидрата, использованного для приготовления раствора.
Решение. №631 (с. 106)
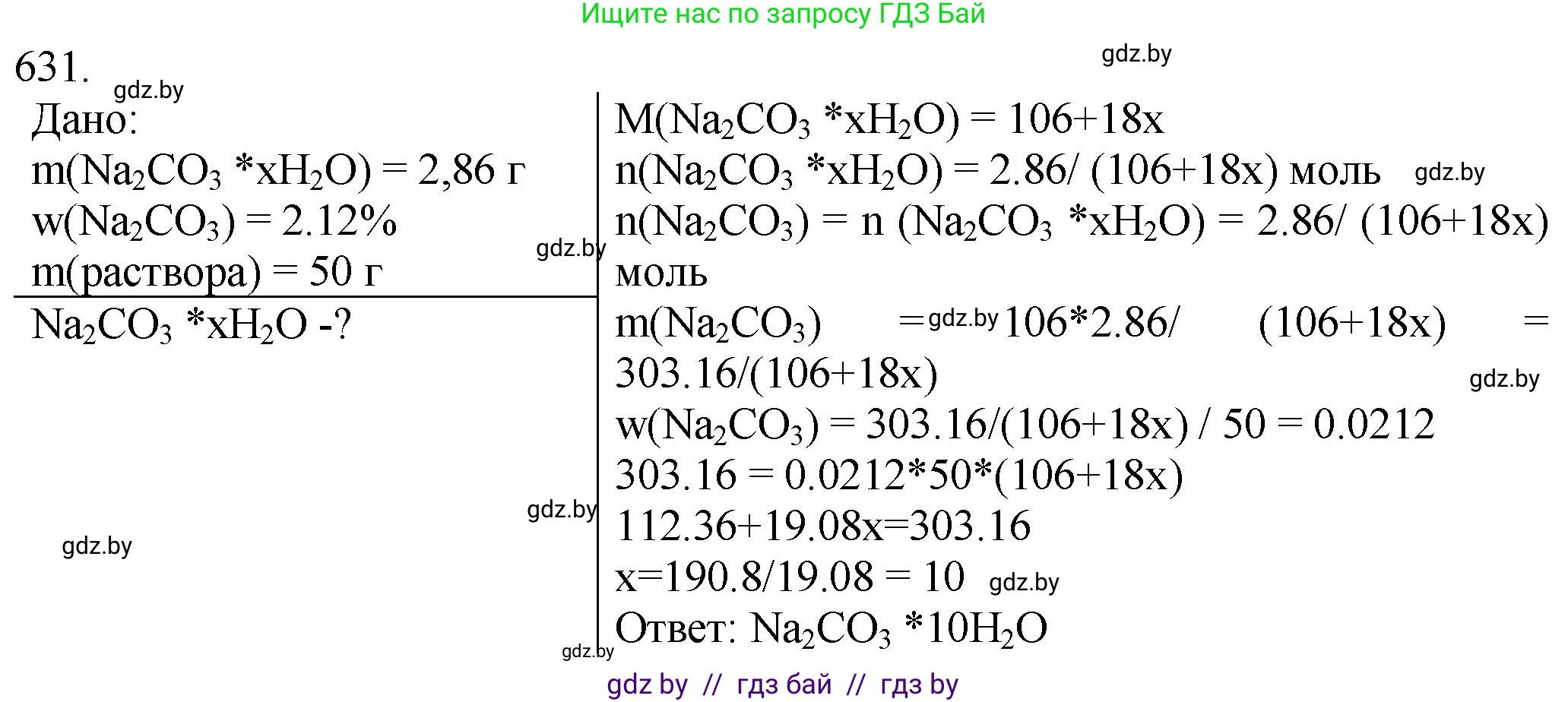
Решение 3. №631 (с. 106)
Дано:
$m(Na_2CO_3 \cdot xH_2O) = 2,86 \text{ г}$
$m_{р-ра} = 50,0 \text{ г}$
$\omega(Na_2CO_3) = 2,12 \% = 0,0212$
Найти:
Формулу кристаллогидрата - $Na_2CO_3 \cdot xH_2O$
Решение:
1. Общая формула кристаллогидрата карбоната натрия — $Na_2CO_3 \cdot xH_2O$. Наша задача — найти коэффициент $x$.
2. Сначала определим массу безводного карбоната натрия ($Na_2CO_3$) в конечном растворе, используя данные о массе раствора и массовой доле вещества.
$m(Na_2CO_3) = m_{р-ра} \cdot \omega(Na_2CO_3)$
$m(Na_2CO_3) = 50,0 \text{ г} \cdot 0,0212 = 1,06 \text{ г}$
Эта масса карбоната натрия содержалась в исходной навеске кристаллогидрата.
3. Теперь мы можем найти массу кристаллизационной воды в исходном образце. Масса кристаллогидрата состоит из массы безводной соли и массы воды.
$m(H_2O)_{\text{крист.}} = m(Na_2CO_3 \cdot xH_2O) - m(Na_2CO_3)$
$m(H_2O)_{\text{крист.}} = 2,86 \text{ г} - 1,06 \text{ г} = 1,80 \text{ г}$
4. Чтобы найти соотношение между солью и водой в кристаллогидрате (коэффициент $x$), необходимо найти их количества вещества (в молях). Для этого рассчитаем молярные массы.
Молярная масса карбоната натрия:
$M(Na_2CO_3) = 2 \cdot Ar(Na) + Ar(C) + 3 \cdot Ar(O) = 2 \cdot 23 + 12 + 3 \cdot 16 = 106 \text{ г/моль}$
Молярная масса воды:
$M(H_2O) = 2 \cdot Ar(H) + Ar(O) = 2 \cdot 1 + 16 = 18 \text{ г/моль}$
5. Рассчитаем количество вещества карбоната натрия и воды:
$\nu(Na_2CO_3) = \frac{m(Na_2CO_3)}{M(Na_2CO_3)} = \frac{1,06 \text{ г}}{106 \text{ г/моль}} = 0,01 \text{ моль}$
$\nu(H_2O) = \frac{m(H_2O)}{M(H_2O)} = \frac{1,80 \text{ г}}{18 \text{ г/моль}} = 0,10 \text{ моль}$
6. Соотношение количеств веществ в кристаллогидрате $\nu(Na_2CO_3) : \nu(H_2O)$ соответствует соотношению индексов в его формуле $1 : x$.
$x = \frac{\nu(H_2O)}{\nu(Na_2CO_3)} = \frac{0,10 \text{ моль}}{0,01 \text{ моль}} = 10$
Таким образом, формула кристаллогидрата — $Na_2CO_3 \cdot 10H_2O$.
Ответ: Формула кристаллогидрата — $Na_2CO_3 \cdot 10H_2O$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 631 расположенного на странице 106 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №631 (с. 106), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














