Номер 4, страница 32, часть 1 - гдз по химии 7 класс тетрадь для практических работ Борушко

Авторы: Борушко И. И.
Тип: Тетрадь для практических работ
Издательство: Сэр-Вит
Год издания: 2022 - 2025
Часть: 1
Цвет обложки: розовый с колбами
ISBN: 978-985-597-590-9
Рекомендовано Научно-методическим учреждением «Национальный институт образования» Министерства образования Республики Беларусь
Популярные ГДЗ в 7 классе
Часть 1. Практические работы. Химический эксперимент. Практическая работа 6. Решение экспериментальных задач - номер 4, страница 32.
№4 (с. 32)
Условие. №4 (с. 32)
скриншот условия

4. К раствору кислоты:
а) $H_2SO_4$;
б) $H_3PO_4$
добавьте 1–2 капли метилоранжа, а затем раствор щелочи гидроксида калия до изменения окраски.
Объясните наблюдаемое явление.
Решение. №4 (с. 32)
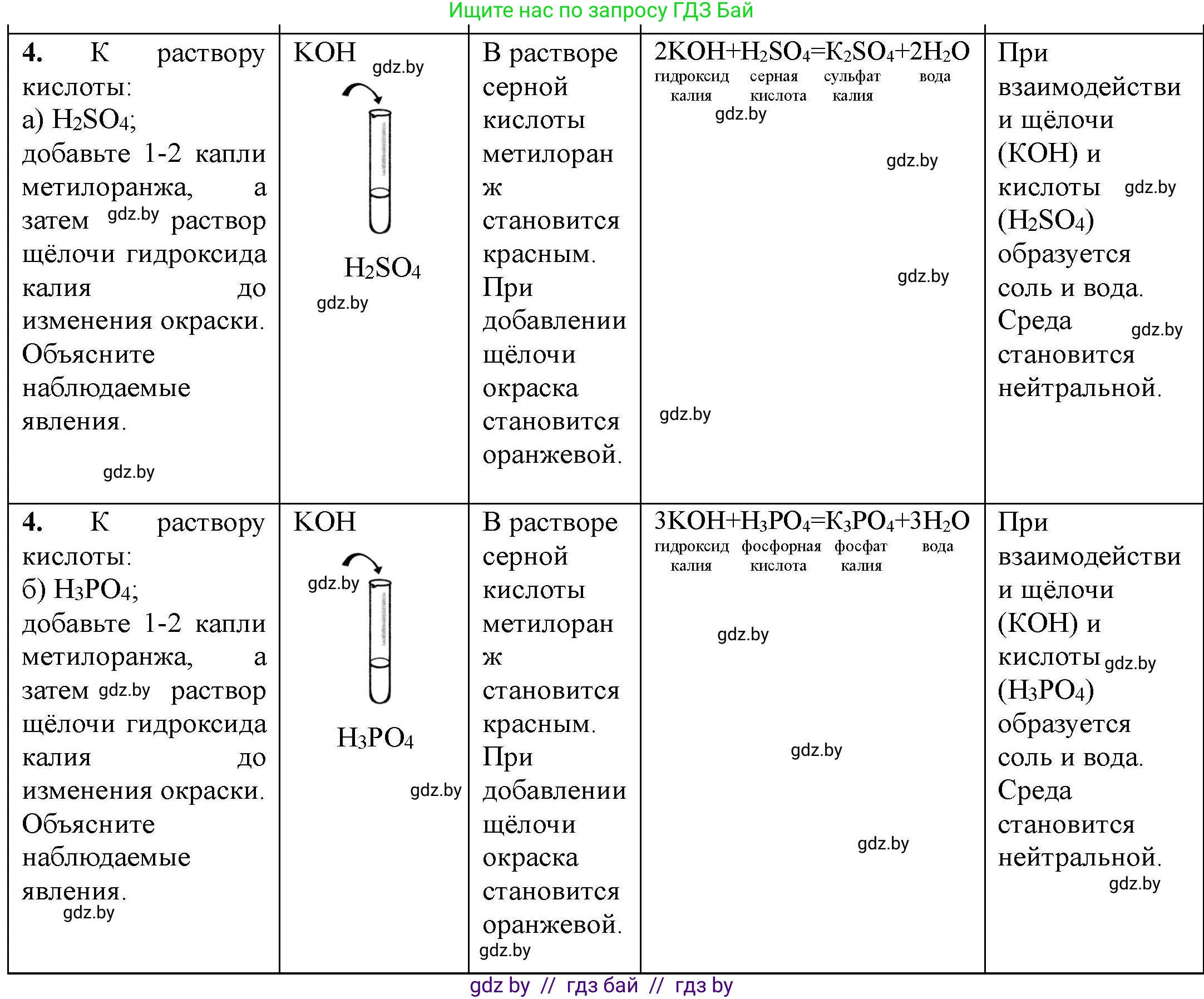
Решение 2. №4 (с. 32)
a) H2SO4
Изначально, при добавлении 1-2 капель метилоранжа к раствору серной кислоты ($H_2SO_4$), раствор окрасится в красный цвет. Это происходит потому, что серная кислота является сильной кислотой, и метилоранж в кислой среде (pH < 3.1) имеет красный цвет.
При последующем добавлении раствора щелочи гидроксида калия ($KOH$) до изменения окраски, цвет раствора изменится с красного на оранжевый, а затем на желтый.
Объяснение: Происходит реакция нейтрализации между серной кислотой и гидроксидом калия. Уравнение реакции:$H_2SO_4(aq) + 2KOH(aq) \rightarrow K_2SO_4(aq) + 2H_2O(l)$В ходе этой реакции ионы водорода ($H^+$) из кислоты взаимодействуют с гидроксид-ионами ($OH^-$) из щелочи, образуя воду. Это приводит к постепенному уменьшению концентрации $H^+$ и увеличению pH раствора. Метилоранж является кислотно-основным индикатором, который меняет свою окраску в диапазоне pH 3.1-4.4 (от красного в кислой среде до желтого в щелочной). При достижении точки эквивалентности, когда кислота практически полностью нейтрализована, pH раствора резко возрастает, и индикатор меняет свой цвет, сигнализируя о завершении реакции нейтрализации.
Ответ: Изначально раствор красный, при добавлении KOH становится оранжевым, затем желтым.
б) H3PO4
Изначально, при добавлении 1-2 капель метилоранжа к раствору фосфорной кислоты ($H_3PO_4$), раствор также окрасится в красный цвет. Это связано с тем, что фосфорная кислота, хотя и является кислотой средней силы, создает кислую среду.
При последующем добавлении раствора щелочи гидроксида калия ($KOH$) до изменения окраски, цвет раствора изменится с красного на оранжевый, а затем на желтый.
Объяснение: Происходит реакция нейтрализации между фосфорной кислотой и гидроксидом калия. Фосфорная кислота является многоосновной кислотой, однако метилоранж (с диапазоном pH 3.1-4.4) позволяет зафиксировать преимущественно первую стадию нейтрализации:$H_3PO_4(aq) + KOH(aq) \rightarrow KH_2PO_4(aq) + H_2O(l)$По мере добавления щелочи, концентрация ионов $H^+$ уменьшается, и pH раствора увеличивается. Когда pH достигает интервала изменения окраски метилоранжа (3.1-4.4), индикатор меняет свой цвет с красного на оранжево-желтый, сигнализируя о завершении первой стадии нейтрализации.
Ответ: Изначально раствор красный, при добавлении KOH становится оранжевым, затем желтым.
Объясните наблюдаемое явление.
Наблюдаемое явление – это **реакция нейтрализации**, которая представляет собой химическое взаимодействие кислоты и основания (щелочи), в результате которого образуется соль и вода. В данном случае, это реакция между серной ($H_2SO_4$) или фосфорной ($H_3PO_4$) кислотой и гидроксидом калия ($KOH$). Общее уравнение реакции можно представить как:$Acid(aq) + Base(aq) \rightarrow Salt(aq) + Water(l)$
Для отслеживания этой реакции используется **кислотно-основной индикатор** – метилоранж. Индикаторы – это органические соединения, которые обладают способностью изменять свою окраску в зависимости от pH среды, то есть от концентрации ионов водорода ($H^+$). Метилоранж имеет красный цвет в сильнокислой среде (pH < 3.1), оранжевый в переходной зоне (pH 3.1-4.4) и желтый в щелочной среде (pH > 4.4).
При добавлении раствора щелочи ($KOH$) к раствору кислоты происходит постепенное расходование ионов водорода ($H^+$), присутствующих в кислоте, за счет их реакции с гидроксид-ионами ($OH^-$) из щелочи, что приводит к образованию воды и увеличению pH раствора. Когда концентрация ионов $H^+$ снижается до критического уровня, соответствующего интервалу изменения окраски метилоранжа (pH 3.1-4.4), индикатор претерпевает структурные изменения, которые проявляются в видимом изменении цвета (с красного на оранжевый, а затем на желтый). Это сигнализирует о том, что среда перестала быть сильнокислой и стала нейтральной или слабощелочной, достигнув точки нейтрализации.
Ответ: Наблюдаемое явление - это реакция нейтрализации кислоты щелочью, отслеживаемая с помощью кислотно-основного индикатора метилоранжа, который изменяет цвет раствора при изменении pH от кислого к нейтральному/щелочному.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 7 класс, для упражнения номер 4 расположенного на странице 32 для 1-й части к тетради для практических работ 2022 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №4 (с. 32), автора: Борушко (Ирина Ивановна), 1-й части учебного пособия издательства Сэр-Вит.













