Номер 1, страница 30, часть 1 - гдз по химии 7 класс тетрадь для практических работ Борушко

Авторы: Борушко И. И.
Тип: Тетрадь для практических работ
Издательство: Сэр-Вит
Год издания: 2022 - 2025
Часть: 1
Цвет обложки: розовый с колбами
ISBN: 978-985-597-590-9
Рекомендовано Научно-методическим учреждением «Национальный институт образования» Министерства образования Республики Беларусь
Популярные ГДЗ в 7 классе
Часть 1. Практические работы. Химический эксперимент. Практическая работа 6. Решение экспериментальных задач - номер 1, страница 30.
№1 (с. 30)
Условие. №1 (с. 30)
скриншот условия

Экспериментальные задачи
Выполнение опыта
Наблюдения
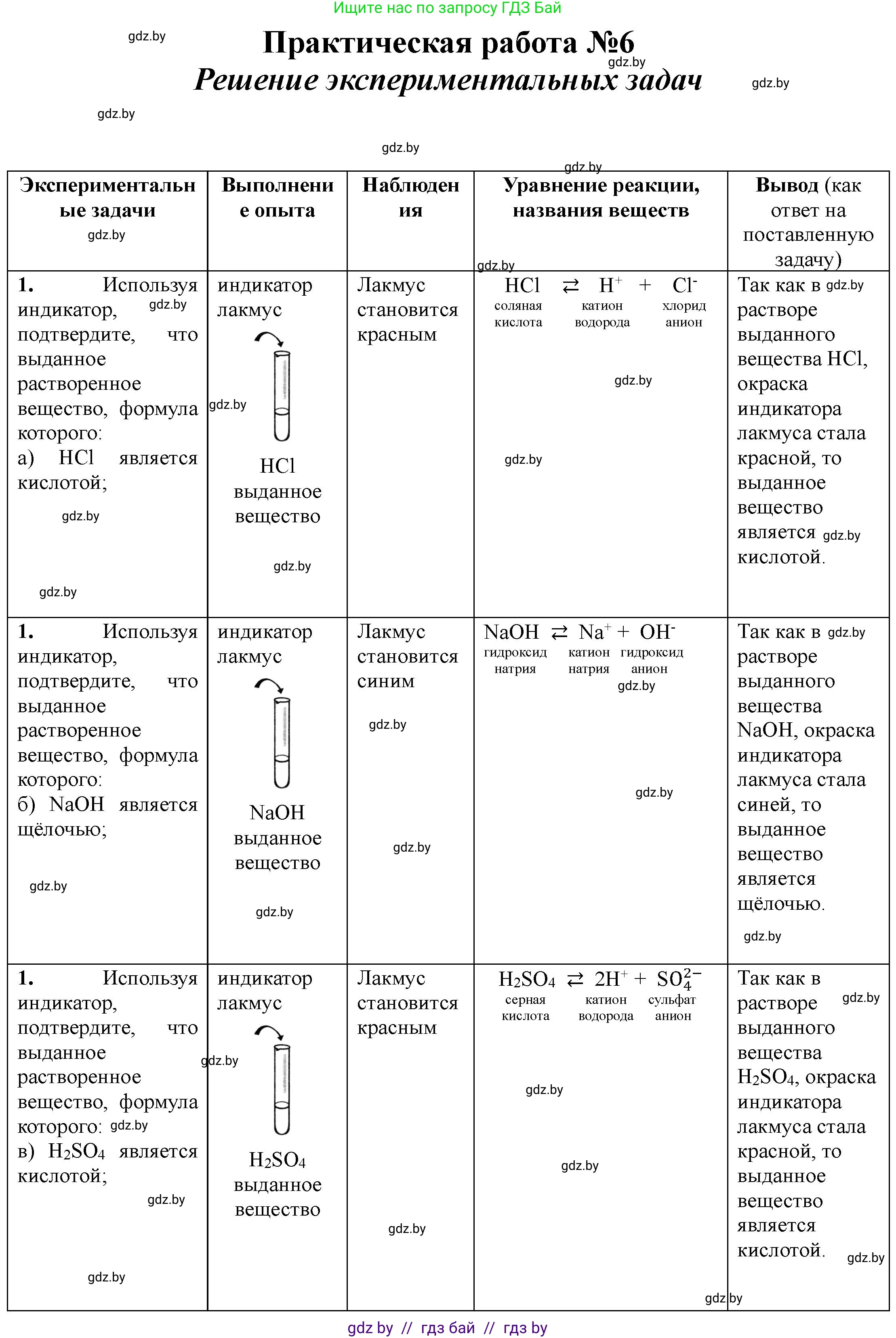
1. Используя индикатор, подтвердите, что выданное растворенное вещество, формула которого:
а) $ \text{HCl} $ является кислотой;
б) $ \text{NaOH} $ является щелочью;
в) $ \text{H}_2\text{SO}_4 $ является кислотой;
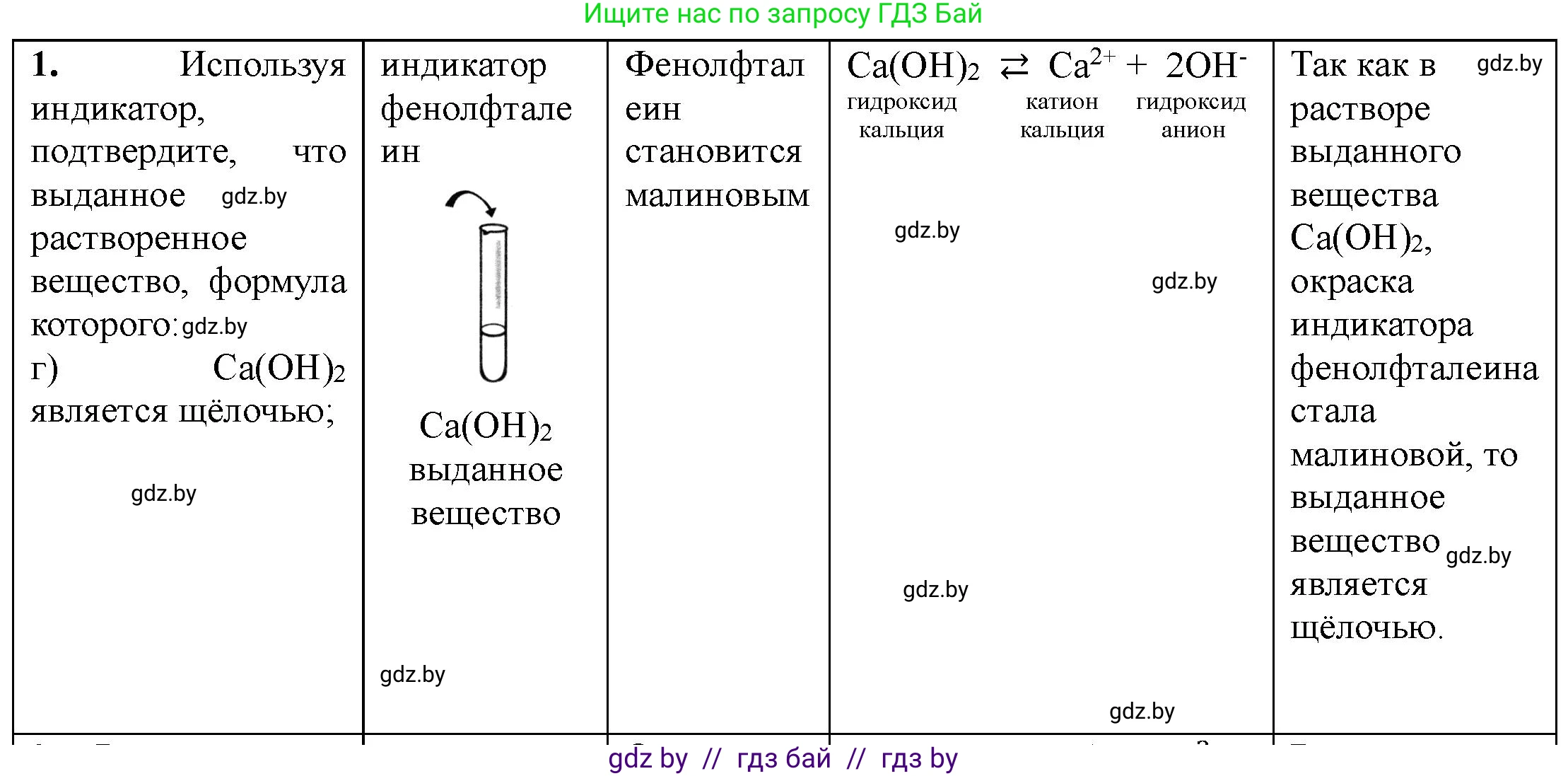
г) $ \text{Ca(OH)}_2 $ является щелочью.
индикатор
выданное вещество
Решение. №1 (с. 30)
Решение 2. №1 (с. 30)
Дано:
Выданные растворенные вещества: $\text{HCl}$, $\text{NaOH}$, $\text{H}_2\text{SO}_4$, $\text{Ca(OH)}_2$.
Индикатор.
Найти:
Подтвердить, что каждое из выданных веществ является кислотой или щелочью, используя индикатор.
Решение:
Для подтверждения кислотной или щелочной природы растворенных веществ используют кислотно-основные индикаторы. Индикаторы – это органические красители, которые изменяют свой цвет в зависимости от концентрации ионов водорода ($\text{H}^+$) или гидроксид-ионов ($\text{OH}^-$) в растворе, то есть от его pH.
Наиболее часто используемые индикаторы и их изменения цвета:
Лакмус: в кислой среде – красный; в нейтральной – фиолетовый; в щелочной – синий.
Фенолфталеин: в кислой и нейтральной среде – бесцветный; в щелочной – малиновый (или розовый).
Метиловый оранжевый: в сильно кислой среде – красный; в нейтральной/слабо кислой – оранжевый; в щелочной – желтый.
Универсальный индикатор: смесь нескольких индикаторов, которая показывает широкий спектр цветов в зависимости от pH, от красного/оранжевого (сильно кислый) до синего/фиолетового (сильно щелочной).
Проведение опыта для каждого вещества будет заключаться в добавлении нескольких капель подходящего индикатора к небольшому объему раствора в пробирке и наблюдении за изменением цвета.
a) HCl является кислотой;
Выполнение опыта: К небольшому количеству раствора соляной кислоты ($\text{HCl}$) в пробирке добавить несколько капель универсального индикатора или опустить лакмусовую бумажку.
Наблюдения: Универсальный индикатор окрасится в красный или оранжевый цвет. Лакмусовая бумажка станет красной. Это свидетельствует о кислой среде раствора, так как соляная кислота является сильной кислотой и диссоциирует в воде с образованием большого количества ионов водорода ($\text{H}^+$).
Ответ: $\text{HCl}$ является кислотой, так как раствор изменяет цвет индикатора на характерный для кислой среды (например, лакмус становится красным).
б) NaOH является щелочью;
Выполнение опыта: К небольшому количеству раствора гидроксида натрия ($\text{NaOH}$) в пробирке добавить несколько капель универсального индикатора или опустить лакмусовую бумажку. Можно также использовать фенолфталеин.
Наблюдения: Универсальный индикатор окрасится в синий или фиолетовый цвет. Лакмусовая бумажка станет синей. При добавлении фенолфталеина раствор окрасится в малиновый цвет. Это подтверждает щелочную среду раствора, так как гидроксид натрия является сильной щелочью и диссоциирует в воде с образованием большого количества гидроксид-ионов ($\text{OH}^-$).
Ответ: $\text{NaOH}$ является щелочью, так как раствор изменяет цвет индикатора на характерный для щелочной среды (например, лакмус становится синим, фенолфталеин - малиновым).
в) H₂SO₄ является кислотой;
Выполнение опыта: К небольшому количеству раствора серной кислоты ($\text{H}_2\text{SO}_4$) в пробирке добавить несколько капель универсального индикатора или опустить лакмусовую бумажку.
Наблюдения: Универсальный индикатор окрасится в красный цвет. Лакмусовая бумажка станет красной. Это подтверждает кислую среду раствора, так как серная кислота является сильной кислотой и диссоциирует в воде с образованием ионов водорода ($\text{H}^+$).
Ответ: $\text{H}_2\text{SO}_4$ является кислотой, так как раствор изменяет цвет индикатора на характерный для кислой среды (например, лакмус становится красным).
г) Ca(OH)₂ является щелочью.
Выполнение опыта: К небольшому количеству насыщенного раствора гидроксида кальция ($\text{Ca(OH)}_2$, известковой воды) в пробирке добавить несколько капель универсального индикатора или опустить лакмусовую бумажку. Можно также использовать фенолфталеин.
Наблюдения: Универсальный индикатор окрасится в синий или фиолетовый цвет. Лакмусовая бумажка станет синей. При добавлении фенолфталеина раствор окрасится в малиновый цвет. Это подтверждает щелочную среду раствора, так как гидроксид кальция, хоть и малорастворим, является сильным основанием, и его насыщенный раствор имеет щелочную реакцию за счет образования гидроксид-ионов ($\text{OH}^-$).
Ответ: $\text{Ca(OH)}_2$ является щелочью, так как раствор изменяет цвет индикатора на характерный для щелочной среды (например, лакмус становится синим, фенолфталеин - малиновым).
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 7 класс, для упражнения номер 1 расположенного на странице 30 для 1-й части к тетради для практических работ 2022 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №1 (с. 30), автора: Борушко (Ирина Ивановна), 1-й части учебного пособия издательства Сэр-Вит.













