лабораторный опыт 1, страница 2, часть 2 - гдз по химии 8 класс тетрадь для практических работ Борушко
Авторы: Борушко И. И.
Тип: Тетрадь для практических работ
Издательство: Сэр-Вит
Год издания: 2022 - 2025
Часть: 2
Цвет обложки: розовый с пробирками
ISBN: 978-985-597-607-4
Рекомендовано Научно-методическим учреждением «Национальный институт образования» Министерства образования Республики Беларусь
Популярные ГДЗ в 8 классе
Часть 2. Лабораторные опыты. Получение нерастворимого основания - страница 2.
лабораторный опыт 1 (с. 2)
Условие. лабораторный опыт 1 (с. 2)
скриншот условия


Лабораторный опыт 1. 20__ г.
Получение нерастворимого основания
Цель: получить нерастворимые основания в результате взаимодействия растворов солей со щелочью.
Реактивы: гидроксид натрия, сульфат меди(II), сульфат магния, хлорид железа(III).
Выполнение опыта
Наблюдения
Уравнения реакций, тип
Проведите опыты с минимальными количествами реактивов по схеме:
$NaOH$ (стрелка к пробирке)
$CuSO_4$
(Пустое поле для наблюдений)
$CuSO_4 + ...NaOH = ... + ...$
$NaOH$ (стрелка к пробирке)
$MgSO_4$
(Пустое поле для наблюдений)
$... + ... = ... + ...$
$NaOH$ (стрелка к пробирке)
$FeCl_3$
(Пустое поле для наблюдений)
$... + ... = ... + ...$
Вывод. Нерастворимые основания получают взаимодействием ________ и ________.
Задание
Был проведен эксперимент по схеме:
$NaOH$ (стрелка к пробирке) $CuCl_2$
$NaOH$ (стрелка к пробирке) $FeCl_2$
$KOH$ (стрелка к пробирке) $FeCl_2$
$KOH$ (стрелка к пробирке) $FeCl_3$
Укажите признак каждой проведенной реакции. Составьте уравнения химических реакций.
_____________________________________________________________________________________
_____________________________________________________________________________________
_____________________________________________________________________________________
_____________________________________________________________________________________
_____________________________________________________________________________________
Решение. лабораторный опыт 1 (с. 2)

Решение 2. лабораторный опыт 1 (с. 2)
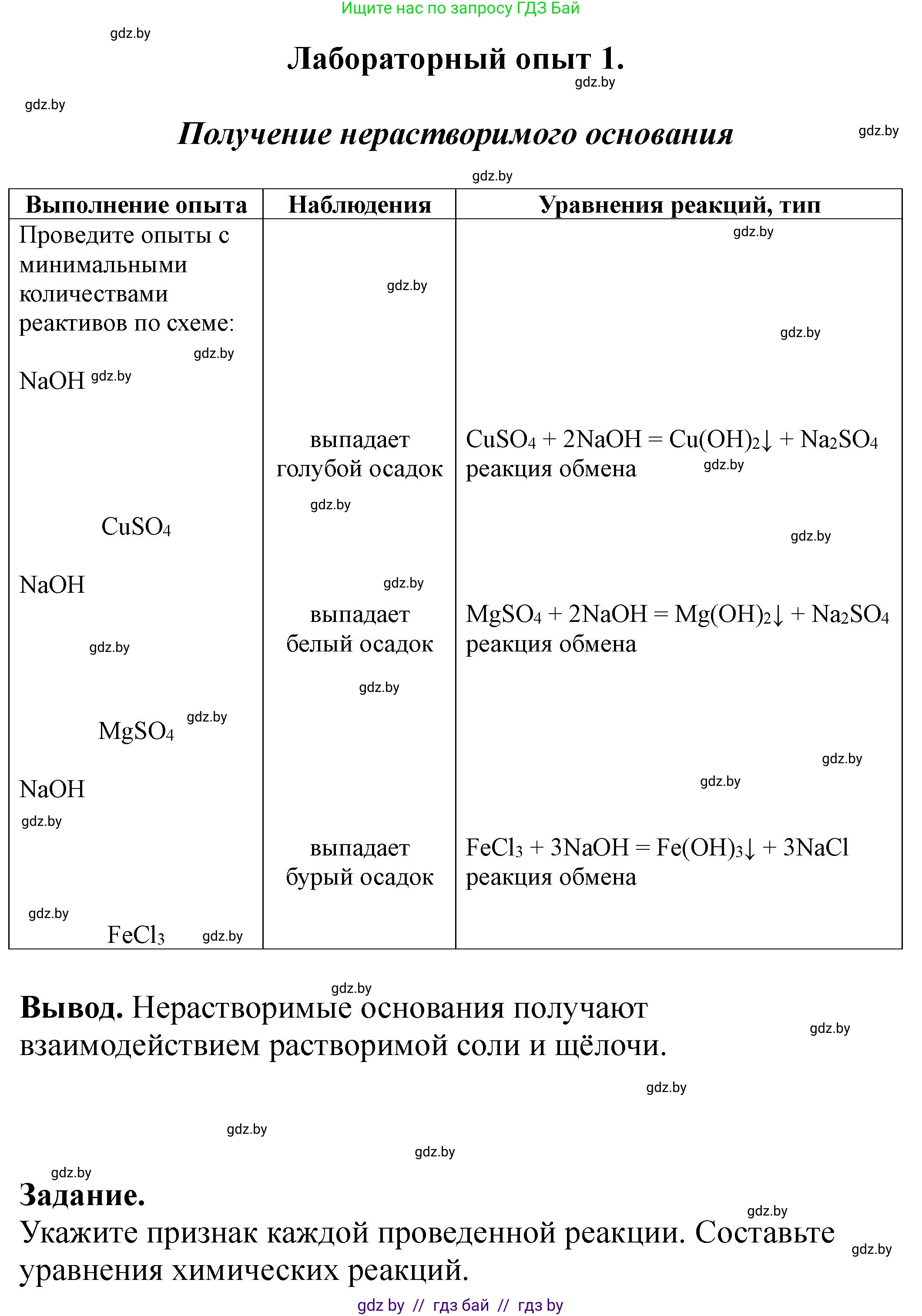
Выполнение опыта
* NaOH + CuSO₄
Наблюдения: Образование голубого студенистого осадка.
Уравнение реакции, тип: $CuSO_4 + 2NaOH \rightarrow Cu(OH)_2 \downarrow + Na_2SO_4$. Тип: реакция обмена.
Ответ:
* NaOH + MgSO₄
Наблюдения: Образование белого студенистого осадка.
Уравнение реакции, тип: $MgSO_4 + 2NaOH \rightarrow Mg(OH)_2 \downarrow + Na_2SO_4$. Тип: реакция обмена.
Ответ:
* NaOH + FeCl₃
Наблюдения: Образование бурого (красно-коричневого) студенистого осадка.
Уравнение реакции, тип: $FeCl_3 + 3NaOH \rightarrow Fe(OH)_3 \downarrow + 3NaCl$. Тип: реакция обмена.
Ответ:
Вывод
Нерастворимые основания получают взаимодействием растворов солей и щелочей.
Ответ:
Задание
* NaOH + CuCl₂
Признак реакции: Образование голубого студенистого осадка.
Уравнение реакции: $CuCl_2 + 2NaOH \rightarrow Cu(OH)_2 \downarrow + 2NaCl$.
Ответ:
* NaOH + FeCl₂
Признак реакции: Образование белого (с зеленоватым оттенком) студенистого осадка, который на воздухе быстро буреет.
Уравнение реакции: $FeCl_2 + 2NaOH \rightarrow Fe(OH)_2 \downarrow + 2NaCl$.
Ответ:
* KOH + FeCl₂
Признак реакции: Образование белого (с зеленоватым оттенком) студенистого осадка, который на воздухе быстро буреет.
Уравнение реакции: $FeCl_2 + 2KOH \rightarrow Fe(OH)_2 \downarrow + 2KCl$.
Ответ:
* KOH + FeCl₃
Признак реакции: Образование бурого (красно-коричневого) студенистого осадка.
Уравнение реакции: $FeCl_3 + 3KOH \rightarrow Fe(OH)_3 \downarrow + 3KCl$.
Ответ:
Другие задания:
вариант 2
стр. 14вариант 3
стр. 14вариант 4
стр. 14вариант 1
стр. 18вариант 2
стр. 18вариант 3
стр. 18вариант 4
стр. 18лабораторный опыт 1
стр. 2лабораторный опыт 2
стр. 4лабораторный опыт 3
стр. 6лабораторный опыт 4
стр. 91
стр. 112
стр. 113
стр. 124
стр. 12к содержанию
список заданийПомогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения лабораторный опыт 1 расположенного на странице 2 для 2-й части к тетради для практических работ 2022 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению лабораторный опыт 1 (с. 2), автора: Борушко (Ирина Ивановна), 2-й части учебного пособия издательства Сэр-Вит.














