Номер 105, страница 30 - гдз по химии 9 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2020 - 2025
Цвет обложки: салатовый, голубой с колбами
ISBN: 978-985-599-248-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 9 классе
Глава 2. Электролитическая диссоциация. Параграф 7. Электролиты и неэлектролиты - номер 105, страница 30.
№105 (с. 30)
Условие. №105 (с. 30)
скриншот условия

105. Все ли соединения с ионной химической связью являются электролитами? Подтвердите ответ соответствующими примерами.
Решение. №105 (с. 30)
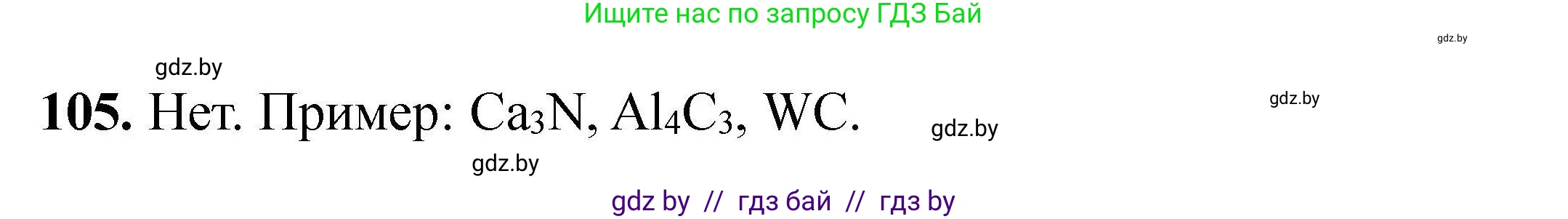
Решение 2. №105 (с. 30)
Да, все соединения с ионной химической связью являются электролитами. Однако важно понимать, что они проявляют способность проводить электрический ток (то есть ведут себя как электролиты) только при определенных условиях: в расплаве или в растворе.
В твердом состоянии ионные соединения образуют кристаллическую решетку. В узлах этой решетки находятся ионы, которые жестко зафиксированы и не могут свободно перемещаться. Поскольку для проведения электрического тока необходимо направленное движение заряженных частиц, твердые ионные соединения являются диэлектриками (не проводят ток).
При плавлении или растворении в полярном растворителе (например, в воде) кристаллическая решетка разрушается. Ионы становятся подвижными и могут свободно перемещаться по всему объему расплава или раствора. Наличие этих подвижных ионов и обусловливает способность вещества проводить электрический ток.
Подтвердим это соответствующими примерами:
Хлорид натрия ($NaCl$) — типичное ионное соединение, которое в быту известно как поваренная соль. В твердом кристаллическом виде он не проводит электрический ток. Однако его расплав или водный раствор являются хорошими электролитами, так как в них происходит диссоциация на подвижные ионы $Na^{+}$ и $Cl^{-}$. Уравнение диссоциации в воде:
$NaCl \xrightarrow{H_2O} Na^{+} + Cl^{-}$
Поэтому хлорид натрия — это сильный электролит.
Сульфат бария ($BaSO_4$) — также является ионным соединением. Он считается практически нерастворимым в воде. Тем не менее, очень незначительная его часть все же растворяется и диссоциирует на ионы $Ba^{2+}$ и $SO_4^{2-}$. Уравнение диссоциации в воде:
$BaSO_4 \rightleftharpoons Ba^{2+}_{(aq)} + SO_4^{2-}_{(aq)}$
Из-за крайне низкой концентрации ионов в насыщенном растворе его электропроводность очень слабая, но она измерима. Таким образом, даже практически нерастворимые ионные соединения являются (очень слабыми) электролитами.
Ответ: Да, все соединения с ионной связью являются электролитами, так как они состоят из ионов и способны диссоциировать на них в расплаве или растворе. Свойства электролита (электропроводность) они проявляют только в этих состояниях, когда ионы становятся подвижными. В твердом состоянии ионные соединения ток не проводят.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 9 класс, для упражнения номер 105 расположенного на странице 30 к сборнику задач 2020 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №105 (с. 30), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














