Номер 127, страница 26 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 1. Основные понятия и законы химии. Параграф 4. Количественные характеристики вещества - номер 127, страница 26.
№127 (с. 26)
Условие. №127 (с. 26)
скриншот условия

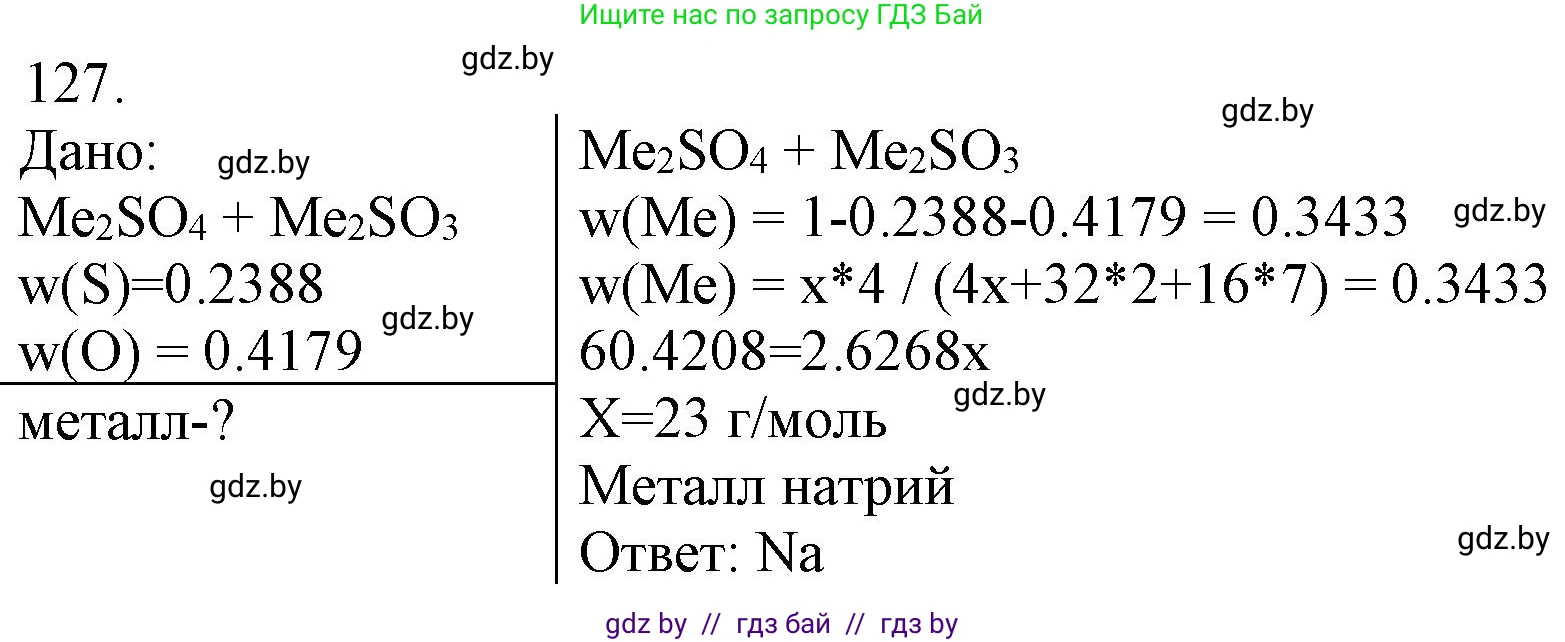
127. *В смеси сульфата и сульфита щелочного металла массовые доли серы и кислорода соответственно равны 0,2388 и 0,4179. Установите металл.
Решение. №127 (с. 26)
Решение 3. №127 (с. 26)
Дано:
Смесь сульфата ($Me_2SO_4$) и сульфита ($Me_2SO_3$) щелочного металла.
Массовая доля серы: $\omega(S) = 0,2388$
Массовая доля кислорода: $\omega(O) = 0,4179$
Найти:
Неизвестный щелочной металл (Me).
Решение:
1. Обозначим неизвестный щелочной металл символом Me. Так как это щелочной металл (I группа), его степень окисления в соединениях равна +1. Формула сульфата этого металла — $Me_2SO_4$, а сульфита — $Me_2SO_3$.
2. Сумма массовых долей всех элементов в смеси равна 1 (или 100%). Найдем массовую долю щелочного металла в смеси:
$\omega(Me) = 1 - \omega(S) - \omega(O)$
$\omega(Me) = 1 - 0,2388 - 0,4179 = 0,3433$
3. В обеих солях, сульфате $Me_2SO_4$ и сульфите $Me_2SO_3$, на один атом серы (S) приходится два атома металла (Me). Это означает, что в любой смеси этих солей молярное соотношение атомов металла и серы будет постоянным и равным 2:1.
$n(Me) : n(S) = 2 : 1$, или $n(Me) = 2 \cdot n(S)$
4. Выразим количество вещества (число молей, $n$) каждого элемента через его массовую долю ($\omega$) и молярную массу ($M$). Для произвольной массы смеси $m_{смеси}$:
$n = \frac{m}{M} = \frac{\omega \cdot m_{смеси}}{M}$
Подставим это в наше соотношение:
$\frac{\omega(Me) \cdot m_{смеси}}{M(Me)} = 2 \cdot \frac{\omega(S) \cdot m_{смеси}}{M(S)}$
Массу смеси $m_{смеси}$ можно сократить:
$\frac{\omega(Me)}{M(Me)} = 2 \cdot \frac{\omega(S)}{M(S)}$
5. Подставим известные значения. Молярная масса серы $M(S) \approx 32,07$ г/моль. Обозначим искомую молярную массу металла как $M_{Me}$.
$\frac{0,3433}{M_{Me}} = 2 \cdot \frac{0,2388}{32,07}$
$\frac{0,3433}{M_{Me}} = \frac{0,4776}{32,07}$
6. Решим уравнение относительно $M_{Me}$:
$M_{Me} = \frac{0,3433 \cdot 32,07}{0,4776}$
$M_{Me} = \frac{11,009931}{0,4776} \approx 23,05$ г/моль
7. Полученное значение молярной массы (23,05 г/моль) соответствует молярной массе натрия (Na), которая равна 22,99 г/моль. Следовательно, неизвестный щелочной металл — натрий.
Ответ: Натрий (Na).
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 127 расположенного на странице 26 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №127 (с. 26), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














