Номер 140, страница 29 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 1. Основные понятия и законы химии. Параграф 5. Основные законы химии. Закон постоянства состава вещества. Закон сохранения массы веществ - номер 140, страница 29.
№140 (с. 29)
Условие. №140 (с. 29)
скриншот условия

140. Смесь цинка и сульфида цинка массой 22,7 г полностью растворили в избытке соляной кислоты. В результате реакции выделился газ объёмом (н. у.) 6,72 $\text{дм}^3$. Рассчитайте массовую долю цинка в смеси.
Решение. №140 (с. 29)

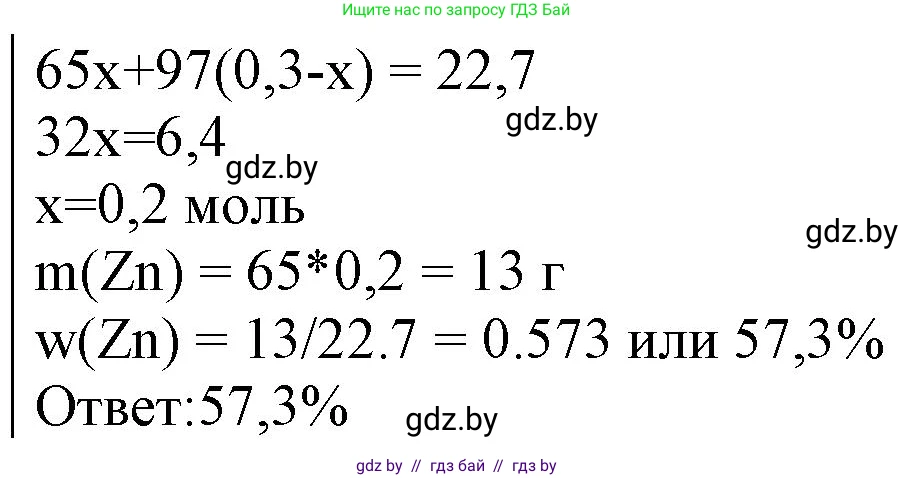
Решение 3. №140 (с. 29)
Дано:
$m(\text{смеси}) = 22,7 \text{ г}$
$V(\text{газов}) = 6,72 \text{ дм}^3$ (н. у.)
$m(\text{смеси}) = 22,7 \cdot 10^{-3} \text{ кг} = 0,0227 \text{ кг}$
$V(\text{газов}) = 6,72 \cdot 10^{-3} \text{ м}^3 = 0,00672 \text{ м}^3$
Найти:
$\omega(Zn)$ - ?
Решение:
При растворении смеси цинка и сульфида цинка в избытке соляной кислоты протекают две химические реакции. В обеих реакциях выделяются газы: в первой — водород ($H_2$), во второй — сероводород ($H_2S$).
1) $Zn + 2HCl \rightarrow ZnCl_2 + H_2\uparrow$
2) $ZnS + 2HCl \rightarrow ZnCl_2 + H_2S\uparrow$
Общий объем выделившихся газов при нормальных условиях (н. у.) составляет 6,72 дм³. Используя молярный объем газов при н. у. ($V_m = 22,4 \text{ дм}^3/\text{моль}$), найдем общее количество вещества газов.
$n(\text{газов}) = \frac{V(\text{газов})}{V_m} = \frac{6,72 \text{ дм}^3}{22,4 \text{ дм}^3/\text{моль}} = 0,3 \text{ моль}$
Пусть в исходной смеси содержалось $x$ моль цинка ($n(Zn) = x$) и $y$ моль сульфида цинка ($n(ZnS) = y$).
Выразим массы компонентов смеси через $x$ и $y$, используя их молярные массы:
$M(Zn) \approx 65 \text{ г/моль}$
$M(ZnS) = M(Zn) + M(S) \approx 65 + 32 = 97 \text{ г/моль}$
Масса цинка: $m(Zn) = n(Zn) \cdot M(Zn) = 65x$ г.
Масса сульфида цинка: $m(ZnS) = n(ZnS) \cdot M(ZnS) = 97y$ г.
Общая масса смеси равна 22,7 г, что позволяет составить первое уравнение системы:
$65x + 97y = 22,7$
Из уравнений реакций следует, что количество вещества выделившихся газов равно количеству вещества исходных реагентов в смеси:
$n(H_2) = n(Zn) = x \text{ моль}$
$n(H_2S) = n(ZnS) = y \text{ моль}$
Общее количество вещества газов равно сумме $n(H_2)$ и $n(H_2S)$, что дает нам второе уравнение системы:
$x + y = n(\text{газов}) = 0,3$
Теперь решим систему из двух линейных уравнений с двумя переменными:
$\begin{cases} 65x + 97y = 22,7 \\ x + y = 0,3 \end{cases}$
Из второго уравнения выразим $x$: $x = 0,3 - y$.
Подставим полученное выражение в первое уравнение:
$65(0,3 - y) + 97y = 22,7$
$19,5 - 65y + 97y = 22,7$
$32y = 22,7 - 19,5$
$32y = 3,2$
$y = \frac{3,2}{32} = 0,1$
Итак, количество вещества сульфида цинка $n(ZnS) = y = 0,1$ моль.
Найдем количество вещества цинка:
$x = 0,3 - y = 0,3 - 0,1 = 0,2$
Итак, количество вещества цинка $n(Zn) = x = 0,2$ моль.
Теперь мы можем найти массу цинка в смеси:
$m(Zn) = n(Zn) \cdot M(Zn) = 0,2 \text{ моль} \cdot 65 \text{ г/моль} = 13,0 \text{ г}$
Наконец, рассчитаем массовую долю ($\omega$) цинка в исходной смеси:
$\omega(Zn) = \frac{m(Zn)}{m(\text{смеси})} \cdot 100\% = \frac{13,0 \text{ г}}{22,7 \text{ г}} \cdot 100\% \approx 57,27\%$
Округляя до десятых, получаем $57,3\%$.
Ответ: массовая доля цинка в смеси составляет $57,3\%$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 140 расположенного на странице 29 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №140 (с. 29), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














