Номер 1480, страница 231 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 7. Металлы. Параграф 50. Важнейшие соединения железа. 1. *Соединения хрома в различных степенях окисления - номер 1480, страница 231.
№1480 (с. 231)
Условие. №1480 (с. 231)
скриншот условия

1480. *Феррохром — это сплав железа с хромом, который можно получить при восстановлении смеси, содержащей оксид хрома(III) и магнетит. Какую массу оксида хрома(III) следует добавить к 1,85 т железной руды, содержащей магнетит и 12,4 % пустой породы, чтобы при восстановлении получить феррохром с массовой долей хрома 34,4 %?
Решение. №1480 (с. 231)

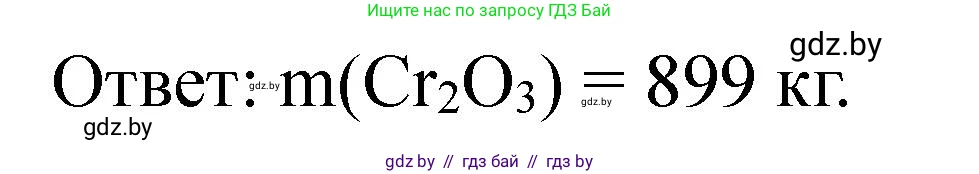
Решение 3. №1480 (с. 231)
Дано:
$m_{руды} = 1,85 \text{ т}$
$\omega_{п.п.} = 12,4 \% = 0,124$ (где п.п. - пустая порода)
$\omega(Cr)_{сплав} = 34,4 \% = 0,344$
Переведем массу руды в килограммы для удобства расчетов:
$m_{руды} = 1,85 \text{ т} = 1850 \text{ кг}$
Найти:
$m(Cr_2O_3) - ?$
Решение:
1. Найдем массу чистого магнетита ($Fe_3O_4$) в железной руде. Массовая доля магнетита составляет:
$\omega(Fe_3O_4) = 100\% - \omega_{п.п.} = 100\% - 12,4\% = 87,6\% = 0,876$
Масса магнетита в руде:
$m(Fe_3O_4) = m_{руды} \times \omega(Fe_3O_4) = 1850 \text{ кг} \times 0,876 = 1620,6 \text{ кг}$
2. Запишем уравнения восстановления металлов из их оксидов. В общем виде процессы можно представить так:
$Fe_3O_4 + \text{восстановитель} \rightarrow 3Fe$
$Cr_2O_3 + \text{восстановитель} \rightarrow 2Cr$
Для расчетов нам понадобятся молярные массы веществ (используем округленные значения атомных масс: $Ar(Fe)=56$, $Ar(Cr)=52$, $Ar(O)=16$):
$M(Fe_3O_4) = 3 \times 56 + 4 \times 16 = 168 + 64 = 232 \text{ г/моль}$
$M(Cr_2O_3) = 2 \times 52 + 3 \times 16 = 104 + 48 = 152 \text{ г/моль}$
$M(Fe) = 56 \text{ г/моль}$
$M(Cr) = 52 \text{ г/моль}$
3. Рассчитаем массу железа, которую можно получить из имеющегося количества магнетита.
Массу железа можно найти через соотношение масс в оксиде:
$m(Fe) = m(Fe_3O_4) \times \frac{3 \times M(Fe)}{M(Fe_3O_4)} = 1620,6 \text{ кг} \times \frac{3 \times 56}{232} = 1620,6 \text{ кг} \times \frac{168}{232} \approx 1173,54 \text{ кг}$
4. Полученный феррохром состоит из железа и хрома. Зная массовую долю хрома, найдем массу хрома в сплаве.
Массовая доля железа в сплаве:
$\omega(Fe)_{сплав} = 1 - \omega(Cr)_{сплав} = 1 - 0,344 = 0,656$
Массовая доля железа также определяется как отношение массы железа к общей массе сплава:
$\omega(Fe)_{сплав} = \frac{m(Fe)}{m(Fe) + m(Cr)}$
Подставим известные значения и найдем массу хрома $m(Cr)$:
$0,656 = \frac{1173,54 \text{ кг}}{1173,54 \text{ кг} + m(Cr)}$
$0,656 \times (1173,54 \text{ кг} + m(Cr)) = 1173,54 \text{ кг}$
$770,04 \text{ кг} + 0,656 \times m(Cr) = 1173,54 \text{ кг}$
$0,656 \times m(Cr) = 1173,54 \text{ кг} - 770,04 \text{ кг} = 403,5 \text{ кг}$
$m(Cr) = \frac{403,5 \text{ кг}}{0,656} \approx 615,09 \text{ кг}$
5. Теперь найдем массу оксида хрома(III), необходимую для получения такой массы хрома.
Используем соотношение масс в оксиде хрома(III):
$m(Cr_2O_3) = m(Cr) \times \frac{M(Cr_2O_3)}{2 \times M(Cr)} = 615,09 \text{ кг} \times \frac{152}{2 \times 52} = 615,09 \text{ кг} \times \frac{152}{104} \approx 898,96 \text{ кг}$
Округлим результат до трех значащих цифр, так как исходные данные приведены с такой же точностью.
$m(Cr_2O_3) \approx 899 \text{ кг}$
Ответ: для получения феррохрома заданного состава необходимо добавить 899 кг оксида хрома(III).
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 1480 расположенного на странице 231 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №1480 (с. 231), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














