Номер 193, страница 36 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 2. Строение атома и периодический закон. Параграф 7. Строение атома - номер 193, страница 36.
№193 (с. 36)
Условие. №193 (с. 36)
скриншот условия

193. Рассчитайте химическое количество $SO_4^{2-}$ анионов, содержащих столько же электронов, сколько все атомы в порции серы массой 100 г.
Решение. №193 (с. 36)
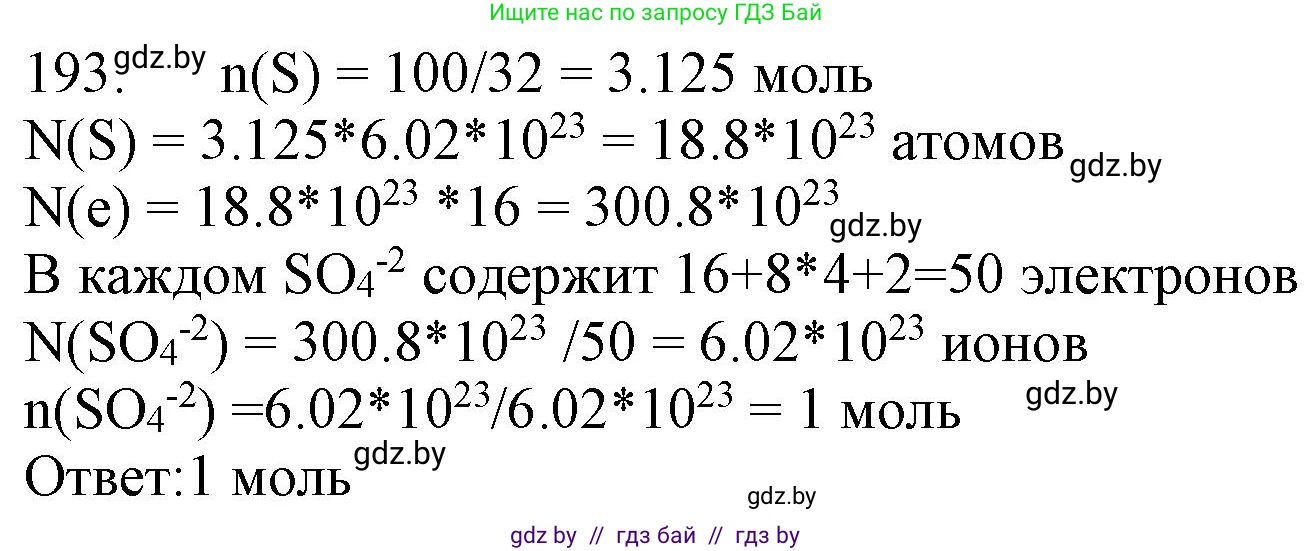
Решение 3. №193 (с. 36)
Дано:
Масса серы, $m(\text{S}) = 100 \text{ г}$
Найти:
Химическое количество сульфат-анионов, $n(\text{SO}_4^{2-})$ — ?
Решение:
1. Первым шагом определим химическое количество (число молей) атомов в порции серы. Для этого нам понадобится молярная масса серы, которую мы можем найти в периодической таблице химических элементов Д.И. Менделеева. Молярная масса серы $M(\text{S}) \approx 32 \text{ г/моль}$.
Химическое количество серы рассчитывается по формуле:
$n(\text{S}) = \frac{m(\text{S})}{M(\text{S})} = \frac{100 \text{ г}}{32 \text{ г/моль}} = 3.125 \text{ моль}$
2. Далее рассчитаем общее количество электронов в данном количестве серы. Порядковый номер серы (S) в периодической таблице равен 16, что означает, что в одном нейтральном атоме серы содержится 16 электронов. Следовательно, в 1 моль атомов серы содержится 16 моль электронов.
Найдем общее химическое количество электронов $n_e(\text{S})$ в порции серы:
$n_e(\text{S}) = n(\text{S}) \times Z(\text{S}) = 3.125 \text{ моль} \times 16 = 50 \text{ моль}$
3. Теперь определим, сколько электронов содержится в одном сульфат-анионе ($\text{SO}_4^{2-}$). Этот ион состоит из одного атома серы (S) и четырех атомов кислорода (O) и имеет заряд 2-, что указывает на наличие двух дополнительных электронов.
- Число электронов в атоме серы (порядковый номер $Z(\text{S})=16$): 16 электронов.
- Число электронов в атоме кислорода (порядковый номер $Z(\text{O})=8$): 8 электронов. В четырех атомах: $4 \times 8 = 32$ электрона.
- Дополнительные электроны из-за заряда 2-: 2 электрона.
Суммарное число электронов в одном сульфат-анионе:
$N_e(\text{SO}_4^{2-}) = 16 + 4 \times 8 + 2 = 16 + 32 + 2 = 50$ электронов.
Это означает, что в 1 моль сульфат-анионов содержится 50 моль электронов.
4. По условию задачи, искомое количество сульфат-анионов должно содержать столько же электронов, сколько и порция серы, то есть 50 моль электронов.
Обозначим искомое химическое количество сульфат-анионов как $n(\text{SO}_4^{2-})$. Тогда общее химическое количество электронов в них равно:
$n_e(\text{общ.}) = n(\text{SO}_4^{2-}) \times 50$
Приравниваем химические количества электронов:
$n_e(\text{общ.}) = n_e(\text{S})$
$n(\text{SO}_4^{2-}) \times 50 = 50 \text{ моль}$
Отсюда находим $n(\text{SO}_4^{2-})$:
$n(\text{SO}_4^{2-}) = \frac{50 \text{ моль}}{50} = 1 \text{ моль}$
Ответ: химическое количество сульфат-анионов составляет $1 \text{ моль}$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 193 расположенного на странице 36 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №193 (с. 36), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














