Номер 290, страница 48 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 2. Строение атома и периодический закон. Параграф 11. Периодичность изменения свойств атомов химических элементов и образуемых ими веществ - номер 290, страница 48.
№290 (с. 48)
Условие. №290 (с. 48)
скриншот условия

290. Рассчитайте массовую долю:
а) кислорода в высшем оксиде фосфора;
б) азота в его водородном соединении;
в) кислорода в высшем гидроксиде хлора.
Решение. №290 (с. 48)
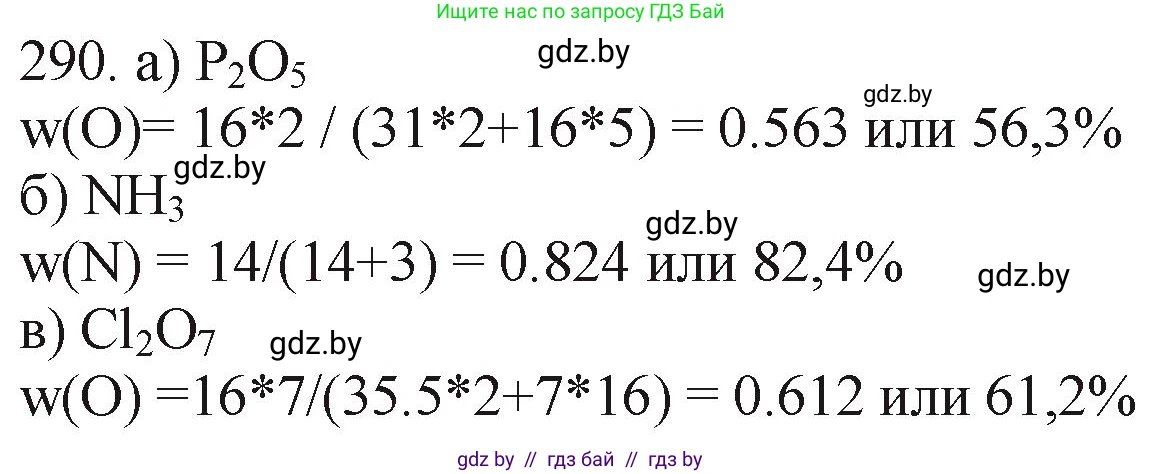
Решение 3. №290 (с. 48)
а) кислорода в высшем оксиде фосфора;
Дано:
Соединение: высший оксид фосфора.
Относительная атомная масса фосфора: $A_r(P) = 31$.
Относительная атомная масса кислорода: $A_r(O) = 16$.
Найти:
Массовую долю кислорода $\omega(O)$ - ?
Решение:
1. Определим химическую формулу высшего оксида фосфора. Фосфор (P) находится в 15-й группе (VА подгруппе) периодической таблицы химических элементов Д.И. Менделеева. Его высшая степень окисления равна +5. Степень окисления кислорода (O) в оксидах, как правило, равна -2. Для составления формулы найдем наименьшее общее кратное для степеней окисления: НОК(5, 2) = 10. Тогда индексы будут: для фосфора 10/5 = 2, для кислорода 10/2 = 5. Следовательно, формула высшего оксида фосфора — $P_2O_5$.
2. Рассчитаем относительную молекулярную массу $M_r$ оксида фосфора(V):
$M_r(P_2O_5) = 2 \cdot A_r(P) + 5 \cdot A_r(O) = 2 \cdot 31 + 5 \cdot 16 = 62 + 80 = 142$.
3. Массовая доля элемента в соединении вычисляется по формуле:
$\omega(Э) = \frac{n \cdot A_r(Э)}{M_r(\text{соединения})}$
где $n$ — количество атомов элемента в формуле, $A_r(Э)$ — относительная атомная масса элемента, $M_r(\text{соединения})$ — относительная молекулярная масса соединения.
В одной формульной единице $P_2O_5$ содержится 5 атомов кислорода. Рассчитаем массовую долю кислорода:
$\omega(O) = \frac{5 \cdot A_r(O)}{M_r(P_2O_5)} = \frac{5 \cdot 16}{142} = \frac{80}{142} \approx 0.5634$.
Чтобы выразить массовую долю в процентах, умножим полученное значение на 100%:
$0.5634 \cdot 100\% = 56.34\%$.
Ответ: массовая доля кислорода в высшем оксиде фосфора ($P_2O_5$) составляет 56.34%.
б) азота в его водородном соединении;
Дано:
Соединение: водородное соединение азота.
Относительная атомная масса азота: $A_r(N) = 14$.
Относительная атомная масса водорода: $A_r(H) = 1$.
Найти:
Массовую долю азота $\omega(N)$ - ?
Решение:
1. Определим химическую формулу водородного соединения азота. Азот (N) — элемент 15-й группы (VА подгруппы). В летучих водородных соединениях неметаллы обычно проявляют свою низшую степень окисления, которую можно рассчитать по формуле: (номер группы) - 8. Для азота это 5 - 8 = -3. Степень окисления водорода (H) в соединениях с неметаллами равна +1. Следовательно, формула водородного соединения азота (аммиака) — $NH_3$.
2. Рассчитаем относительную молекулярную массу $M_r$ аммиака:
$M_r(NH_3) = 1 \cdot A_r(N) + 3 \cdot A_r(H) = 1 \cdot 14 + 3 \cdot 1 = 14 + 3 = 17$.
3. Рассчитаем массовую долю азота в $NH_3$. В одной молекуле $NH_3$ содержится 1 атом азота.
$\omega(N) = \frac{1 \cdot A_r(N)}{M_r(NH_3)} = \frac{1 \cdot 14}{17} = \frac{14}{17} \approx 0.8235$.
В процентах:
$0.8235 \cdot 100\% = 82.35\%$.
Ответ: массовая доля азота в его водородном соединении ($NH_3$) составляет 82.35%.
в) кислорода в высшем гидроксиде хлора.
Дано:
Соединение: высший гидроксид хлора.
Относительная атомная масса хлора: $A_r(Cl) = 35.5$.
Относительная атомная масса кислорода: $A_r(O) = 16$.
Относительная атомная масса водорода: $A_r(H) = 1$.
Найти:
Массовую долю кислорода $\omega(O)$ - ?
Решение:
1. Определим химическую формулу высшего гидроксида хлора. Хлор (Cl) находится в 17-й группе (VIIА подгруппе), его высшая степень окисления равна +7. Высшему оксиду элемента соответствует его высший гидроксид (кислородсодержащая кислота). Высший оксид хлора — $Cl_2O_7$. Ему соответствует хлорная кислота, формула которой — $HClO_4$. Проверим степень окисления хлора в $HClO_4$: у водорода +1, у кислорода -2. Пусть степень окисления хлора равна $x$. Тогда: $(+1) + x + 4 \cdot (-2) = 0 \Rightarrow 1 + x - 8 = 0 \Rightarrow x = +7$. Формула определена верно.
2. Рассчитаем относительную молекулярную массу $M_r$ хлорной кислоты:
$M_r(HClO_4) = 1 \cdot A_r(H) + 1 \cdot A_r(Cl) + 4 \cdot A_r(O) = 1 \cdot 1 + 1 \cdot 35.5 + 4 \cdot 16 = 1 + 35.5 + 64 = 100.5$.
3. Рассчитаем массовую долю кислорода в $HClO_4$. В одной молекуле $HClO_4$ содержится 4 атома кислорода.
$\omega(O) = \frac{4 \cdot A_r(O)}{M_r(HClO_4)} = \frac{4 \cdot 16}{100.5} = \frac{64}{100.5} \approx 0.6368$.
В процентах:
$0.6368 \cdot 100\% = 63.68\%$.
Ответ: массовая доля кислорода в высшем гидроксиде хлора ($HClO_4$) составляет 63.68%.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 290 расположенного на странице 48 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №290 (с. 48), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














