Номер 516, страница 80 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 4. Химические реакции. Параграф 19. Тепловые эффекты химических реакций - номер 516, страница 80.
№516 (с. 80)
Условие. №516 (с. 80)
скриншот условия

516. При взаимодействии водорода объёмом (н. у.) 224 см3 с фтором массой 304 мг выделилось 4,32 кДж теплоты. Составьте термохимическое уравнение реакции водорода с фтором.
Решение. №516 (с. 80)
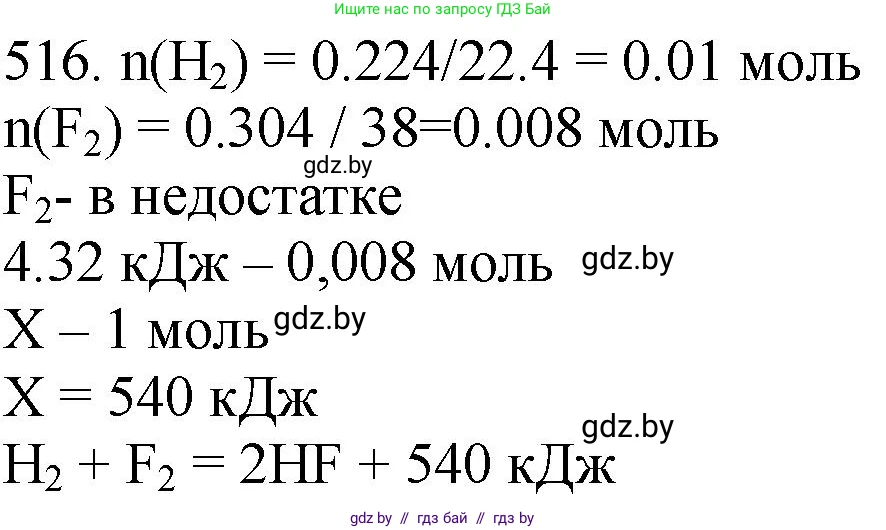
Решение 3. №516 (с. 80)
Дано:
$V(H_2) = 224 \text{ см}^3$ (н. у.)
$m(F_2) = 304 \text{ мг}$
$Q_{выд} = 4,32 \text{ кДж}$
$V(H_2) = 224 \text{ см}^3 = 0,224 \text{ л} = 0,000224 \text{ м}^3$
$m(F_2) = 304 \text{ мг} = 0,304 \text{ г} = 0,000304 \text{ кг}$
$Q_{выд} = 4,32 \text{ кДж} = 4320 \text{ Дж}$
Найти:
Термохимическое уравнение реакции.
Решение:
1. Сначала запишем уравнение реакции взаимодействия водорода и фтора. В результате реакции образуется фтороводород (HF):
$H_2(г) + F_2(г) = 2HF(г)$
2. Для составления термохимического уравнения необходимо рассчитать тепловой эффект реакции, отнесенный к молярным количествам веществ, указанным в уравнении. Для этого определим, какой из реагентов находится в недостатке (лимитирующий реагент), так как именно он определит количество выделившейся теплоты.
Найдем количество вещества водорода, используя молярный объем газов при нормальных условиях ($V_m = 22,4$ л/моль). Предварительно переведем объем водорода в литры: $V(H_2) = 224 \text{ см}^3 = 0,224 \text{ л}$.
$n(H_2) = \frac{V(H_2)}{V_m} = \frac{0,224 \text{ л}}{22,4 \text{ л/моль}} = 0,01 \text{ моль}$
Найдем количество вещества фтора, используя его молярную массу. Молярная масса фтора $M(F_2)$ равна $2 \times 19 = 38$ г/моль. Предварительно переведем массу фтора в граммы: $m(F_2) = 304 \text{ мг} = 0,304 \text{ г}$.
$n(F_2) = \frac{m(F_2)}{M(F_2)} = \frac{0,304 \text{ г}}{38 \text{ г/моль}} = 0,008 \text{ моль}$
3. Согласно уравнению реакции, водород и фтор реагируют в молярном соотношении $1:1$. У нас есть $0,01$ моль $H_2$ и $0,008$ моль $F_2$. Так как количество вещества фтора меньше, он является лимитирующим реагентом и прореагирует полностью. Водород взят в избытке. Дальнейшие расчеты ведем по фтору.
4. По условию задачи, при реакции $0,008$ моль фтора выделилось $4,32$ кДж теплоты. Рассчитаем тепловой эффект для реакции $1$ моль фтора, что соответствует стехиометрическому коэффициенту в уравнении. Составим пропорцию:
при реакции $0,008$ моль $F_2$ — выделилось $4,32$ кДж теплоты;
при реакции $1$ моль $F_2$ — выделится $Q$ кДж теплоты.
$Q = \frac{1 \text{ моль} \cdot 4,32 \text{ кДж}}{0,008 \text{ моль}} = 540 \text{ кДж}$
5. Таким образом, при взаимодействии 1 моль газообразного водорода с 1 моль газообразного фтора выделяется 540 кДж теплоты. Теперь мы можем записать термохимическое уравнение. Так как теплота выделяется (экзотермическая реакция), мы указываем ее со знаком плюс в правой части уравнения, либо как отрицательное значение энтальпии $\Delta H$.
Ответ: $H_2(г) + F_2(г) = 2HF(г) + 540 \text{ кДж}$ (или $H_2(г) + F_2(г) = 2HF(г); \Delta H = -540 \text{ кДж}$).
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 516 расположенного на странице 80 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №516 (с. 80), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














