Номер 602, страница 100 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 4. Химические реакции. Параграф 22. Химическое равновесие - номер 602, страница 100.
№602 (с. 100)
Условие. №602 (с. 100)
скриншот условия

602. *В системе установилось равновесие:
$2NO_{(г)} + O_{2(г)} \rightleftharpoons 2NO_{2(г)}$
Рассчитайте отношение величины скорости прямой реакции к величине скорости обратной реакции после увеличения концентрации оксида азота(II) в 3 раза и оксида азота(IV) в 2 раза.
Решение. №602 (с. 100)
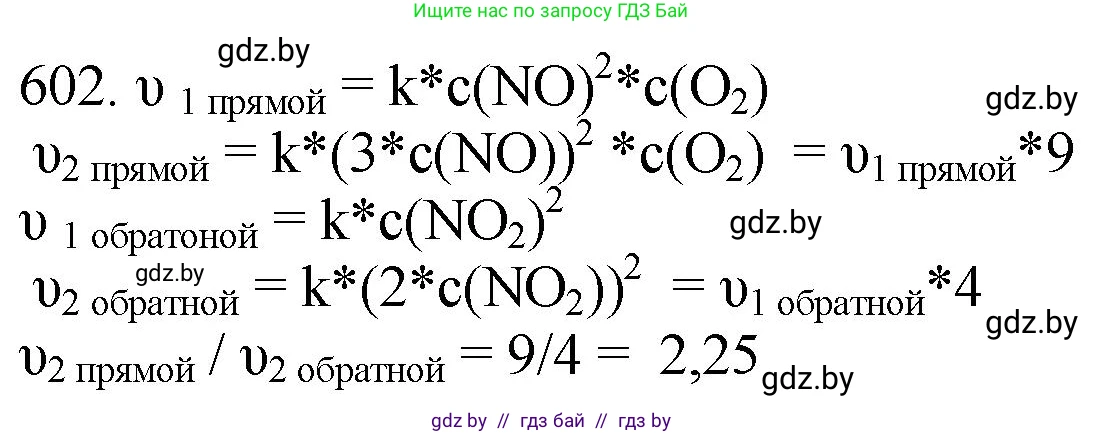
Решение 3. №602 (с. 100)
Дано:
Реакция в состоянии равновесия: $2NO_{(г)} + O_{2(г)} \rightleftharpoons 2NO_{2(г)}$
Начальное состояние (равновесие): $v_{1,равн} = v_{2,равн}$
Изменение концентрации оксида азота(II): $[NO]' = 3 \cdot [NO]_{равн}$
Изменение концентрации оксида азота(IV): $[NO_2]' = 2 \cdot [NO_2]_{равн}$
Концентрация кислорода не изменяется: $[O_2]' = [O_2]_{равн}$
Найти:
Отношение скорости прямой реакции к скорости обратной реакции после изменения концентраций: $\frac{v'_1}{v'_2}$
Решение:
Запишем выражения для скоростей прямой и обратной реакций, используя закон действующих масс. Для элементарных реакций (или если не указано иное) показатели степени в кинетическом уравнении равны стехиометрическим коэффициентам.
Скорость прямой реакции ($v_1$): $v_1 = k_1 \cdot [NO]^2 \cdot [O_2]$
Скорость обратной реакции ($v_2$): $v_2 = k_2 \cdot [NO_2]^2$
где $k_1$ и $k_2$ – константы скорости прямой и обратной реакций, а в квадратных скобках указаны молярные концентрации веществ.
В начальном состоянии система находится в равновесии, это означает, что скорости прямой и обратной реакций равны:
$v_{1,равн} = v_{2,равн}$
Следовательно:
$k_1 \cdot [NO]_{равн}^2 \cdot [O_2]_{равн} = k_2 \cdot [NO_2]_{равн}^2$
После увеличения концентрации оксида азота(II) в 3 раза и оксида азота(IV) в 2 раза, система выходит из состояния равновесия. Рассчитаем новые скорости прямой ($v'_1$) и обратной ($v'_2$) реакций при новых концентрациях:
Новая скорость прямой реакции:
$v'_1 = k_1 \cdot ([NO]')^2 \cdot [O_2]' = k_1 \cdot (3 \cdot [NO]_{равн})^2 \cdot [O_2]_{равн} = 9 \cdot (k_1 \cdot [NO]_{равн}^2 \cdot [O_2]_{равн})$
Так как выражение в скобках равно начальной скорости прямой реакции $v_{1,равн}$, то:
$v'_1 = 9 \cdot v_{1,равн}$
Новая скорость обратной реакции:
$v'_2 = k_2 \cdot ([NO_2]')^2 = k_2 \cdot (2 \cdot [NO_2]_{равн})^2 = 4 \cdot (k_2 \cdot [NO_2]_{равн}^2)$
Так как выражение в скобках равно начальной скорости обратной реакции $v_{2,равн}$, то:
$v'_2 = 4 \cdot v_{2,равн}$
Теперь найдем отношение новой скорости прямой реакции к новой скорости обратной реакции:
$\frac{v'_1}{v'_2} = \frac{9 \cdot v_{1,равн}}{4 \cdot v_{2,равн}}$
Поскольку в начальном состоянии равновесия $v_{1,равн} = v_{2,равн}$, мы можем сократить эти величины в числителе и знаменателе:
$\frac{v'_1}{v'_2} = \frac{9}{4} = 2.25$
Таким образом, после изменения концентраций скорость прямой реакции станет в 2,25 раза больше скорости обратной реакции.
Ответ: отношение величины скорости прямой реакции к величине скорости обратной реакции равно 2,25.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 602 расположенного на странице 100 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №602 (с. 100), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














