Номер 502, страница 76 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 4. Химические реакции. Параграф 18. Классификация и общие характеристики химических реакций - номер 502, страница 76.
№502 (с. 76)
Условие. №502 (с. 76)
скриншот условия

502*. Какую максимальную массу этана можно окислить смесью озона и кислорода объёмом (н. у.) $14,3 \text{ дм}^3$, в которой массовая доля кислорода больше массовой доли озона в 7 раз?
Решение. №502 (с. 76)
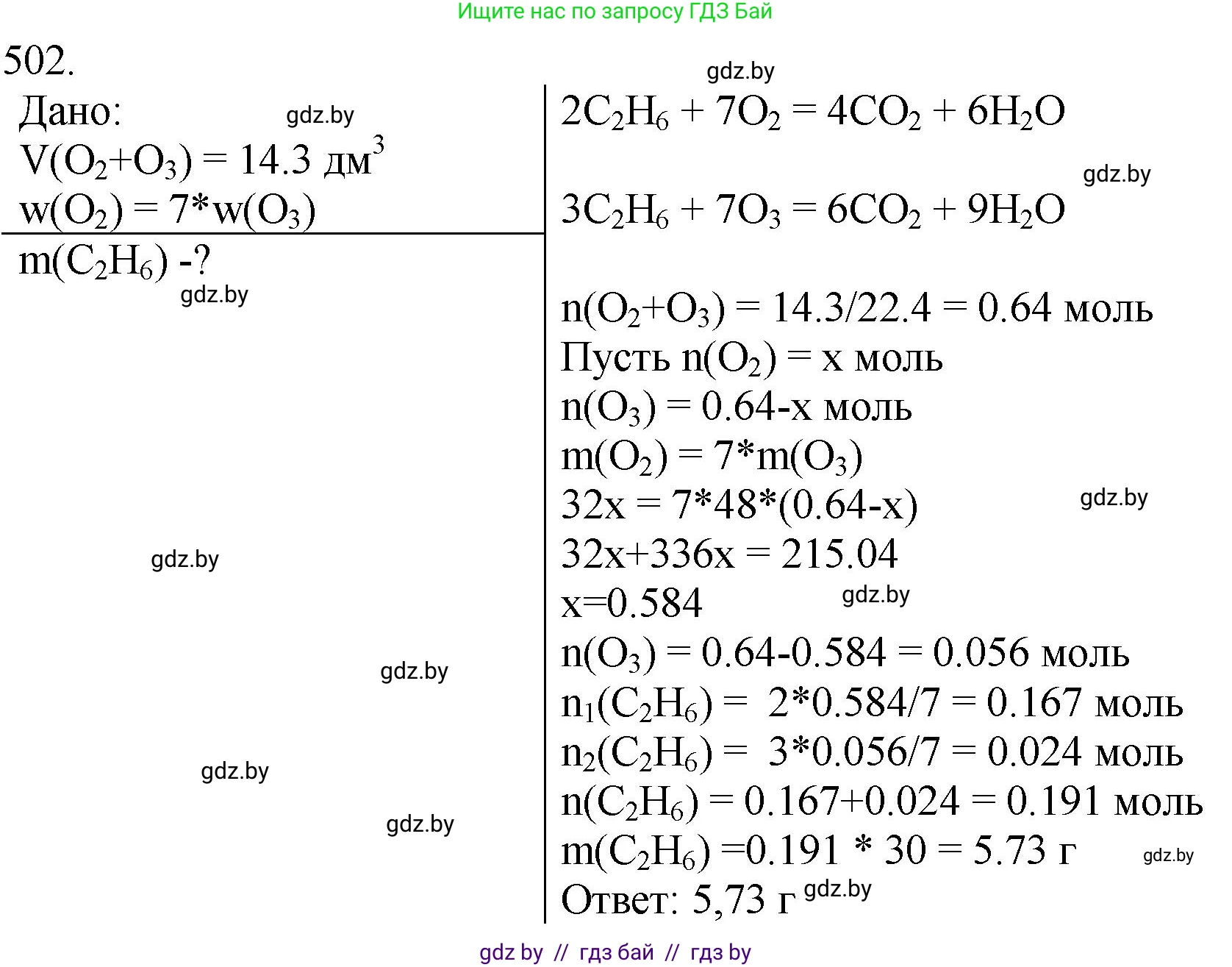
Решение 3. №502 (с. 76)
Дано:
Объем смеси озона и кислорода $V(\text{смеси } O_2, O_3) = 14,3 \text{ дм}^3$ (н. у.)
Массовая доля кислорода в 7 раз больше массовой доли озона $\omega(O_2) = 7 \cdot \omega(O_3)$
Молярный объем газа при нормальных условиях $V_m = 22,4 \text{ дм}^3/\text{моль}$
Найти:
Максимальную массу этана $m(C_2H_6)$ , которую можно окислить.
Решение:
Запишем уравнения реакций полного окисления этана ($C_2H_6$) кислородом ($O_2$) и озоном ($O_3$):
$2C_2H_6 + 7O_2 \rightarrow 4CO_2 + 6H_2O$
$C_2H_6 + \frac{7}{3}O_3 \rightarrow 2CO_2 + 3H_2O \quad$ (или $3C_2H_6 + 7O_3 \rightarrow 6CO_2 + 9H_2O$)
Найдем общее количество вещества (моль) в газовой смеси:
$n(\text{смеси}) = \frac{V(\text{смеси})}{V_m} = \frac{14,3 \text{ дм}^3}{22,4 \text{ дм}^3/\text{моль}} \approx 0,6384 \text{ моль}$
Определим мольный состав смеси. Пусть $n(O_2)$ и $n(O_3)$ — количества вещества кислорода и озона соответственно.
Соотношение массовых долей $\omega(O_2) = 7 \cdot \omega(O_3)$ означает, что масса кислорода в 7 раз больше массы озона: $m(O_2) = 7 \cdot m(O_3)$.
Выразим массы через количество вещества и молярную массу ($M(O_2) = 32 \text{ г/моль}$, $M(O_3) = 48 \text{ г/моль}$):
$n(O_2) \cdot M(O_2) = 7 \cdot n(O_3) \cdot M(O_3)$
$n(O_2) \cdot 32 = 7 \cdot n(O_3) \cdot 48$
$32 \cdot n(O_2) = 336 \cdot n(O_3)$
$n(O_2) = \frac{336}{32} \cdot n(O_3) = 10,5 \cdot n(O_3)$
Составим систему уравнений и найдем $n(O_2)$ и $n(O_3)$:
$\begin{cases} n(O_2) + n(O_3) = n(\text{смеси}) \approx 0,6384 \text{ моль} \\ n(O_2) = 10,5 \cdot n(O_3) \end{cases}$
Подставим второе уравнение в первое:
$10,5 \cdot n(O_3) + n(O_3) = 0,6384$
$11,5 \cdot n(O_3) = 0,6384$
$n(O_3) = \frac{0,6384}{11,5} \approx 0,0555 \text{ моль}$
$n(O_2) = 10,5 \cdot 0,0555 \approx 0,5829 \text{ моль}$
Рассчитаем максимальное количество вещества этана, которое может быть окислено всей смесью. Для полного окисления 1 моль этана требуется 7 моль атомарного кислорода ($O$).
Общее количество вещества атомарного кислорода в смеси:
$n(O)_{\text{общ}} = 2 \cdot n(O_2) + 3 \cdot n(O_3) = 2 \cdot 0,5829 + 3 \cdot 0,0555 = 1,1658 + 0,1665 = 1,3323 \text{ моль}$
Количество вещества этана:
$n(C_2H_6) = \frac{n(O)_{\text{общ}}}{7} = \frac{1,3323 \text{ моль}}{7} \approx 0,1903 \text{ моль}$
Найдем максимальную массу этана. Молярная масса этана $M(C_2H_6) = 2 \cdot 12 + 6 \cdot 1 = 30 \text{ г/моль}$.
$m(C_2H_6) = n(C_2H_6) \cdot M(C_2H_6) = 0,1903 \text{ моль} \cdot 30 \text{ г/моль} \approx 5,709 \text{ г}$
С учетом точности исходных данных (3 значащие цифры), округляем результат.
Ответ: максимальная масса этана, которую можно окислить данной смесью, составляет 5,71 г.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 502 расположенного на странице 76 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №502 (с. 76), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














