Номер 658, страница 111 - гдз по химии 11 класс сборник задач Хвалюк, Резяпкин

Авторы: Хвалюк В. Н., Резяпкин В. И.
Тип: Сборник задач
Издательство: Адукацыя i выхаванне
Год издания: 2023 - 2025
Цвет обложки: зелёный, голубой с колбами
ISBN: 978-985-599-534-1
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава 5. Химия растворов. Параграф 25. Электролитическая диссоциация веществ в растворах - номер 658, страница 111.
№658 (с. 111)
Условие. №658 (с. 111)
скриншот условия

658. Укажите верные утверждения:
а) все жидкие при н. у. вещества являются электролитами;
б) к электролитам относятся только вещества, которые в чистом виде при н. у. проводят электрический ток;
в) все соли являются электролитами;
г) при прохождении электрического тока через водный раствор электролита электрический заряд переносят ионы;
д) в водном растворе любого электролита заряд в основном переносят ионы $H^+$ и $OH^-$;
е) электролитом может быть вещество любого класса неорганических соединений — оксид, кислота, основание и соль;
ж) все неорганические кислоты являются сильными электролитами, а органические — слабыми;
з) по составу ионы бывают простые и сложные;
и) при протекании тока через раствор электролита анионы движутся к катоду, который имеет положительный заряд;
к) водные растворы органических кислот совершенно не проводят электрический ток.
Решение. №658 (с. 111)
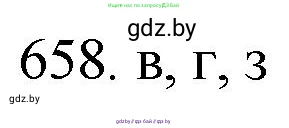
Решение 3. №658 (с. 111)
а) все жидкие при н. у. вещества являются электролитами;
Утверждение неверно. Электролиты — это вещества, растворы или расплавы которых проводят электрический ток за счёт диссоциации на ионы. Многие вещества, жидкие при нормальных условиях, не являются электролитами. Например, чистая (дистиллированная) вода является очень слабым электролитом, а многие органические жидкости (бензол, спирты в чистом виде, масла) являются диэлектриками. Металл ртуть, хотя и жидкий, проводит ток за счёт электронов (проводник первого рода), а не ионов.
Ответ: Неверно.
б) к электролитам относятся только вещества, которые в чистом виде при н. у. проводят электрический ток;
Утверждение неверно. Вещества, проводящие ток в чистом виде при н. у. — это, как правило, металлы (проводники первого рода). Электролиты же проводят ток в растворах или расплавах. Большинство электролитов, например, поваренная соль $NaCl$ или гидроксид натрия $NaOH$, в чистом виде при н. у. являются твёрдыми кристаллическими веществами и не проводят электрический ток.
Ответ: Неверно.
в) все соли являются электролитами;
Утверждение верно. Соли по своей природе являются ионными соединениями. При плавлении или растворении в полярном растворителе (например, в воде) их кристаллическая решётка разрушается, и они диссоциируют на свободные ионы, которые способны переносить электрический заряд. Даже практически нерастворимые в воде соли (например, $AgCl$, $BaSO_4$) считаются сильными электролитами, так как та небольшая их часть, которая переходит в раствор, полностью диссоциирует на ионы.
Ответ: Верно.
г) при прохождении электрического тока через водный раствор электролита электрический заряд переносят ионы;
Утверждение верно. Это фундаментальный принцип электропроводности растворов и расплавов. Электрический ток в них представляет собой упорядоченное движение заряженных частиц — ионов. Положительно заряженные ионы (катионы) движутся к отрицательному электроду (катоду), а отрицательно заряженные ионы (анионы) — к положительному электроду (аноду).
Ответ: Верно.
д) в водном растворе любого электролита заряд в основном переносят ионы H+ и OH-;
Утверждение неверно. Основными переносчиками заряда в водном растворе электролита являются ионы, образовавшиеся при диссоциации самого растворённого вещества. Например, в растворе хлорида калия $KCl$ ток переносят ионы $K^+$ и $Cl^-$. Ионы $H^+$ и $OH^-$ образуются при автодиссоциации воды ($H_2O \rightleftharpoons H^+ + OH^-$), но их концентрация в нейтральных растворах очень мала (по $10^{-7}$ моль/л) и становится значимой только в растворах сильных кислот или щелочей, но и в этих случаях ионы самого электролита вносят основной вклад в перенос заряда.
Ответ: Неверно.
е) электролитом может быть вещество любого класса неорганических соединений — оксид, кислота, основание и соль;
Утверждение верно. Формулировка "может быть" указывает на принципиальную возможность.
- Кислоты (например, $H_2SO_4$), основания (например, $KOH$) и соли (например, $NaNO_3$) являются классическими примерами электролитов.
- Оксиды: некоторые ионные оксиды (например, $Al_2O_3$, $CaO$) в расплавленном состоянии проводят электрический ток, то есть являются электролитами. Кроме того, многие оксиды (кислотные и основные) реагируют с водой, образуя кислоты и основания, которые являются электролитами.
Таким образом, представители всех перечисленных классов могут быть электролитами.
Ответ: Верно.
ж) все неорганические кислоты являются сильными электролитами, а органические — слабыми;
Утверждение неверно. Это чрезмерное обобщение. Среди неорганических кислот есть как сильные ($HCl$, $HNO_3$), так и многочисленные слабые ($H_2CO_3$, $H_3PO_4$, $HF$, $H_2S$). Аналогично, хотя большинство органических кислот являются слабыми (например, уксусная $CH_3COOH$), существуют и сильные органические кислоты (например, трихлоруксусная $CCl_3COOH$).
Ответ: Неверно.
з) по составу ионы бывают простые и сложные;
Утверждение верно. Это одна из основных классификаций ионов.
- Простые ионы состоят из одного атома ($Na^+$, $Cl^-$, $Ca^{2+}$).
- Сложные (или полиатомные) ионы состоят из группы ковалентно связанных атомов, имеющих общий заряд ($SO_4^{2-}$, $NH_4^+$, $OH^-$).
Ответ: Верно.
и) при протекании тока через раствор электролита анионы движутся к катоду, который имеет положительный заряд;
Утверждение неверно и содержит две ошибки. В процессе электролиза:
- Анионы — это отрицательно заряженные ионы, поэтому они движутся к положительно заряженному электроду — аноду.
- Катод — это отрицательно заряженный электрод, к которому движутся положительно заряженные ионы — катионы.
Ответ: Неверно.
к) водные растворы органических кислот совершенно не проводят электрический ток.
Утверждение неверно. Органические кислоты — типичные слабые электролиты. Они диссоциируют в воде обратимо и не полностью, но всё же образуют ионы. Например, уксусная кислота: $CH_3COOH \rightleftharpoons CH_3COO^- + H^+$. Наличие даже небольшой концентрации ионов делает раствор проводником электрического тока, хотя и слабым. Совершенно не проводят ток только неэлектролиты.
Ответ: Неверно.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 658 расположенного на странице 111 к сборнику задач 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №658 (с. 111), авторов: Хвалюк (Виктор Николаевич), Резяпкин (Виктор Ильич), учебного пособия издательства Адукацыя i выхаванне.














