Номер 7, страница 136 - гдз по химии 11 класс учебник Мычко, Прохоревич

Авторы: Мычко Д. И., Прохоревич К. Н., Борушко И. И.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2021 - 2025
Цвет обложки: зелёный с колбами
ISBN: 978-985-599-297-5
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 11 классе
Глава V. Химия растворов. Параграф 24. Приготовление растворов - номер 7, страница 136.
№7 (с. 136)
Условия. №7 (с. 136)
скриншот условия

7. В воде массой 50 г растворили серную кислоту массой 50 г. Рассчитайте массовую долю и молярную концентрацию кислоты в растворе, если его плотность равна $1,395 \text{ г/см}^3$.
Решение. №7 (с. 136)
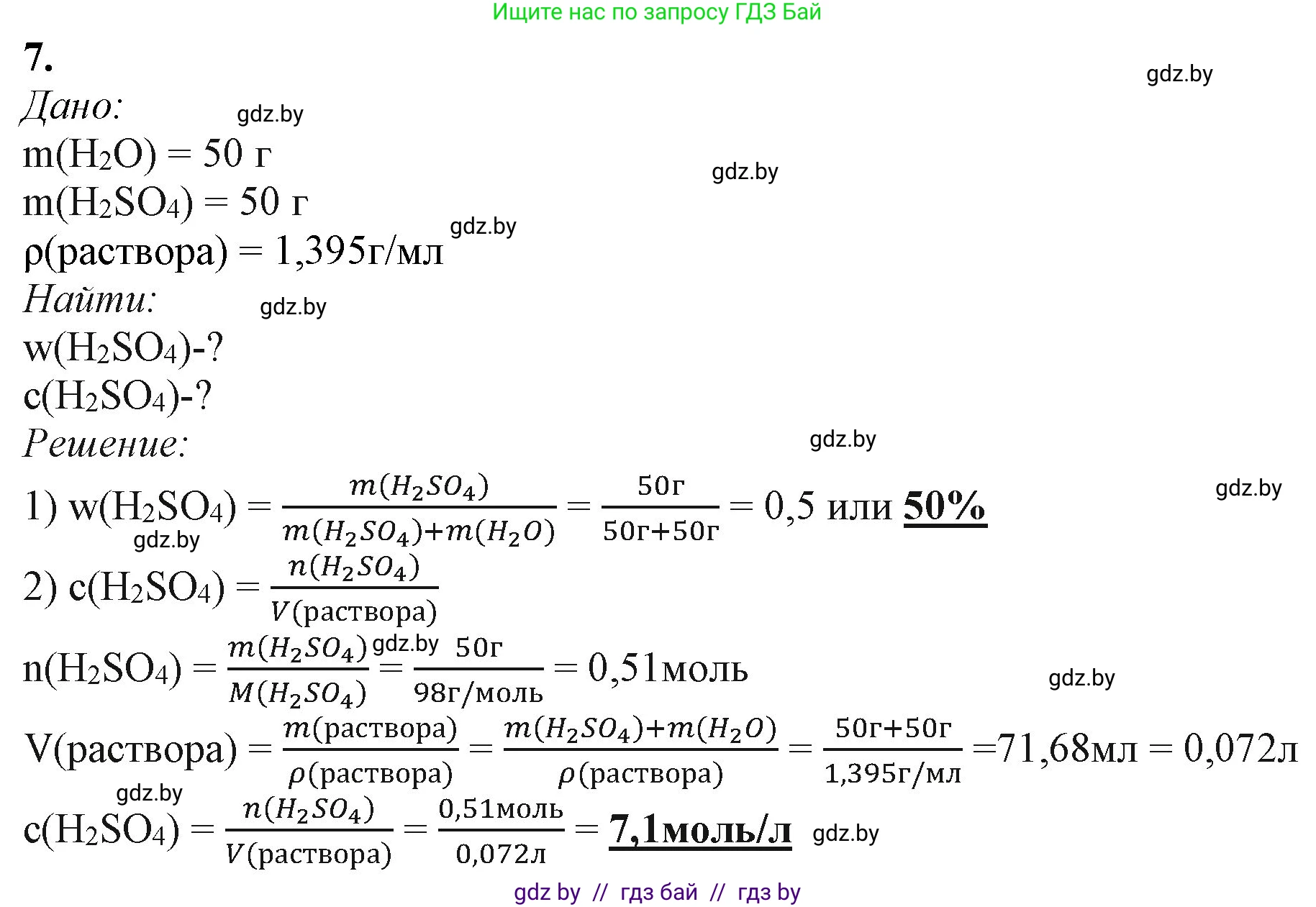
Решение 2. №7 (с. 136)
Дано:
$m(H_2O) = 50 \text{ г}$
$m(H_2SO_4) = 50 \text{ г}$
$\rho_{р-ра} = 1,395 \text{ г/см}^3$
Перевод в систему СИ:
$m(H_2O) = 0,05 \text{ кг}$
$m(H_2SO_4) = 0,05 \text{ кг}$
$\rho_{р-ра} = 1,395 \text{ г/см}^3 = 1395 \text{ кг/м}^3$
Найти:
$\omega(H_2SO_4) - ?$
$C_M(H_2SO_4) - ?$
Решение:
Расчет массовой доли кислоты ($\omega$)
1. Найдем общую массу раствора ($m_{р-ра}$), которая равна сумме масс растворителя (воды) и растворенного вещества (серной кислоты).
$m_{р-ра} = m(H_2O) + m(H_2SO_4) = 50 \text{ г} + 50 \text{ г} = 100 \text{ г}$
2. Массовая доля растворенного вещества вычисляется по формуле:
$\omega(\text{вещества}) = \frac{m(\text{вещества})}{m(\text{раствора})}$
3. Подставим значения для серной кислоты:
$\omega(H_2SO_4) = \frac{50 \text{ г}}{100 \text{ г}} = 0,5$
Массовую долю также можно выразить в процентах, умножив на 100%:
$0,5 \times 100\% = 50\%$
Ответ: Массовая доля серной кислоты в растворе составляет 0,5 или 50%.
Расчет молярной концентрации ($C_M$)
1. Молярная концентрация определяется по формуле:
$C_M = \frac{n(\text{вещества})}{V(\text{раствора})}$
где $n$ - количество вещества в молях, а $V$ - объем раствора в литрах.
2. Сначала рассчитаем количество вещества серной кислоты ($n(H_2SO_4)$). Для этого нам понадобится молярная масса серной кислоты ($M(H_2SO_4)$).
$M(H_2SO_4) = 2 \times M(H) + M(S) + 4 \times M(O) = 2 \times 1 + 32 + 4 \times 16 = 98 \text{ г/моль}$
Теперь найдем количество вещества:
$n(H_2SO_4) = \frac{m(H_2SO_4)}{M(H_2SO_4)} = \frac{50 \text{ г}}{98 \text{ г/моль}} \approx 0,5102 \text{ моль}$
3. Далее найдем объем раствора ($V_{р-ра}$), используя его массу ($m_{р-ра} = 100 \text{ г}$) и плотность ($\rho_{р-ра} = 1,395 \text{ г/см}^3$):
$V_{р-ра} = \frac{m_{р-ра}}{\rho_{р-ра}} = \frac{100 \text{ г}}{1,395 \text{ г/см}^3} \approx 71,685 \text{ см}^3$
4. Переведем объем из см³ в литры (1 л = 1000 см³):
$V_{р-ра} = 71,685 \text{ см}^3 = 0,071685 \text{ л}$
5. Теперь можем рассчитать молярную концентрацию:
$C_M(H_2SO_4) = \frac{n(H_2SO_4)}{V_{р-ра}} = \frac{0,5102 \text{ моль}}{0,071685 \text{ л}} \approx 7,117 \text{ моль/л}$
Округлим результат до сотых.
Ответ: Молярная концентрация серной кислоты в растворе равна примерно 7,12 моль/л.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 11 класс, для упражнения номер 7 расположенного на странице 136 к учебнику 2021 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №7 (с. 136), авторов: Мычко (Дмитрий Иванович), Прохоревич (Константин Николаевич), Борушко (Ирина Ивановна), учебного пособия издательства Адукацыя i выхаванне.













