Номер 612, страница 137 - гдз по химии 10 класс сборник задач Матулис, Матулис

Авторы: Матулис В. Э., Матулис В. Э., Колевич Т. А.
Тип: Сборник задач
Издательство: Национальный институт образования
Год издания: 2021 - 2025
Уровень обучения: базовый и повышенный
Цвет обложки: синий
ISBN: 978-985-594-959-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 10 классе
Глава 3. Кислородсодержащие органические соединения. 3.4. Карбоновые кислоты - номер 612, страница 137.
№612 (с. 137)
Условие. №612 (с. 137)
скриншот условия
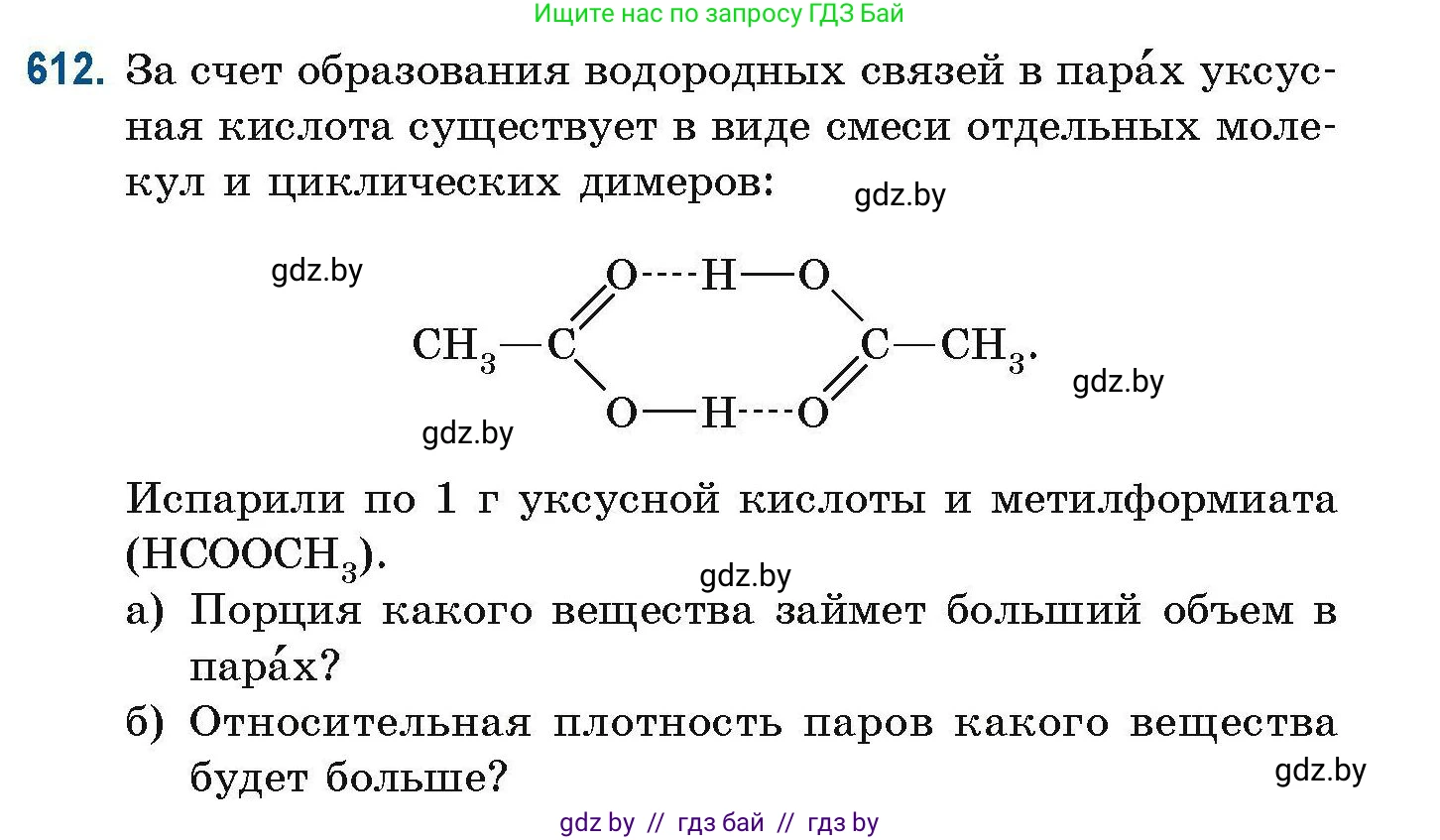
612. За счет образования водородных связей в парах уксусная кислота существует в виде смеси отдельных молекул и циклических димеров:
$\begin{array}{c}\quad \quad \text{O}\text{...}\text{H}\text{-}\text{O} \\\quad \quad \Vert \quad \quad \quad \Vert \\\text{CH}_3\text{-}\text{C} \quad \quad \quad \text{C}\text{-}\text{CH}_3 \\\quad \quad \text{O}\text{-}\text{H}\text{...}\text{O}\end{array}$
Испарили по 1 г уксусной кислоты и метилформиата (H$COOCH_3$).
а) Порция какого вещества займет больший объем в парах?
б) Относительная плотность паров какого вещества будет больше?
Решение. №612 (с. 137)

Решение 2. №612 (с. 137)
Дано:
$m(\text{CH}_3\text{COOH}) = 1 \text{ г}$
$m(\text{HCOOCH}_3) = 1 \text{ г}$
Найти:
a) $V_{больший} - ?$
b) $D_{большая} - ?$
Решение:
Сначала определим молярные массы уксусной кислоты ($CH_3COOH$) и метилформиата ($HCOOCH_3$). Оба вещества имеют одинаковую химическую формулу $C_2H_4O_2$, то есть являются изомерами.
Молярная масса $M(C_2H_4O_2) = 2 \cdot A_r(C) + 4 \cdot A_r(H) + 2 \cdot A_r(O) = 2 \cdot 12 + 4 \cdot 1 + 2 \cdot 16 = 24 + 4 + 32 = 60 \text{ г/моль}$.
Таким образом, молярные массы мономерных молекул обоих веществ одинаковы: $M(\text{CH}_3\text{COOH}) = M(\text{HCOOCH}_3) = 60 \text{ г/моль}$.
а) Порция какого вещества займет больший объем в пара́х?
Согласно закону Авогадро, при одинаковых условиях (температуре и давлении) равные количества вещества (в молях) любого газа занимают одинаковый объем. Следовательно, больший объем займет то вещество, у которого количество моль газообразных частиц больше.
Найдем количество вещества для каждого соединения.
Для метилформиата, который не образует водородных связей и в парах существует в виде отдельных молекул, количество вещества равно:
$\nu(\text{HCOOCH}_3) = \frac{m(\text{HCOOCH}_3)}{M(\text{HCOOCH}_3)} = \frac{1 \text{ г}}{60 \text{ г/моль}} \approx 0,0167 \text{ моль}$.
Уксусная кислота в парах существует в виде равновесной смеси отдельных молекул (мономеров) и циклических димеров:
$2\text{CH}_3\text{COOH} \rightleftharpoons (\text{CH}_3\text{COOH})_2$
Образование димеров приводит к уменьшению общего числа частиц в газовой фазе. Например, из двух мономерных молекул образуется одна димерная частица. Поэтому общее количество моль частиц в парах уксусной кислоты будет меньше, чем количество моль, рассчитанное по массе и молярной массе мономера.
$\nu_{общ}(\text{CH}_3\text{COOH}) < \frac{m(\text{CH}_3\text{COOH})}{M(\text{CH}_3\text{COOH})} = \frac{1 \text{ г}}{60 \text{ г/моль}}$.
Сравнивая количество моль частиц: $\nu(\text{HCOOCH}_3) > \nu_{общ}(\text{CH}_3\text{COOH})$.
Поскольку объем газа прямо пропорционален количеству моль частиц ($V \propto \nu$), то объем, занимаемый парами метилформиата, будет больше, чем объем, занимаемый парами уксусной кислоты.
Ответ: больший объем в парах займет порция метилформиата.
б) Относительная плотность паров какого вещества будет больше?
Относительная плотность газа по другому газу (например, по воздуху или водороду) прямо пропорциональна молярной массе этого газа ($D = M/M_{справ}$). Таким образом, чтобы сравнить относительные плотности паров, нужно сравнить их эффективные (средние) молярные массы в газовой фазе.
Эффективная молярная масса определяется как отношение общей массы газа к общему количеству моль частиц в нем: $M_{эфф} = \frac{m_{общ}}{\nu_{общ}}$.
Для метилформиата, состоящего только из мономерных молекул, эффективная молярная масса равна его молярной массе:
$M_{эфф}(\text{HCOOCH}_3) = M(\text{HCOOCH}_3) = 60 \text{ г/моль}$.
Для уксусной кислоты пар представляет собой смесь мономеров ($M = 60 \text{ г/моль}$) и димеров ($M = 120 \text{ г/моль}$). Наличие более тяжелых димерных частиц в смеси приводит к тому, что средняя (эффективная) молярная масса паров уксусной кислоты будет больше молярной массы ее мономера.
$M_{эфф}(\text{CH}_3\text{COOH}) > 60 \text{ г/моль}$.
Сравнивая эффективные молярные массы:
$M_{эфф}(\text{CH}_3\text{COOH}) > M_{эфф}(\text{HCOOCH}_3)$.
Следовательно, относительная плотность паров уксусной кислоты будет больше, чем у метилформиата.
Ответ: относительная плотность паров уксусной кислоты будет больше.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10 класс, для упражнения номер 612 расположенного на странице 137 к сборнику задач 2021 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №612 (с. 137), авторов: Матулис (Вадим Эдвардович), Матулис (Виталий Эдвардович), Колевич (Татьяна Александровна), базовый и повышенный уровень обучения учебного пособия издательства Национальный институт образования.














