Номер 613, страница 137 - гдз по химии 10 класс сборник задач Матулис, Матулис

Авторы: Матулис В. Э., Матулис В. Э., Колевич Т. А.
Тип: Сборник задач
Издательство: Национальный институт образования
Год издания: 2021 - 2025
Уровень обучения: базовый и повышенный
Цвет обложки: синий
ISBN: 978-985-594-959-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 10 классе
Глава 3. Кислородсодержащие органические соединения. 3.4. Карбоновые кислоты - номер 613, страница 137.
№613 (с. 137)
Условие. №613 (с. 137)
скриншот условия

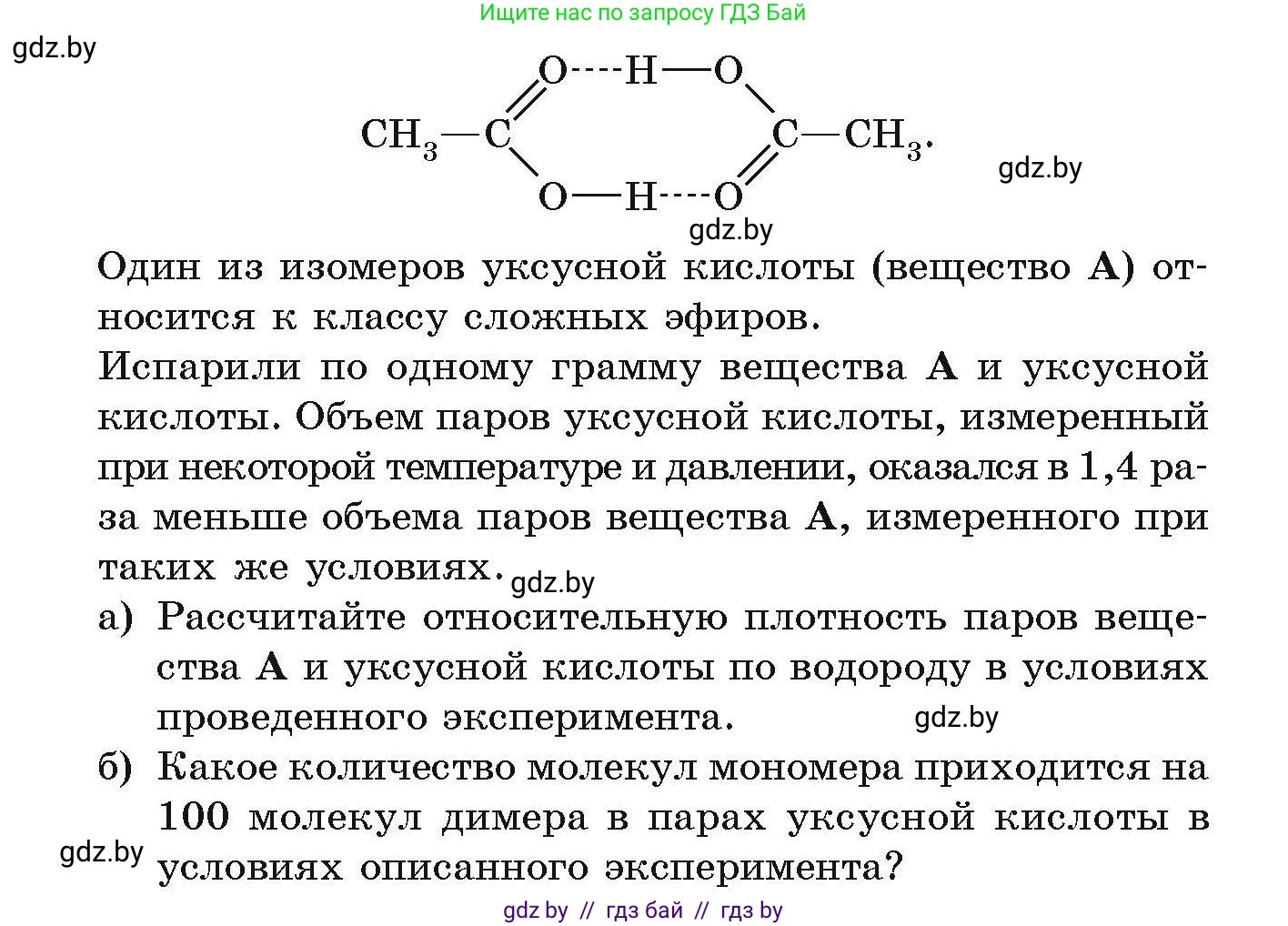
613. За счет образования водородных связей в парах уксусная кислота существует в виде смеси отдельных молекул и циклических димеров:
$$ \begin{array}{ccc} & \text{O---H} & \\ \text{CH}_3-\text{C} & & \text{C}-\text{CH}_3 \\ \Vert & & \Vert \\ \text{O} & & \text{O} \\ & \text{O---H} & \end{array} $$
Один из изомеров уксусной кислоты (вещество А) относится к классу сложных эфиров. Испарили по одному грамму вещества А и уксусной кислоты. Объем паров уксусной кислоты, измеренный при некоторой температуре и давлении, оказался в 1,4 раза меньше объема паров вещества А, измеренного при таких же условиях.
a) Рассчитайте относительную плотность паров вещества А и уксусной кислоты по водороду в условиях проведенного эксперимента.
б) Какое количество молекул мономера приходится на 100 молекул димера в парах уксусной кислоты в условиях описанного эксперимента?
Решение. №613 (с. 137)

Решение 2. №613 (с. 137)
Дано:
$m(A) = 1$ г
$m(УК) = 1$ г
$\frac{V(A)}{V(УК)} = 1.4$
$P, T = const$
Вещество A - изомер уксусной кислоты ($CH_3COOH$), относящийся к классу сложных эфиров.
$m(A) = 0.001$ кг
$m(УК) = 0.001$ кг
Найти:
а) $D_{H_2}(A)$, $D_{H_2}(УК)$ - ?
б) Количество молекул мономера на 100 молекул димера в парах уксусной кислоты - ?
Решение:
а) Рассчитайте относительную плотность паров вещества А и уксусной кислоты по водороду в условиях проведенного эксперимента.
1. Определим вещество А. Формула уксусной кислоты - $CH_3COOH$. Её молекулярная формула - $C_2H_4O_2$. Вещество А является изомером уксусной кислоты и относится к классу сложных эфиров. Единственный сложный эфир с такой молекулярной формулой - это метилформиат ($HCOOCH_3$).
2. Рассчитаем молярную массу вещества А (метилформиата) и мономера уксусной кислоты. Поскольку они являются изомерами, их молярные массы равны.
$M(A) = M(CH_3COOH_{мономер}) = M(C_2H_4O_2) = 2 \cdot Ar(C) + 4 \cdot Ar(H) + 2 \cdot Ar(O) = 2 \cdot 12 + 4 \cdot 1 + 2 \cdot 16 = 60$ г/моль.
3. В парах вещество А (метилформиат) не образует водородных связей и существует в виде отдельных молекул. Поэтому молярная масса его паров равна молярной массе молекулы.
$M(паров\;A) = 60$ г/моль.
4. Рассчитаем относительную плотность паров вещества А по водороду ($D_{H_2}$).
$D_{H_2}(A) = \frac{M(A)}{M(H_2)} = \frac{60}{2} = 30$.
5. Пары уксусной кислоты (УК) представляют собой смесь мономеров и димеров. Найдем среднюю молярную массу паров уксусной кислоты ($M_{ср}(УК)$). Согласно закону Авогадро, при одинаковых температуре и давлении отношение объемов газов равно отношению их количеств вещества:
$\frac{V(A)}{V(УК)} = \frac{n(A)}{n(УК)}$
Количество вещества $n$ можно выразить через массу $m$ и молярную массу $M$: $n = \frac{m}{M}$.
$\frac{V(A)}{V(УК)} = \frac{m(A)/M(A)}{m(УК)/M_{ср}(УК)}$
Так как по условию массы веществ равны ($m(A) = m(УК) = 1$ г), формула упрощается:
$\frac{V(A)}{V(УК)} = \frac{M_{ср}(УК)}{M(A)}$
Подставим известные значения:
$1.4 = \frac{M_{ср}(УК)}{60}$
$M_{ср}(УК) = 1.4 \cdot 60 = 84$ г/моль.
6. Рассчитаем относительную плотность паров уксусной кислоты по водороду.
$D_{H_2}(УК) = \frac{M_{ср}(УК)}{M(H_2)} = \frac{84}{2} = 42$.
Ответ: Относительная плотность паров вещества А по водороду равна 30; относительная плотность паров уксусной кислоты по водороду равна 42.
б) Какое количество молекул мономера приходится на 100 молекул димера в парах уксусной кислоты в условиях описанного эксперимента?
1. Пары уксусной кислоты состоят из мономеров ($CH_3COOH$) и димеров ($(CH_3COOH)_2$).
Молярная масса мономера: $M_{мон} = 60$ г/моль.
Молярная масса димера: $M_{дим} = 2 \cdot 60 = 120$ г/моль.
Средняя молярная масса паров уксусной кислоты, как мы рассчитали в пункте а), составляет $M_{ср}(УК) = 84$ г/моль.
2. Пусть $\chi_{мон}$ - мольная доля мономеров, а $\chi_{дим}$ - мольная доля димеров в газовой смеси. Сумма мольных долей равна 1:
$\chi_{мон} + \chi_{дим} = 1$
Средняя молярная масса смеси вычисляется по формуле:
$M_{ср} = \chi_{мон} \cdot M_{мон} + \chi_{дим} \cdot M_{дим}$
Подставим известные значения, выразив $\chi_{дим}$ через $\chi_{мон}$ ($\chi_{дим} = 1 - \chi_{мон}$):
$84 = \chi_{мон} \cdot 60 + (1 - \chi_{мон}) \cdot 120$
$84 = 60 \cdot \chi_{мон} + 120 - 120 \cdot \chi_{мон}$
$84 - 120 = 60 \cdot \chi_{мон} - 120 \cdot \chi_{мон}$
$-36 = -60 \cdot \chi_{мон}$
$\chi_{мон} = \frac{36}{60} = \frac{6}{10} = 0.6$
Тогда мольная доля димеров:
$\chi_{дим} = 1 - 0.6 = 0.4$
3. Отношение числа молекул мономера ($N_{мон}$) к числу молекул димера ($N_{дим}$) равно отношению их мольных долей:
$\frac{N_{мон}}{N_{дим}} = \frac{\chi_{мон}}{\chi_{дим}} = \frac{0.6}{0.4} = 1.5$
Это означает, что на каждую молекулу димера приходится 1.5 молекулы мономера. Чтобы найти, сколько молекул мономера приходится на 100 молекул димера, умножим это соотношение на 100:
$1.5 \cdot 100 = 150$
Таким образом, на 100 молекул димера приходится 150 молекул мономера.
Ответ: На 100 молекул димера приходится 150 молекул мономера.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10 класс, для упражнения номер 613 расположенного на странице 137 к сборнику задач 2021 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №613 (с. 137), авторов: Матулис (Вадим Эдвардович), Матулис (Виталий Эдвардович), Колевич (Татьяна Александровна), базовый и повышенный уровень обучения учебного пособия издательства Национальный институт образования.














