Номер 750, страница 169 - гдз по химии 10 класс сборник задач Матулис, Матулис

Авторы: Матулис В. Э., Матулис В. Э., Колевич Т. А.
Тип: Сборник задач
Издательство: Национальный институт образования
Год издания: 2021 - 2025
Уровень обучения: базовый и повышенный
Цвет обложки: синий
ISBN: 978-985-594-959-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 10 классе
Глава 3. Кислородсодержащие органические соединения. 3.5. Сложные эфиры. Жиры - номер 750, страница 169.
№750 (с. 169)
Условие. №750 (с. 169)
скриншот условия
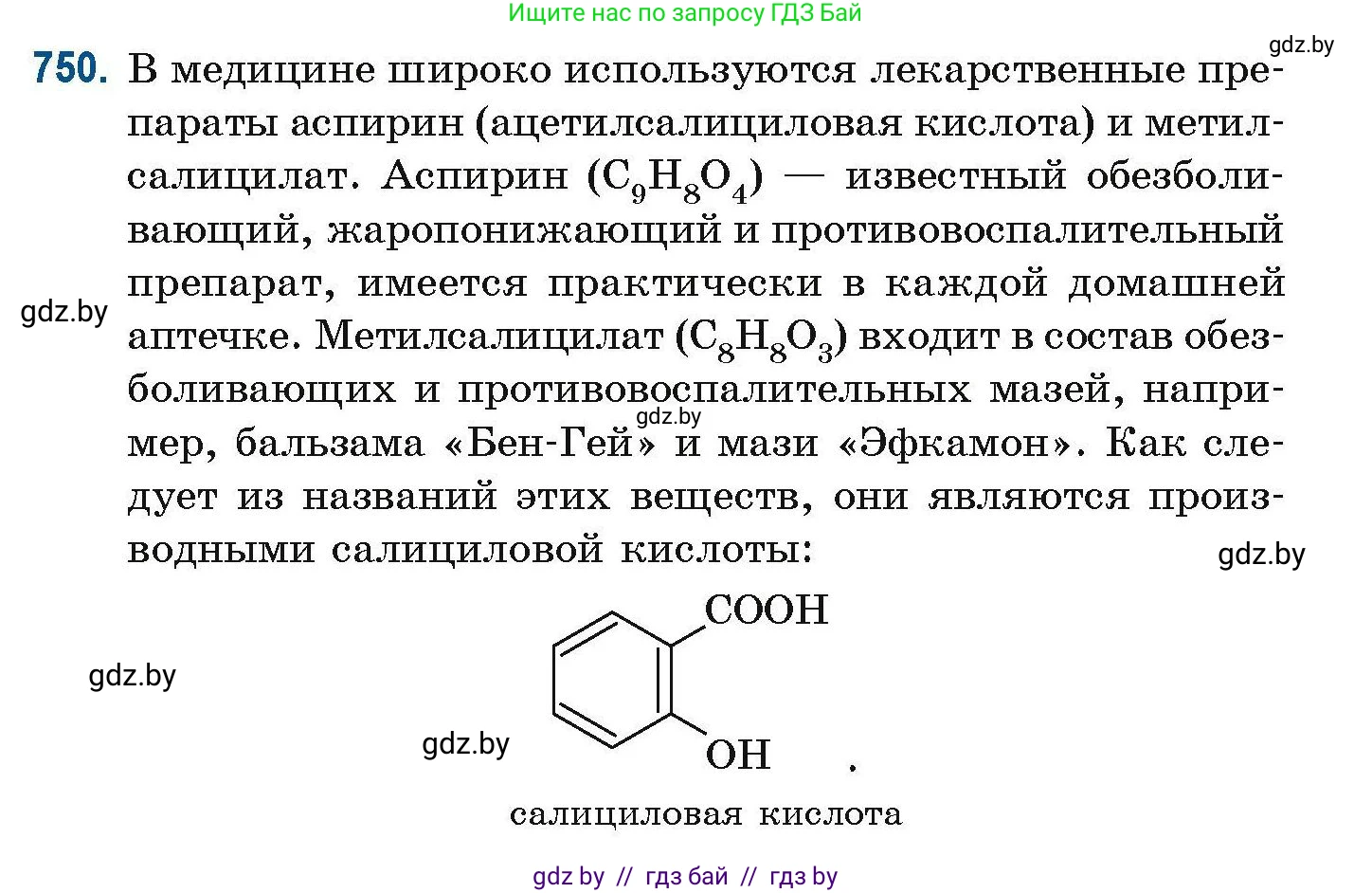

750. В медицине широко используются лекарственные препараты аспирин (ацетилсалициловая кислота) и метилсалицилат. Аспирин ($C_9H_8O_4$) — известный обезболивающий, жаропонижающий и противовоспалительный препарат, имеется практически в каждой домашней аптечке. Метилсалицилат ($C_8H_8O_3$) входит в состав обезболивающих и противовоспалительных мазей, например, бальзама «Бен-Гей» и мази «Эфкамон». Как следует из названий этих веществ, они являются производными салициловой кислоты:
${C6H4(COOH)(OH)}$
салициловая кислота
В молекуле салициловой кислоты имеются карбоксильная и гидроксильная группы, непосредственно связанные с бензольным кольцом. Она представляет собой белое кристаллическое вещество, хорошо растворимое в органических растворителях. В воде при температуре $20 \degree \text{C}$ ее растворимость составляет $0,18 \text{ г}$ на $100 \text{ г}$ воды, при нагревании растворимость увеличивается ($8,5 \text{ г}$ на $100 \text{ г}$ воды при $80 \degree \text{C}$).
Как видно из строения молекулы, салициловая кислота является бифункциональным соединением — карбоновой кислотой и фенолом.
а) Назовите салициловую кислоту по номенклатуре ИЮПАК.
б) Для очистки салициловой кислоты от хорошо растворимых в воде примесей $20,00 \text{ г}$ загрязненной салициловой кислоты полностью растворили в $250 \text{ мл}$ горячей воды (примерно $80 \degree \text{C}$). Затем раствор охладили до температуры $20 \degree \text{C}$, выпавший осадок отфильтровали. Какую максимальную массу очищенного вещества можно получить при этом?
в) Аспирин и метилсалицилат являются продуктами реакции этерификации салициловой кислоты. Какое из веществ — уксусная кислота либо метиловый спирт — используется в реакции этерификации для получения аспирина, а какое — для получения метилсалицилата?
г) Напишите уравнения реакций получения аспирина и метилсалицилата, учитывая, что катализатором является серная кислота (используйте структурные формулы веществ).
д) У аспирина имеется изомер, также являющийся сложным эфиром ароматической карбоновой кислоты, которая используется для синтеза синтетического волокна лавсан. Напишите его структурную формулу.
Решение. №750 (с. 169)

Решение 2. №750 (с. 169)
а) Назовите салициловую кислоту по номенклатуре ИЮПАК.
Согласно номенклатуре ИЮПАК, салициловая кислота называется 2-гидроксибензойная кислота. Нумерация атомов углерода в бензольном кольце начинается с атома, связанного с карбоксильной группой (-COOH), которая имеет старшинство перед гидроксильной группой (-OH).
Ответ: 2-гидроксибензойная кислота.
б) Для очистки салициловой кислоты от хорошо растворимых в воде примесей 20,00 г загрязненной салициловой кислоты полностью растворили в 250 мл горячей воды (примерно 80 °C). Затем раствор охладили до температуры 20 °C, выпавший осадок отфильтровали. Какую максимальную массу очищенного вещества можно получить при этом?
Дано:Масса загрязненной салициловой кислоты = 20,00 г
Объем воды $V_{воды}$ = 250 мл
Температура горячей воды $T_1$ = 80 °C
Температура холодной воды $T_2$ = 20 °C
Растворимость при 80 °C ($S_1$) = 8,5 г на 100 г воды
Растворимость при 20 °C ($S_2$) = 0,18 г на 100 г воды
Плотность воды $\rho_{воды}$ ≈ 1,0 г/мл
Максимальная масса очищенной салициловой кислоты ($m_{очищ}$) - ?
Решение:Метод очистки основан на перекристаллизации, которая использует различие в растворимости вещества при разных температурах.
1. Найдем массу воды, используемой для растворения. Принимая плотность воды равной 1 г/мл:
$m_{воды} = V_{воды} \cdot \rho_{воды} = 250 \text{ мл} \cdot 1 \text{ г/мл} = 250 \text{ г}$
2. Проверим, может ли 20,00 г салициловой кислоты полностью раствориться в 250 г воды при 80 °C. Рассчитаем максимальную массу салициловой кислоты, которую можно растворить в данном объеме горячей воды:
$m_{раств., 80°C} = \frac{8,5 \text{ г}}{100 \text{ г воды}} \cdot 250 \text{ г воды} = 21,25 \text{ г}$
Поскольку $20,00 \text{ г} < 21,25 \text{ г}$, вся салициловая кислота может раствориться (и, по условию, растворилась). Для расчета максимального выхода будем считать, что исходные 20,00 г - это масса чистой салициловой кислоты.
3. Рассчитаем, какая масса салициловой кислоты останется в растворе после охлаждения до 20 °C. Растворимость при этой температуре составляет 0,18 г на 100 г воды:
$m_{ост., 20°C} = \frac{0,18 \text{ г}}{100 \text{ г воды}} \cdot 250 \text{ г воды} = 0,45 \text{ г}$
4. Масса выпавшего в осадок (очищенного) вещества равна разности между исходной массой и массой, оставшейся в растворе. Предполагается, что примеси хорошо растворимы и остаются в растворе.
$m_{очищ} = m_{исходная} - m_{ост., 20°C} = 20,00 \text{ г} - 0,45 \text{ г} = 19,55 \text{ г}$
Ответ: Максимальная масса очищенной салициловой кислоты, которую можно получить, составляет 19,55 г.
в) Аспирин и метилсалицилат являются продуктами реакции этерификации салициловой кислоты. Какое из веществ — уксусная кислота либо метиловый спирт — используется в реакции этерификации для получения аспирина, а какое — для получения метилсалицилата?
Салициловая кислота имеет две функциональные группы: карбоксильную (-COOH) и фенольную гидроксильную (-OH). Реакция этерификации может идти по любой из них.
Для получения аспирина (ацетилсалициловой кислоты) необходимо этерифицировать фенольную гидроксильную группу (-OH). Для этого салициловую кислоту обрабатывают кислотой или ее ангидридом. Из предложенных вариантов, уксусная кислота ($CH_3COOH$) является источником ацетильной группы ($CH_3CO-$), необходимой для синтеза аспирина.
Для получения метилсалицилата (метилового эфира салициловой кислоты) этерифицируют карбоксильную группу (-COOH). Для этого используют спирт. Из предложенных вариантов, метиловый спирт ($CH_3OH$) реагирует с карбоксильной группой, образуя сложный эфир.
Ответ: Для получения аспирина используется уксусная кислота, для получения метилсалицилата — метиловый спирт.
г) Напишите уравнения реакций получения аспирина и метилсалицилата, учитывая, что катализатором является серная кислота (используйте структурные формулы веществ).
Уравнения реакций с использованием структурных формул (в конденсированном виде). Катализатор (серная кислота, $H_2SO_4$) указывается над стрелкой.
1. Получение аспирина (ацетилсалициловой кислоты). Происходит реакция этерификации фенольной группы салициловой кислоты уксусной кислотой:
$$ \underset{\text{салициловая кислота}}{HO-C_6H_4-COOH} + \underset{\text{уксусная кислота}}{CH_3COOH} \xrightarrow{H_2SO_4, t} \underset{\text{аспирин}}{CH_3COO-C_6H_4-COOH} + H_2O $$2. Получение метилсалицилата. Происходит реакция этерификации карбоксильной группы салициловой кислоты метиловым спиртом (реакция Фишера):
$$ \underset{\text{салициловая кислота}}{HO-C_6H_4-COOH} + \underset{\text{метиловый спирт}}{CH_3OH} \xrightarrow{H_2SO_4, t} \underset{\text{метилсалицилат}}{HO-C_6H_4-COOCH_3} + H_2O $$Ответ: Уравнения реакций приведены выше.
д) У аспирина имеется изомер, также являющийся сложным эфиром ароматической карбоновой кислоты, которая используется для синтеза синтетического волокна лавсан. Напишите его структурную формулу.
Сначала определим брутто-формулу аспирина (ацетилсалициловой кислоты). Его формула $C_9H_8O_4$.
Искомый изомер имеет ту же брутто-формулу $C_9H_8O_4$. По условию, это сложный эфир ароматической карбоновой кислоты, которая используется для синтеза лавсана.
Синтетическое волокно лавсан (полиэтилентерефталат, ПЭТ) получают поликонденсацией терефталевой кислоты и этиленгликоля. Следовательно, упомянутая ароматическая кислота — это терефталевая кислота (бензол-1,4-дикарбоновая кислота).
Структурная формула терефталевой кислоты: $HOOC-C_6H_4-COOH$. Её брутто-формула: $C_8H_6O_4$.
Сравним брутто-формулы изомера ($C_9H_8O_4$) и терефталевой кислоты ($C_8H_6O_4$). Разница составляет группу $CH_2$. Это указывает на то, что изомер является метиловым эфиром терефталевой кислоты. Так как у терефталевой кислоты две карбоксильные группы, искомый изомер является продуктом этерификации одной из них, то есть это монометиловый эфир терефталевой кислоты (монометилтерефталат).
Ответ: Структурная формула изомера (монометилтерефталата):
$$ HOOC-C_6H_4-COOCH_3 $$где карбоксильная (-COOH) и сложноэфирная (-COOCH3) группы находятся в пара-положении (1,4) относительно друг друга в бензольном кольце.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10 класс, для упражнения номер 750 расположенного на странице 169 к сборнику задач 2021 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №750 (с. 169), авторов: Матулис (Вадим Эдвардович), Матулис (Виталий Эдвардович), Колевич (Татьяна Александровна), базовый и повышенный уровень обучения учебного пособия издательства Национальный институт образования.














